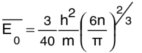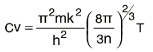This site is not complete. The work to converting the volumes of സര്വ്വവിജ്ഞാനകോശം is on progress. Please bear with us
Please contact webmastersiep@yahoo.com for any queries regarding this website.
Reading Problems? see Enabling Malayalam
ക്വാണ്ടംസിദ്ധാന്തം
സര്വ്വവിജ്ഞാനകോശം സംരംഭത്തില് നിന്ന്
ഉള്ളടക്കം |
ക്വാണ്ടം സിദ്ധാന്തം
Quantum Theory
ദ്രവ്യം, വിദ്യുത്കാന്തിക വികിരണം, ദ്രവ്യവും വികിരണവും തമ്മിലുള്ള അന്യോന്യക്രിയ, വസ്തുക്കളുടെ സൂക്ഷ്മാവസ്ഥയിലുള്ള ചില പ്രതിഭാസങ്ങള് മുതലായവയെക്കുറിച്ചുള്ള നവീനാശയം. ക്വാണ്ടം സിദ്ധാന്തത്തിന് ബലതന്ത്രം, ആപേക്ഷികീയ ബലതന്ത്രം, സാംഖ്യികം എന്നീ മൂന്നു പിരിവുകളുണ്ട്. ക്വാണ്ടം ബലതന്ത്രത്തിന് തരംഗബലതന്ത്രം (Wave Mechanics) എന്നും പേരുണ്ട്. ആപേക്ഷികതാ സിദ്ധാന്തത്തിന്റെ സ്വാധീനമാണ് ആപേക്ഷികീയ ബലതന്ത്രത്തില് അന്തര്ഭവിച്ചിരിക്കുന്നത്. സ്ഥിതിവിവരശാസ്ത്രത്തിന്റെ അതിസൂക്ഷ്മമായ പ്രയോഗമാണ് ക്വാണ്ടം സാംഖ്യികത്തിന്നാധാരം. 20-ാം ശതകത്തില് രൂപംകൊണ്ടു വികസിച്ച ഒരു ശാസ്ത്രശാഖയാണ് ക്വാണ്ടം സിദ്ധാന്തം. അതിനു മുമ്പുണ്ടായിരുന്ന ന്യൂട്ടന്റെ ക്ലാസ്സിക്കല് ബലതന്ത്രത്തിനും മാക്സ്വെല്ലിന്റെ വിദ്യുത്കാന്തിക സിദ്ധാന്ത(electromagnetic theory)ത്തിനും കൈകാര്യം ചെയ്യാന് കഴിയാതിരുന്ന അനേകം പ്രശ്നങ്ങളെ ഈ പുതിയ സിദ്ധാന്തം വിജയകരമായി വിശകലനം ചെയ്തെന്നു മാത്രമല്ല, സൂക്ഷ്മപ്രപഞ്ചത്തിന്റെ ചില വിചിത്രഭാവങ്ങള് വെളിപ്പെടുത്തുകയും ചെയ്തു.
ക്വാണ്ടം എന്ന ലാറ്റിന് പദത്തിന്റെ അര്ഥം അളവ് എന്നാണ്. എന്നാല് ഭൗതികവസ്തുക്കളുടെ ചില സൂക്ഷ്മാവസ്ഥകളെ വിവരിക്കാന് പര്യാപ്തമായ ഒരടിസ്ഥാനഘടകമെന്ന നിലയ്ക്കാണ് ഭൗതികശാസ്ത്രത്തില് ഈ പദം പ്രയോഗിച്ചുവരുന്നത്. 'ബലതന്ത്രം' എന്ന പദം ഒരു പ്രത്യേക ഗണിതപദ്ധതിയെ സൂചിപ്പിക്കുന്നു. സൂക്ഷ്മകണങ്ങളുടെ ബലതന്ത്രമാണ് ക്വാണ്ടം. ബലതന്ത്രം ചര്ച്ച ചെയ്യുന്നത്. ദ്രവ്യമാനം കൂടിയ പദാര്ഥങ്ങളുടെ കാര്യത്തില് അത് ക്ലാസ്സിക്കല് ബലതന്ത്രത്തിന്റെ രൂപംകൈക്കൊള്ളുന്നു.
നിലവിലുള്ള സിദ്ധാന്തങ്ങള്കൊണ്ടു പരിഹൃതമാകാത്ത പ്രശ്നങ്ങള് ഉദിക്കുമ്പോഴാണ് ശാസ്ത്രത്തില് പുതിയ സിദ്ധാന്തങ്ങള് രംഗത്തുവരുന്നത്. 20-ാം ശതകത്തിന്റെ തുടക്കത്തില്, ശാസ്ത്രജ്ഞന്മാരെ കുഴക്കിയിരുന്ന ചില പ്രശ്നങ്ങള് ഭൗതികശാസ്ത്രത്തെ ഒരു പ്രതിസന്ധിയിലെത്തിച്ചിരുന്നു. അവയിലൊന്ന് താപവികിരണത്തെ സംബന്ധിച്ചുള്ള പഠനങ്ങളില്നിന്നു രൂപംകൊണ്ടതായിരുന്നു. ക്ലാസ്സിക്കല് സിദ്ധാന്തങ്ങള് ഇവയെ സംബന്ധിച്ചിടത്തോളം അപര്യാപ്തമാണെന് തെളിഞ്ഞപ്പോള്, ശാസ്ത്രജ്ഞന്മാര് പുതിയ സിദ്ധാന്തങ്ങള്ക്കുവേണ്ടിയുള്ള അന്വേഷണമാരംഭിച്ചു.
ക്വാണ്ടം എന്ന സങ്കല്പം
ചൂടുള്ള വസ്തുക്കളുടെ സമീപത്തു ചെന്നാല് അവയില്നിന്നു പ്രസരിക്കുന്ന ചൂട് നമുക്കനുഭവപ്പെടുന്നു. വസ്തു അതിതപ്തമാണെങ്കില് ചൂടും വെളിച്ചവും അതു പ്രസരിപ്പിക്കും. ശാസ്ത്രജ്ഞന്മാര് വെളിച്ചത്തെ താപവികിരണത്തിന്റെ ഒരു ഭാഗമായിട്ടാണ് കരുതുന്നത്. താഴ്ന്ന താപനിലയിലുള്ള വസ്തുക്കളില്നിന്നു പൊതുവേ പ്രകാശം പുറപ്പെടുന്നില്ല. അതായത് നമ്മുടെ കണ്ണിന് ഉത്തേജനം നല്കാന് ശക്തിയുള്ള രശ്മികള് അവയില്നിന്നു പ്രസരിക്കുന്നില്ല. എങ്കിലും അവയുടെ താപനിലയ്ക്കനുസരിച്ചുള്ള വികിരണം അവയില് നടക്കുന്നുണ്ട്. വസ്തുവിന്റെ താപനിലയനുസരിച്ച് വികിരണത്തിന്റെ സ്വഭാവം മാറുന്നു. ഒരിരുമ്പുവടി തീയില് വച്ചാല്, തുടക്കത്തില് അതു കറുത്തിരിക്കുമെങ്കിലും ചൂടാകുമ്പോള് നിറം മാറുന്നതു കാണാം. ആദ്യം ചുവപ്പും പിന്നെ മഞ്ഞയും അവസാനം വെള്ളയുമായ പ്രകാശം അതു പ്രസരിപ്പിക്കുന്നു-പ്രകാശത്തിന്റെ നിറം തന്നെ അതിന്റെ താപനിലയെ സൂചിപ്പിക്കാന് പര്യാപ്തമാണ്. നേരിയ ചുവപ്പ് ഏകദേശം 500oC -ഉം മഞ്ഞ 800oC-ഉം വെണ്മ 1000oC-ഉം സൂചിപ്പിക്കുന്നു. താപനിലയ്ക്കനുസരിച്ച് വികിരണത്തിനുണ്ടാവുന്ന മാറ്റത്തിന് ഇതൊരുദാഹരണമാണ്.
വികിരണത്തെ സംബന്ധിച്ച് ചില നിയമങ്ങള് 19-ാം ശതകത്തില്ത്തന്നെ ശാസ്ത്രജ്ഞന്മാര് കണ്ടെത്തിയിരുന്നു. ഏറ്റവും ശക്തമായി താപവികിരണം പുറപ്പെടുവിക്കുന്ന കൃഷ്ണികകള് (black bodies) ആണ് പരീക്ഷണങ്ങള്ക്കായി അവര് സ്വീകരിച്ചത്. ഒരു (കറുത്ത) വസ്തുവിന്റെ പ്രസാരണശക്തി, അതായത് വികിരണ രൂപത്തില് അതില്നിന്ന് ഒരു സെക്കന്ഡില് ബഹിര്ഗമിക്കുന്ന ഊര്ജം ആ വസ്തുവിന്റെ കേവല താപനിലയുടെ നാലാംഘാതത്തിന് ആനുപാതികമാണെന്ന് ഒരു നിയമം (Stefan-Boltzmann law) പ്രസ്താവിക്കുന്നു. മറ്റൊരു നിയമം (Wein's displacement law) അനുശാസിക്കുന്നത്, വസ്തുവിന്റെ താപനില ഉയരുന്തോറും വികിരണത്തിലുള്ള ഏറ്റവും തീവ്രമായ തരംഗത്തിന്റെ ദൈര്ഘ്യം കുറഞ്ഞുവരുമെന്നാണ്. ഈ നിയമങ്ങളെ ഏകീകരിക്കാന് ബ്രിട്ടീഷ് ശാസ്ത്രജ്ഞന്മാരായ റാലേയും ജീന്സും ശ്രമിച്ചു. പക്ഷേ അവര് കണ്ടെത്തിയ നിയമം (Rayleigh-Jeans law) പുതിയൊരു പ്രശ്നം സൃഷ്ടിച്ചു. ഈ നിയമമനുസരിച്ച് തപ്തമായ വസ്തുവിന്റെ വികിരണത്തില് തരംഗദൈര്ഘ്യം കുറയുന്നതനുസരിച്ച് പ്രസാരണശക്തി ക്രമാതീതമായി വര്ധിച്ചുവരുന്നു. എന്നാല് അങ്ങനെയുള്ള അപരിമേയമായ വികിരണ വര്ധന പ്രകൃതിയില് സംഭവിക്കുന്നില്ല. ക്ലാസ്സിക്കല് ഭൗതികത്തിലെ വികിരണസിദ്ധാന്തം ഇങ്ങനെയൊരു പ്രതിസന്ധിയിലെത്തി. വികിരണത്തെ സംബന്ധിച്ച മൗലികധാരണകളില് സാരമായ എന്തോ ന്യൂനതയുണ്ടെന്നു വ്യക്തമായി. ഇതിനു പരിഹാരമായി 1900-ത്തില് ക്വാണ്ടം എന്ന സങ്കല്പം മാക്സ് പ്ലാങ്ക് (Max Planck) അവതരിപ്പിച്ചു.
ഒരു വസ്തുവിന്റെ താപനില എന്നത് അതിലടങ്ങിയിട്ടുള്ള ഊര്ജസഞ്ചയത്തിന്റെ ഒരു സൂചകമാകുന്നു. അതിലുള്ള തന്മാത്രകളുടെ കമ്പനങ്ങളായിട്ടാണ് ഊര്ജം പ്രത്യക്ഷപ്പെടുന്നത്. തന്മാത്രകള് വൈദ്യുതചാര്ജുകളുടെ ഇരിപ്പിടമായതിനാല് കമ്പനങ്ങള്കൊണ്ട് ഈ ചാര്ജുകള് നിരന്തരമായ ചലനത്തിനു വിധേയമാവുകയും അവയില്നിന്നു വൈദ്യുത കാന്തികതരംഗങ്ങള് ഉദ്ഭവിക്കുകയും ചെയ്യുന്നു. ഇതായിരുന്നു ക്ലാസ്സിക്കല് സിദ്ധാന്തം. കമ്പിതവസ്തുക്കളില്നിന്ന് വായുവില് പരക്കുന്ന ശബ്ദതരംഗങ്ങളുടെ പ്രസരണത്തോട് സാദൃശ്യമുള്ള ഒരു പ്രക്രിയയായി താപപ്രസരണവും കരുതപ്പെട്ടിരുന്നു. ഇങ്ങനെ ചുറ്റുപാടും തരംഗരൂപത്തില് വ്യാപിക്കുന്ന താപോര്ജം, വെള്ളം ഒഴുകുന്നതുപോലെ ഒരു അവിച്ഛിന്ന ധാരയായി സംഭവിക്കുകയാണ്. ഒരു തരംഗം വഹിക്കുന്ന ഊര്ജപരിമാണത്തിന് പൂജ്യം മുതല് അനന്തതവരെ ഏതു മൂല്യവുമാകാം. ഈ സങ്കല്പമാണ് പ്ലാങ്ക് തിരുത്തിയത്. ഏതു പരിതഃസ്ഥിതിയിലായാലും ഊര്ജം ഒരടിസ്ഥാനമാത്രയുടെ ഗുണിതങ്ങളായിട്ടാണ് പ്രത്യക്ഷപ്പെടുന്നത്. ഓരോ തരംഗവും അതിന്റെ ആവൃത്തിയനുസരിച്ച് ഊര്ജത്തിന്റെ അടിസ്ഥാനമാത്രകളെ സംവഹിക്കുന്നു. അതായത്, തരംഗങ്ങള് ഊര്ജകണങ്ങളെ പ്രതിനിധാനം ചെയ്യുന്നു. ഈ അടിസ്ഥാനമാത്രകള്ക്ക് ക്വാണ്ടം എന്നു പേര്. തരംഗത്തോടൊപ്പം നീങ്ങുന്ന ഊര്ജം ഇത്തരം ക്വാണ്ടങ്ങളുടെ ശൃംഖലയാണ്. തരംഗത്തിന്റെ ആവൃത്തി (ν)യും, ക്വാണ്ടത്തിന്റെ ഊര്ജ(E)വും തമ്മില് ബന്ധിപ്പിക്കുന്ന സമവാക്യം E=h ν ആണെന്ന് പ്ലാങ്ക് സങ്കല്പിച്ചു. 'h' എന്നത് ഒരു സ്ഥിരാങ്കം (പ്ലാങ്ക് സ്ഥിരാങ്കം) ആണ്. തരംഗം ഏതായാലും h-നു മാറ്റമില്ല. അതിന്റെ മൂല്യം അതീവസൂക്ഷ്മമാണ്. 6.67 x 10-34 J.S. ഇതിനാല് ഓരോ ക്വാണ്ടത്തിന്റെയും ഊര്ജം എപ്പോഴും നിസ്സാരമാകുന്നു.
ക്വാണ്ടങ്ങളെ വേറിട്ടു കാണാനുള്ള കഴിവ് മനുഷ്യദൃഷ്ടികള്ക്കില്ല. ഇതിനുകാരണം ഒരുദാഹരണംകൊണ്ടു വ്യക്തമാക്കാം. 25 വാട്ട് ശക്തിയുള്ള ഒരു വൈദ്യുതബള്ബിന്റെ പ്രകാശത്തില് ഓരോ സെക്കന്ഡിലും പുറപ്പെടുന്നത് ഏകദേശം 1019 ക്വാണ്ടമാണ്. ഇപ്രകാരം അതിദ്രുതമായ ഊര്ജകണപ്രവാഹം അവിച്ഛിന്നമായ ഒരു ഊര്ജധാരയാണെന്നേ നമുക്കു തോന്നുകയുള്ളൂ.
വികിരണം മേല്പറഞ്ഞ വിധത്തില് കണികാരൂപത്തിലാണു പ്രസരിക്കുന്നതും അവശോഷണം ചെയ്യപ്പെടുന്നതുമെന്ന തത്ത്വം ഉള്ക്കൊള്ളിച്ചുകൊണ്ട് വികിരണ സിദ്ധാന്തം തിരുത്തിയപ്പോള് പരീക്ഷണങ്ങളോട് അതു യോജിച്ചുവന്നു. മാത്രമല്ല, പ്രകാശ വിദ്യുത്പ്രഭാവത്തെ (Photo eletric effect) സംബന്ധിച്ച് 1905-ല് ഐന്സ്റ്റൈന് നല്കിയ വിശദീകരണവും ക്വാണ്ട സങ്കല്പത്തിന് ഉപോദ്ബലകമായിത്തീര്ന്നു. ചില ലോഹങ്ങളില് പ്രകാശം പതിക്കുമ്പോള് അവയില്നിന്ന് ഇലക്ട്രോണുകള് നിഷ്കാസിതമാകുന്നു. ഇതാണ് പ്രകാശവിദ്യുത്പ്രഭാവം. പ്രകാശം നല്കുന്ന ഊര്ജം ഉള്ക്കൊള്ളുന്നതുകൊണ്ടാണ് ഇലക്ട്രോണുകള്ക്ക് ലോഹത്തിലെ ആകര്ഷണമണ്ഡലത്തില്നിന്നു ബഹിര്ഗമിക്കാന് ശക്തി ലഭിക്കുന്നത്. പ്രകാശം തീവ്രമാണോ അല്ലയോ എന്നുള്ളതല്ല ഈ പ്രക്രിയയെ നിയന്ത്രിക്കുന്നത്. പ്രകാശത്തിലെ ക്വാണ്ടം നല്കുന്ന ഊര്ജത്തിന്റെ വലുപ്പമാണ് പ്രധാനം. തരംഗദൈര്ഘ്യം കൂടിയിരുന്നാല് ക്വാണ്ടം ദുര്ബലമായിരിക്കും. അത്തരം തരംഗങ്ങള്ക്കു മേല്പറഞ്ഞ പ്രഭാവം സൃഷ്ടിക്കാന് കഴിവുണ്ടാകില്ല. ഏതായാലും പരീക്ഷണങ്ങള്കൊണ്ട് സ്ഥാപിതമായ വസ്തുത, പ്രകാശത്തിലടങ്ങിയിട്ടുള്ളത് പ്രകാശകണങ്ങളാണെന്നതായിരുന്നു. ന്യൂട്ടന് ആവിഷ്കരിച്ച പ്രകാശകണസിദ്ധാന്തത്തിനോട് ഈ ആശയം യോജിച്ചു. പ്രകാശകണങ്ങള് ഫോട്ടോണ് എന്ന പേരില് വ്യവഹരിക്കപ്പെടാനും തുടങ്ങി.
ഇവിടെ മറ്റൊരു വൈഷമ്യം പൊന്തിവന്നു. വ്യതികരണം (interference), വിഭംഗനം (diffraction), ധ്രുവണം (polarisation) എന്നീ പ്രതിഭാസങ്ങള് പ്രകാശം പ്രകടിപ്പിച്ചിരുന്നതില്നിന്ന്, പ്രകാശം തരംഗരൂപത്തിലാണ് സഞ്ചരിക്കുന്നതെന്നു 19-ാം ശതകത്തില്ത്തന്നെ സ്ഥാപിതമായിരുന്നു. ഇത് ക്വാണ്ട സങ്കല്പത്തിനു നിരക്കുന്നതല്ല. പ്രകാശം ഒരേസമയം കണികയും തരംഗവുമാകുന്നതെങ്ങനെ? ഇതായി ശാസ്ത്രജ്ഞന്മാരുടെ പിന്നത്തെ പ്രശ്നം.
ദ്രവ്യതരംഗങ്ങള്
പ്രകാശതരംഗങ്ങളെ സംബന്ധിച്ച് മറ്റൊരു രീതിയിലുള്ള ഗവേഷണം ഇതോടൊപ്പം വികസിച്ചു വന്നിരുന്നു. വര്ണരാജിപഠനം (spectroscopy) ആയിരുന്നു അത്. തത്ഫലമായി ഓരോ വസ്തുവും അതിന്റേതായ സവിശേഷതകളോടുകൂടിയ വര്ണരാജി സൃഷ്ടിക്കുന്നു എന്ന് സ്ഥാപിക്കപ്പെട്ടു. അതായത് ഓരോ വസ്തുവിനും അനുകൂലമായ ഉത്തേജനം ലഭിച്ചാല്, പ്രത്യേക തീവ്രതയോടുകൂടിയ പ്രത്യേക പ്രകാശതരംഗങ്ങള് ഉത്സര്ജിക്കാന് കഴിയും. പക്ഷേ ഈ പ്രക്രിയ എങ്ങനെയാണ് സംഭവിക്കുന്നതെന്നു ശാസ്ത്രജ്ഞര്ക്കു വ്യാഖ്യാനിക്കാന് കഴിഞ്ഞിരുന്നില്ല. പ്രകാശം പുറപ്പെടുവിക്കുമ്പോള് അണുവിന്റെ ഉള്ളിലെന്താണു സംഭവിക്കുന്നത്? ഊര്ജമാണ് അണുവില്നിന്ന് പ്രസരിക്കുന്നത്. പക്ഷേ ആ ഊര്ജത്തിനു പ്രത്യേക ക്രമീകരണമുണ്ടെന്നു വ്യക്തമാണ്. കാരണം, ഊര്ജത്തെ പ്രതിനിധാനം ചെയ്യുന്ന തരംഗങ്ങള് പ്രത്യേക തരംഗദൈര്ഘ്യമുള്ളവയാണ്. ഈ പ്രക്രിയ വിവരിക്കുവാന് ആദ്യമായി ഒരു സിദ്ധാന്തം നിര്ദേശിച്ചത് നീല്സ് ബോര് (Niels Bohr) ആയിരുന്നു. ഊര്ജത്തിന്റെ നിശ്ചിതമായ ചില അളവുകള് മാത്രമേ സാധാരണരീതിയില് അണുവില്നിന്നു പുറത്തുപോകുന്നുള്ളൂ. പ്രകാശം അണുവില് വിലയിക്കുന്ന സന്ദര്ഭങ്ങളിലും ഇതേ തോതില് ക്ളിപ്തമായ ഊര്ജപരിണാമമാണ് അത് ഉള്ക്കൊള്ളുന്നത്. ഇതിനര്ഥം അണുവിനു ചില പ്രത്യേകമായ ഊര്ജനിലകളില് മാത്രമേ വര്ത്തിക്കാനാവൂ എന്നാണെന്ന് ബോര് സങ്കല്പിച്ചു. അനുസ്യൂതമായ ഊര്ജപരിമാണം ഇവിടെ സ്വീകരിക്കാന് സാധ്യമല്ല. പ്ലാങ്കിന്റെ ക്വാണ്ടം സിദ്ധാന്തം ഇവിടെ പ്രായോഗികമാക്കാമെന്നു ബോര് കണ്ടെത്തി. അണുവിന്റെ ഉള്ളിലെ ഘടന കേന്ദ്രത്തിലൊരു ന്യൂക്ളിയസ്സും അതിനു ചുറ്റും കറങ്ങിക്കൊണ്ടിരിക്കുന്ന ഇലക്ട്രോണുകളും ഉള്ക്കൊള്ളുന്നതാണ്. സാധാരണ പ്രകാശത്തെ സംബന്ധിച്ചിടത്തോളം ഏറ്റവും പുറത്തുള്ള ഭ്രമണപഥത്തില് ചലിക്കുന്ന ഇലക്ട്രോണ് ആണ് ശ്രദ്ധേയമായിട്ടുള്ളത്. ഈ ഇലക്ട്രോണ്, പ്രകാശം ഉള്ക്കൊള്ളുന്ന അവസരത്തില് ന്യൂക്ളിയസ്സില് നിന്ന് കൂടുതല് അകന്ന ഭ്രമണപഥങ്ങളിലേക്കു ചാടുന്നു. പ്രകാശം ഉത്സര്ജിക്കുമ്പോഴാകട്ടെ ഉയര്ന്ന ഭ്രമണപഥങ്ങളില്നിന്നു താഴ്ന്ന ഭ്രമണപഥങ്ങളിലേക്കും പതിക്കുന്നു. ഓരോ ഭ്രമണപഥവും ഓരോ ഊര്ജസ്തര(energy level)ത്തെ സൂചിപ്പിക്കുന്നു. ഒരു ഭ്രമണപഥത്തില്ത്തന്നെ സ്ഥിരമായി ചലിച്ചുകൊണ്ടിരിക്കുമ്പോള് ഇലക്ട്രോണിന് ഊര്ജമാറ്റമില്ല. അതു പ്രകാശം പ്രസരിപ്പിക്കുകയുമില്ല. ഒരു പഥത്തില് നിന്നു മറ്റൊരു പഥത്തിലേക്കു മാറുമ്പോഴാണ് ഇലക്ട്രോണ് പ്രകാശം ഉത്സര്ജിക്കുകയോ ഉള്ക്കൊള്ളുകയോ ചെയ്യുന്നത്. ഇതായിരുന്നു ബോറിന്റെ സങ്കല്പം.
E1 എന്ന ഊര്ജമൂല്യമുള്ള ഒരു പഥത്തില്നിന്ന് E2 എന്ന മറ്റൊരു പഥത്തിലേക്കു വീഴുമ്പോള് അണുവിന് അഥവാ ഇലക്ട്രോണിന് ഉത്പാദിപ്പിക്കാന് കഴിയുന്ന തരംഗത്തിന്റെ ഊര്ജം E1 - E2 ആയിരിക്കും. ക്വാണ്ടം സിദ്ധാന്തമനുസരിച്ച് തരംഗത്തിന്റെ ആവൃത്തി ν ആണെങ്കില് E1 - E2 = h ν വവ്യത്യസ്തമായ ഊര്ജസ്തരങ്ങള് തമ്മില് സംക്രമണം ഉണ്ടാകുമ്പോള് വ്യത്യസ്ത തരംഗങ്ങള് ഉണ്ടാവുമെന്ന് ഇതില്നിന്നു വ്യക്തമാകുന്നു. വര്ണരാജിയിലെ രേഖകളെ ഈ രീതിയില് വ്യാഖ്യാനിക്കുവാന് ബോര്സിദ്ധാന്തത്തിന് ഏറെക്കുറെ സാധിച്ചു. എങ്കിലും ചില തരംഗങ്ങള് മറ്റുള്ളവയെക്കാള് തീവ്രമോ ദുര്ബലമോ ആവുന്നതെങ്ങനെയെന്നു തൃപ്തികരമായി വിശദീകരിക്കുവാന് ആ സിദ്ധാന്തം അപര്യാപ്തമായിരുന്നു. ഇലക്ട്രോണിനെ ഒരു കണികയായും അതിന്റെ സഞ്ചാരപഥങ്ങളെ നിശ്ചിത വൃത്തപഥങ്ങളായും സങ്കല്പിച്ചത് ഒരു ഏകദേശനം മാത്രമാണെന്നു പിന്നീടുണ്ടായ ചില കണ്ടുപിടിത്തങ്ങള് തെളിയിച്ചു.
ക്വാണ്ടം സിദ്ധാന്തത്തിന്റെ മുന്നോട്ടുള്ള കാല്വയ്പ് പിന്നീടുണ്ടായത് ദ്രവ്യതരംഗങ്ങ (matter waves)ളുടെ കണ്ടുപിടിത്തത്തോടെയാണ്. ദ്രവ്യതരംഗങ്ങളെപ്പറ്റി ആദ്യമായി (1924) ലൂയി ദ് ബ്രോയ് (Louis de Broglie) പ്രതിപാദിച്ചു. തികച്ചും നൂതനമായ ഒരാശയമായിരുന്നു അത്. ചലിക്കുന്ന ഏതൊരു വസ്തുവിനോടും അത് ചെറുതോ വലുതോ ആകാം - അനുബന്ധിച്ച് ദ്രവ്യതരംഗങ്ങള് ഉണ്ടായിരിക്കുമെന്ന് ലൂയി ദ് ബ്രോയ് സമര്ഥിച്ചു. വൈദ്യുതാധാനമില്ലാത്ത വസ്തുക്കളും ഇവയെ പ്രസരിപ്പിക്കുന്നതിനാല്, ഇവ വൈദ്യുതകാന്തതരംഗങ്ങളല്ല. സാധാരണ ശബ്ദതരംഗങ്ങള് ശ്രവണേന്ദ്രിയത്തിലും വൈദ്യുതകാന്തതരംഗങ്ങള് നേത്രത്തിലും പ്രതികരണങ്ങളുണ്ടാക്കുന്നു. പക്ഷേ ദ്രവ്യതരംഗങ്ങള് ഇത്തരത്തിലൊന്നും പെടാത്തതിനാല് അവയെ നേരിട്ടറിയാന് സാധ്യമല്ല.
ദ് ബ്രോഗ്ലി തരംഗങ്ങളുടെ ദൈര്ഘ്യത്തെ λ = h/mν എന്ന സമവാക്യം സൂചിപ്പിക്കുന്നു. λ എന്നതു തരംഗദൈര്ഘ്യവും m വസ്തുവിന്റെ ദ്രവ്യമാനവും ν പ്രവേഗവുമാകുന്നു; h പ്ലാങ്കിന്റെ സ്ഥിരാങ്കവും. ഈ സമീകരണത്തില്നിന്നു വ്യക്തമാകുന്നത് ദ്രവ്യതരംഗങ്ങള്ക്കു ക്വാണ്ടം സ്വഭാവമുണ്ടെന്നാണ്. സാധാരണ വസ്തുക്കളെ സംബന്ധിച്ചിടത്തോളം തരംഗദൈര്ഘ്യം നിസ്സാരമാണുതാനും. ഒരു കിലോഗ്രാം ദ്രവ്യമാനമുള്ളതും സെക്കന്ഡില് ഒരു മീ. പ്രവേഗത്തോടെ ചലിക്കുന്നതുമായ ഒരു കല്ലിന്റെ തരംഗദൈര്ഘ്യം
ആകുന്നു. യാതൊരു ഉപകരണത്തിനും ഇത്ര ചെറിയ തരംഗദൈര്ഘ്യം അളന്നു തിട്ടപ്പെടുത്താന് സാധ്യമല്ല. പക്ഷേ വസ്തുവിന്റെ ദ്രവ്യമാനം വളരെ ചെറുതായിരുന്നാല് തരംഗദൈര്ഘ്യം വലുതാകാനിടയുണ്ട്. അങ്ങനെ ഇലക്ട്രോണുകളുടെ ചലനത്തിലുള്ള തരംഗങ്ങള് മാപനക്ഷമമാണ്. ഇലക്ട്രോണ് തരംഗങ്ങള് മറ്റു തരംഗങ്ങളെപ്പോലെതന്നെ ഉചിതമായ സംവിധാനത്തില് വിഭംഗനരൂപങ്ങള് സൃഷ്ടിക്കുവാന് പര്യാപ്തമാണെന്നു പിന്നീട് തെളിഞ്ഞു. ദ്രവ്യതരംഗങ്ങളുടെ അസ്ഥിത്വം അതോടെ സ്ഥാപിതമായി. ഇലക്ട്രോണ് ഒരു കണിക മാത്രമല്ല; തരംഗസ്വഭാവം കൂടി അതിനുണ്ട്. ചെറുതും വലുതുമായ ഏതു വസ്തുവിനും ഈ ദ്വന്ദ്വഭാവം പ്രസക്തവുമാണ്. പക്ഷേ ദ്രവ്യമാനം ലഘുവായിരിക്കുന്ന വസ്തുക്കളടങ്ങുന്ന സൂക്ഷ്മലോകത്തില് മാത്രമേ അത് പ്രകടമാകുന്നുള്ളൂ. ബോറിന്റെ സിദ്ധാന്തമനുസരിച്ച് ഇലക്ട്രോണ് ഒരു നിശ്ചിതരൂപത്തില് ഒതുങ്ങി നില്ക്കുന്ന കണികയും അതിന്റെ ചലനം വ്യക്തമായ ഒരു പഥവുമാണ്. ദ്രവ്യതരംഗസങ്കല്പം ആവിര്ഭവിച്ചപ്പോള് ഈ വാദത്തിന് നിലനില്പില്ലാതായി. ഈവിധമാണ് ക്വാണ്ടം മെക്കാനിക്സിന്റെ ആവിര്ഭാവം. വിപുലവും ഗണിതസങ്കല്പങ്ങള്കൊണ്ടു സങ്കീര്ണവുമായ ഈ ശാസ്ത്രശാഖയുടെ ഒരു ഏകദേശ രൂപവും ചില പ്രയോഗഫലങ്ങളും ഇനി ചുരുക്കി വിവരിക്കുന്നു.
ക്വാണ്ടം ബലതന്ത്രം
പരീക്ഷണങ്ങളിലൂടെ ദ്രവ്യതരംഗങ്ങളെ കണ്ടെത്തുന്നതിനു മുമ്പുതന്നെ പുതിയൊരു ബലതന്ത്രമാതൃക ആവിഷ്കരിക്കുവാന് പല ശാസ്ത്രജ്ഞരും കിണഞ്ഞു പരിശ്രമിച്ചിരുന്നു. ഈ മാതൃകയില്, കണികകളുടെ ചലനത്തെ പ്രതിപാദിക്കുമ്പോള് അവയുടെ തരംഗസ്വഭാവംകൂടി ഉള്പ്പെടുത്തുകയാണ് വേണ്ടിയിരുന്നത്. ഇതിലാദ്യമായി എര്വിന് ഷ്റോഡിങ്ഗറും (Erwin Schroedinger) വെര്നര് ഹൈസന് ബെര്ഗും (Werner Heisenberg) വിജയം നേടി. ക്വാണ്ടം ബലതന്ത്രത്തെ ഹൈസന്ബെര്ഗ് ഒരു മാട്രിക്സ് രൂപത്തിലൂടെ അവതരിപ്പിച്ചപ്പോള് ഷ്റോഡിങ്ഗര് ഒരു തരംഗസമവാക്യ (wave equation)ത്തെയാണ് അതിനവലംബിച്ചത്. രൂപം വ്യത്യസ്തമാണെങ്കിലും ഫലത്തില് രണ്ടും തുല്യമാണ്. പക്ഷേ ഷ്റോഡിങ്ഗറുടെ രീതിയാണ് പ്രയോഗ വൈപുല്യത്തിലും സങ്കല്പന ലാളിത്യത്തിലും മുന്നിട്ടുനിന്നത്. അതുകൊണ്ട് അതിനെപ്പറ്റിമാത്രം ഇവിടെ പ്രസ്താവിക്കാം.
ഒരു കണികയെ പരീക്ഷണവിധേയമാക്കുമ്പോള് നിരീക്ഷിക്കപ്പെടുന്നത് അതിനെ സംബന്ധിക്കുന്ന ഒരു വിവരം-സ്ഥാനമോ സംവേഗമോ ഊര്ജമോ മറ്റോ-ആയിരിക്കും. ഈ രാശികളെല്ലാം കണികയെ സംബന്ധിക്കുന്ന സമീകരണങ്ങളില് അതേപടി ഉള്പ്പെടുത്തുകയാണ് ക്ലാസ്സിക്കല് ബലതന്ത്രത്തിന്റെ രീതി. പക്ഷേ ക്വാണ്ടം ബലതന്ത്രത്തില് ഇവയ്ക്കെല്ലാം പ്രാതിനിധ്യം വഹിച്ചുകൊണ്ടുള്ള ഒരു തരംഗഫലനം (wave function ) ഷ്റോഡിങ്ഗര് സങ്കല്പിച്ചു (1926). ψ എന്ന ഗ്രീക്കക്ഷരം കൊണ്ടാണ് പൊതുവേ ഇതിനെ സൂചിപ്പിച്ചുവരുന്നത്. ഒരു കണികയുടെ തരംഗഫലനം എന്താണെന്നു കണ്ടെത്തിയാല് അതില്നിന്നു മറ്റു വിവരങ്ങള് ഗണിച്ചെടുക്കാനുള്ള ഉപായങ്ങളുണ്ട്. ആദ്യമായി തരംഗഫലനം ഉള്പ്പെടുന്ന ഒരു സമവാക്യം രചിക്കുകയും നിര്ധാരണം വഴി, അതു കണ്ടെത്തുകയും വേണം. ഈ സമവാക്യം ഒരു തരംഗഫലനത്തിന്റെ ദ്വിതീയ ക്രമത്തിലുള്ള ഭാഗികാവകലന സമവാക്യം (Second order partial differential equation) ആണെന്നു ഷ്റോഡിങ്ഗര് സമര്ഥിച്ചു. ഇതിനെ 'ഷ്റോഡിങ്ഗര് സമവാക്യം' എന്നു വിളിക്കുന്നു. പൊതുവേ ഈ സമവാക്യത്തെ നിര്ധാരണം ചെയ്യുക എളുപ്പമല്ല. എങ്കിലും ചില പ്രത്യേക പ്രശ്നങ്ങളെ സംബന്ധിച്ചിടത്തോളം അതിന്റെ പൂര്ണമായ നിര്ധാരണം സാധിച്ചിട്ടുണ്ട്.
ഷ്റോഡിങ്ഗര് സമവാക്യത്തിലുള്ള അജ്ഞാതരാശിയാണ് തരംഗഫലനം. ഇതുപയോഗിച്ച് അനേകം പ്രതിഭാസങ്ങളെ വിശദീകരിക്കുവാന് ശാസ്ത്രജ്ഞര്ക്കു കഴിഞ്ഞിട്ടുണ്ടെങ്കിലും തരംഗഫലനത്തിന്റെ യഥാര്ഥമായ അര്ഥം അജ്ഞാതമാണ്. ദ്രവ്യതരംഗത്തോടു ബന്ധപ്പെട്ട ഒരു ഗണിതരാശിയാണിത്. ഇതിന്റെ വര്ഗം സംഭാവ്യതയെ (probability) സൂചിപ്പിക്കുന്നു. ഏതെങ്കിലും ഒരു സ്ഥാനത്ത് കണികയെ കണ്ടെത്താനുള്ള സാധ്യത ഈ സംഭാവ്യതയെ അടിസ്ഥാനപ്പെടുത്തിയാണ് നിലകൊള്ളുന്നത്. സംഭാവ്യതയ്ക്ക് ഏറ്റവുമധികം മൂല്യമുള്ള സ്ഥാനത്തായിരിക്കും കണികയെ കണ്ടെത്താന് ഏറ്റവുമധികം സാധ്യതയുള്ളത്. ഒരു കണികയുടെ സ്ഥാനത്തിനു നിഷ്കൃഷ്ടമായ ഒരു സ്ഥാനം ഇവിടെ കല്പിക്കപ്പെട്ടിട്ടില്ല-ക്ലാസ്സിക്കല് ബലതന്ത്രത്തിലുള്ളതുപോലെ. കണികയുടെ സ്ഥാനം സ്പേസില് വ്യാപിച്ചു നില്ക്കുന്നതായിട്ടാണ് കരുതപ്പെടുന്നത്. പക്ഷേ ചിലടത്തു സംഭാവ്യത കൂടുതലായിരിക്കും. മറ്റു ചിലടത്ത് കുറവോ പൂജ്യമോ ആകാം. കണികയുടെ രൂപവും സ്ഥാനവും ഈ സിദ്ധാന്തത്തില് അവ്യക്തമാണ്. സാംഖ്യികീയമായ (statistical) അടിസ്ഥാനത്തില് മാത്രമേ വ്യക്തമായ പരിമാണ മൂല്യങ്ങള് കണികയ്ക്ക് നല്കാനാവുകയുള്ളൂ. പ്രപഞ്ചത്തിലെ പ്രതിഭാസങ്ങളുടെ സൂക്ഷ്മവശങ്ങള് അവ്യക്തമാണെന്നും സ്ഥൂലമായ സാമാന്യബുദ്ധിയ്ക്ക് വിചിത്രമായി തോന്നാവുന്ന തരത്തിലുള്ള പ്രത്യേകതകള് അവയ്ക്കുണ്ടെന്നും ക്വാണ്ടം ബലതന്ത്രം ചൂണ്ടിക്കാട്ടുന്നു.
തരംഗഫലനത്തെ സംബന്ധിച്ചുള്ള പൊതുവിവരങ്ങളാണ് മുകളില് നല്കിയത്. കുറേക്കൂടി ഇക്കാര്യം വിശദീകരിക്കുവാന് ഗണിതസംജ്ഞകളെ സ്വീകരിക്കേണ്ടതുണ്ട്. ഷ്റോഡിങ്ഗര് സമവാക്യത്തെ ഏറ്റവും ലളിതമായി എഴുതാവുന്ന രീതി H ψ = E ψ എന്നാണ്; E കണികയുടെ (അല്ലെങ്കില് ഏതെങ്കിലും വ്യവസ്ഥയുടെ) ഊര്ജതുല്യമാണ്. സാധാരണയായി പരീക്ഷണങ്ങളില് നിന്നു ലഭിക്കുന്ന രാശി (സംഖ്യ)യാണിത്. H എന്നത് സ്ഥിത (static)വും ഗതിജ(dynamic)വുമായ ഊര്ജങ്ങളുടെ ആകെത്തുകയ്ക്ക് പ്രാതിനിധ്യം നല്കിക്കൊണ്ടുള്ള ഒരു സംകാരകം (operator) ആകുന്നു. ഗണിതഭാഷയില് ψ ഒരു 'ഐഗന്ഫലന'വും (eigen function), E ഒരു 'ഐഗന്മൂല്യ'വുമാണ്. ഈ സമീകരണത്തിന്റെ നിര്ധാരണത്തില് നിന്നാണ് ψ കണ്ടെത്തുന്നത്. ഇതിനു സഹായകമായി സീമാന്ത നിബന്ധനകള് (boundary conditions) പ്രയോജനപ്പെടുത്തുന്നു. സംകാരകങ്ങളെ സംബന്ധിച്ച് ചില സങ്കല്പനങ്ങളുണ്ട്. അവയ്ക്ക് തനതായ ഉപപത്തിയൊന്നും കണ്ടെത്തിയിട്ടില്ല. ഷ്റോഡിങ്ഗര് സമവാക്യം എങ്ങനെ വിരചിക്കാമെന്നു മനസ്സിലാക്കുവാന് അവ സഹായകമാണ്.
1. ഗതികീയമായ ഓരോ ചരത്തിനും (dynamical variable) തുല്യമായ ഓരോ സംകാരമുണ്ട്. ഈ സംകാരകത്തെ ആശ്രയിട്ടുണ്ടാകുന്ന ഐഗന് മൂല്യമാണ് പരീക്ഷണങ്ങളിലൂടെ കണ്ടെത്തുന്ന രാശി.
2. q, r എന്നിവ പ്രത്യേക തരത്തില്പ്പെടുന്ന രണ്ടു ചരങ്ങള് (canonically conjugate variables) ആണെങ്കില്, അവയ്ക്കു തുല്യമായ q, r എന്നീ സംകാരകങ്ങള് താഴെ പറയുന്ന സമവാക്യത്തിലൂടെ ബന്ധപ്പെട്ടിരിക്കണം: ![]()
h പ്ലാങ്ക് സ്ഥിരാങ്കം, ; i2 = -1. ഉദാഹരണമായി x എന്ന നിര്ദേശാങ്കവും P എന്ന സംവേഗവും സംകാരങ്ങളാക്കുമ്പോള് യഥാക്രമം x ഉം
![]() ഉം ആയിത്തീരുന്നു.
ഉം ആയിത്തീരുന്നു.
3. (a) തരംഗഫലനത്തിന്റെ വര്ഗം ψ∗ ψ സംഭാവ്യതയെ സൂചിപ്പിക്കുന്നു. (ψ യുടെ സങ്കീര്ണ പൂരകം (complex conjugate) ആണ് ψ ∗) ഉദാ.x നും (x + dx)നും ഇടയിലായി x ഉണ്ടാകാനുള്ള സംഭാവ്യത ψ∗ ψ dx ആകുന്നു. മറ്റു നിര്ദേശാങ്കങ്ങള്ക്കും ഇതുപോലെതന്നെ.
3. (b) q ഒരു ഗതികീയ ചരമാണെങ്കില് അതിന്റെ ശരാശരി മൂല്യം ![]() (സമാകലനത്തിലുള്ള q സംകാരകമാകുന്നു).
(സമാകലനത്തിലുള്ള q സംകാരകമാകുന്നു).
4. സമയമനുസരിച്ച് ψ മാറുന്നതാണെങ്കില് തരംഗഫലനത്തെ e - i2π Et/h കൊണ്ട് ഗുണിക്കേണ്ടതാണ്; t = സമയം.
മേല്പറഞ്ഞ തത്ത്വങ്ങളുപയോഗിച്ച് പ്രതിഭാസങ്ങളെ എങ്ങനെ കൈകാര്യം ചെയ്യാമെന്നും എന്താണ് അതുകൊണ്ടുളവാകുന്ന ഫലങ്ങളെന്നും ഇനി പരിശോധിക്കാം.
ഉദാഹരണങ്ങള്
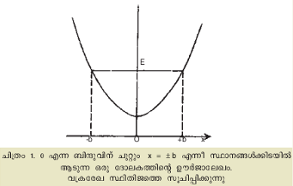
(1) സരളാവര്ത്തക ദോലകം (Simple Harmonic Oscillator). ക്ലാസ്സിക്കല് സിദ്ധാന്തം കൈകാര്യം ചെയ്തിട്ടുള്ള ലളിതമായ ഒരു പ്രമേയമാണിത്. പെന്ഡുലം മാതിരി, ഒരു മാധ്യബിന്ദുവിനു ചുറ്റും ആടിക്കൊണ്ടിരിക്കുന്ന ഒരു വസ്തുവിന്റെ ചലനത്തില്, x എന്ന വിസ്ഥാപനത്തിനു സ്ഥിതിജമായ ഊര്ജം V (x) = ½ F x 2 ആണെന്നും ഗതിജമായ ഊര്ജം ![]() ആണെന്നും ക്ലാസ്സിക്കല് ബലതന്ത്രം പറയുന്നു. ഇവയുടെ ആകെത്തുക E = T + V.. ബാഹ്യമായ മറ്റു ബലങ്ങളൊന്നും ഇടപെടുന്നില്ലെങ്കില് E സ്ഥിരമായി നിലനില്ക്കുന്നു. ദോലകം x = +b, x = -b എന്നീ സ്ഥാനങ്ങള്ക്കിടയില് ആടിക്കൊണ്ടിരിക്കുകയും ചെയ്യും (ചിത്രം 1). F = ബലസ്ഥിരാങ്കം; m = ദ്രവ്യമാനം.
ആണെന്നും ക്ലാസ്സിക്കല് ബലതന്ത്രം പറയുന്നു. ഇവയുടെ ആകെത്തുക E = T + V.. ബാഹ്യമായ മറ്റു ബലങ്ങളൊന്നും ഇടപെടുന്നില്ലെങ്കില് E സ്ഥിരമായി നിലനില്ക്കുന്നു. ദോലകം x = +b, x = -b എന്നീ സ്ഥാനങ്ങള്ക്കിടയില് ആടിക്കൊണ്ടിരിക്കുകയും ചെയ്യും (ചിത്രം 1). F = ബലസ്ഥിരാങ്കം; m = ദ്രവ്യമാനം.
E പ്രാരംഭത്തില് ഏതു മൂല്യം സ്വീകരിക്കുന്നുവോ ആ മൂല്യമാണ് സ്ഥിരമായി നിലനില്ക്കുന്നത്. പക്ഷേ പ്രാരംഭമൂല്യം ഏതുമാകാം. ക്ലാസ്സിക്കല് സിദ്ധാന്തത്തില് അതിന് അവിച്ഛിന്നതയില്ല. ദോലനത്തിന്റെ ആവൃത്തി ![]() ആകുന്നു. ഇനി ക്വാണ്ടം ബലതന്ത്രമനുസരിച്ചുള്ള സമീകരണം പരിഗണിക്കാം. ഊര്ജത്തിനു സമാനമായ സംകാരകം (H). ഇവിടെ,
ആകുന്നു. ഇനി ക്വാണ്ടം ബലതന്ത്രമനുസരിച്ചുള്ള സമീകരണം പരിഗണിക്കാം. ഊര്ജത്തിനു സമാനമായ സംകാരകം (H). ഇവിടെ, ![]() എന്നാകുന്നു.
എന്നാകുന്നു.
ഷ്റോഡിങ്ഗര് സമവാക്യം Hψ = Eψ ആയതുകൊണ്ട് ![]() എന്നു ലഭിക്കുന്നു. ഇതിന്റെ നിര്ധാരണം ചൂണ്ടിക്കാട്ടുന്ന വസ്തുത, ഐഗന് മൂല്യം അഥവാ ഊര്ജം വിച്ഛിന്നം (discontinuous) ആണെന്നാണ്. പ്രസക്തമായ സമവാക്യം E ν = ( ν + ½) h ν വഎന്നതാണ് n = 0,1,2,3... എന്നിങ്ങനെ ഏതു പൂര്ണസംഖ്യയുമാകാം. ഓരോന്നിനും ഓരോ ഊര്ജം ലഭിക്കുന്നു. അതായത്,
എന്നു ലഭിക്കുന്നു. ഇതിന്റെ നിര്ധാരണം ചൂണ്ടിക്കാട്ടുന്ന വസ്തുത, ഐഗന് മൂല്യം അഥവാ ഊര്ജം വിച്ഛിന്നം (discontinuous) ആണെന്നാണ്. പ്രസക്തമായ സമവാക്യം E ν = ( ν + ½) h ν വഎന്നതാണ് n = 0,1,2,3... എന്നിങ്ങനെ ഏതു പൂര്ണസംഖ്യയുമാകാം. ഓരോന്നിനും ഓരോ ഊര്ജം ലഭിക്കുന്നു. അതായത്,
E0 = h ν /2 ( ν എന്നത് ക്ലാസ്സിക്കല് ആവൃത്തി)
E1 = 3h ν / 2 E2 = 5h ν / 2 ...
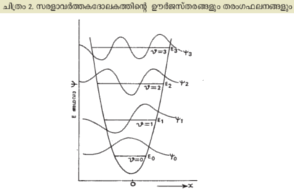
ക്ലാസ്സിക്കല് സിദ്ധാന്തമനുസരിച്ച് ഒരു ദോലകത്തിന് സ്വീകാര്യമായ ഊര്ജമൂല്യം എന്തുമാകാം. പക്ഷേ ക്വാണ്ടം ബലതന്ത്രത്തില് ചില നിശ്ചിതമൂല്യങ്ങളേ സാധ്യമാകൂ. ഏറ്റവും കുറഞ്ഞ ഊര്ജം E0 ആകുന്നു. അതിനുമേല് h ν കൂട്ടിയാല് E1 രണ്ടു h ചേര്ത്താല് E2 മുതലായ ഊര്ജസ്തരങ്ങള് ലഭിക്കുന്നു. ഊര്ജം ഒരിക്കലും പൂജ്യമാവുന്നില്ല. ഏറ്റവും ചുരുങ്ങിയ ഊര്ജം E0 ആകുന്നു. ഓരോ ഊര്ജമൂല്യത്തിനനുസരിച്ചും തരംഗഫലനം മാറിക്കൊണ്ടിരിക്കും. (ചിത്രം 2) ഏറ്റവും താഴ്ന്ന ഊര്ജനിലയായ E0 -യ്ക്ക് സംഗതമായ തരംഗഫലനം ആകുന്നു. ഇതിന്റെ ആയാമം (amplitude) മധ്യസ്ഥാനത്ത് ഏറ്റവും ഉയര്ന്നിരിക്കുന്നു. അതുകൊണ്ട് അതിന്റെ വര്ഗമായ സംഭാവ്യതയും അവിടെത്തന്നെ ഏറ്റവും കൂടുതലായിരിക്കും. ഉയര്ന്ന ഊര്ജസ്തരങ്ങളില് ഇതുപോലെ ആയാമമനുസരിച്ച് സംഭാവ്യതയും ഏറിയും കുറഞ്ഞും വരുന്നതു ചിത്രത്തില്നിന്ന് ഊഹിക്കാവുന്നതാണ്. ഒരു പ്രത്യേകസ്തരത്തില് വര്ത്തിക്കുന്ന ദോലകം ഊര്ജത്തെ ഉള്ക്കൊള്ളുമ്പോള് തൊട്ടടുത്ത പടിയിലേക്കു കയറും. ഊര്ജത്തെ ത്യജിക്കുകയാണെങ്കില് താഴേക്ക് ഒരു പടി ഇറങ്ങുകയും ചെയ്യും. അതായത് n എന്ന ക്വാണ്ടം സംഖ്യയുടെ മാറ്റം Δν = ±1 എന്നാകുന്നു. ഇതും ക്വാണ്ടം ബലതന്ത്രത്തിന്റെ നിഗമനമാണ്. അതിനാല് ദോലകം ഉത്സര്ജിക്കുന്ന ഊര്ജം നിരീക്ഷിക്കുകയാണെങ്കില് അതിന്റെ മൂല്യം hν മാത്രമാണ്. പ്ലാങ്കിന്റെ ക്വാണ്ടത്തിനു തുല്യം തന്നെ. രണ്ട് അണുക്കള് തമ്മില് യോജിച്ചുണ്ടാകുന്ന തന്മാത്രകളുടെ (diatomic molecules) കമ്പനത്തിനും ഇതേ ഊര്ജസ്തരങ്ങള് തന്നെയാണുള്ളത്. അതൊരു സരളാവര്ത്തന ദോലനമാണ്.
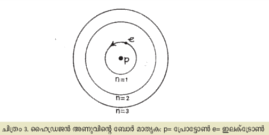
(b) ഹൈഡ്രജന് അണുഘടന. അണുക്കളില്വച്ച് ഏറ്റവും ലളിതമായ ഘടനയുള്ളത് ഹൈഡ്രജനാണ്. ബോര് സിദ്ധാന്തമനുസരിച്ച് ഈ അണുവിന്റെ നടുവില് ഒരു പ്രോട്ടോണും അതിനു ചുറ്റും പ്രത്യേക ഭ്രമണപഥങ്ങളില് ഏതിലെങ്കിലും സഞ്ചരിക്കുന്ന ഒരു ഇലക്ട്രോണുമാണുള്ളത്. ഭ്രമണപഥങ്ങളെ സൂചിപ്പിക്കുന്നത് അവയുടെ മുഖ്യ ക്വാണ്ടംസംഖ്യ (n) കൊണ്ടാണ്. അണുകേന്ദ്രത്തോട് ഏറ്റവും അടുത്തുള്ള ഭ്രമണപഥത്തിന് n = 1 അതിനടുത്ത് n = 2, പിന്നെ n = 3... (ചിത്രം 3). പ്രോട്ടോണും ഇലക്ട്രോണും തമ്മിലുള്ള ആകര്ഷണബലവും പ്ലാങ്കിന്റെ ക്വാണ്ടം സിദ്ധാന്തവും പ്രയോജനപ്പെടുത്തിക്കൊണ്ട്, ഓരോ ഭ്രമണപഥത്തിലും സഞ്ചരിക്കുമ്പോള് ഇലക്ട്രോണിനുണ്ടാകുന്ന ഊര്ജം എത്രയെന്ന് ബോര് കണക്കാക്കി. m, e എന്നിവ ഇലക്ട്രോണിന്റെ ദ്രവ്യമാനവും ചാര്ജും ആയാല്, ക്വാണ്ടം സംഖ്യ n ആയിട്ടുള്ള പഥത്തില് ഊര്ജമൂല്യം, ഇലക്ട്രോണ് വോള്ട്ട് (eV) മാത്രയില്, ![]() ആകുന്നു. ഏറ്റവും താഴ്ന്ന (ഋണാത്മകമായ) ഊര്ജം ഒന്നാം ഭ്രമണപഥത്തിനാണുള്ളത്. ഉത്തേജിതമല്ലാത്ത അണുവില് ഈ പഥത്തിലാണ് ഇലക്ട്രോണ് സഞ്ചരിക്കുക. ഈ പഥത്തിന് അണുകേന്ദ്രത്തില് നിന്നുള്ള ദൂരം 0.529 x 10-8 സെ.മീ. ആകുന്നു. രണ്ട് ഊര്ജസ്തരങ്ങള് തമ്മിലുള്ള ഊര്ജവ്യത്യാസം.
ആകുന്നു. ഏറ്റവും താഴ്ന്ന (ഋണാത്മകമായ) ഊര്ജം ഒന്നാം ഭ്രമണപഥത്തിനാണുള്ളത്. ഉത്തേജിതമല്ലാത്ത അണുവില് ഈ പഥത്തിലാണ് ഇലക്ട്രോണ് സഞ്ചരിക്കുക. ഈ പഥത്തിന് അണുകേന്ദ്രത്തില് നിന്നുള്ള ദൂരം 0.529 x 10-8 സെ.മീ. ആകുന്നു. രണ്ട് ഊര്ജസ്തരങ്ങള് തമ്മിലുള്ള ഊര്ജവ്യത്യാസം. ![]()
ഇതനുസരിച്ച് ഇലക്ട്രോണ് സ്ഥാനം മാറുമ്പോള് അണുവില്നിന്ന് ഒരു വൈദ്യുതകാന്തികതരംഗം പുറപ്പെടുന്നു. അതിന്റെ ആവൃത്തി ν ആയിരിക്കും. ക്വാണ്ടം നിയമമനുസരിച്ച് hν = En2-En1 .ഇങ്ങനെ മുകളിലുള്ള സ്തരങ്ങളില്നിന്ന് ഇലക്ട്രോണ് താഴേക്കുള്ള പഥങ്ങളിലേക്കു സംക്രമിക്കുമ്പോള് വിവിധ തരംഗങ്ങള് സംജാതമാകുന്നു. ഇതാണ് ഹൈഡ്രജന്റെ വര്ണരാജി. ഇനി ക്വാണ്ടം ബലതന്ത്രം ഈ പ്രതിഭാസത്തെ എങ്ങനെ പ്രതിപാദിക്കുന്നുവെന്നു നോക്കാം.
പ്രോട്ടോണിനെ നിശ്ചലമാക്കി നിര്ത്തിക്കൊണ്ട് ഇലക്ട്രോണിന്റെ ചലനം മാത്രം കണക്കിലെടുക്കുന്നതിനു പകരം രണ്ടുംകൂടി ചേര്ന്നുള്ള ഒരു വ്യൂഹത്തിന്റെ ചലനമാണ് ഇവിടെ പരിഗണിക്കുന്നത്. അതിനാല് പ്രാഥമികമായ ഷ്റോഡിങ്ഗര് സമവാക്യത്തില് അതുള്പ്പെടുത്തിയിരിക്കുന്നു. അതായത്
1, 2 എന്നീ പാദാങ്കങ്ങള് ഇലക്ട്രോണിനെയും പ്രോട്ടോണിനെയും സൂചിപ്പിക്കുന്നു. m = ദ്രവ്യനാമം
![]() നിര്ദേശാങ്കം. അതിനാല് തരംഗസമവാക്യം H ψ (r1, r2) = E ψ (r1, r2) ഇതിന്റെ നിര്ധാരണത്തില് നിന്ന് ഊര്ജമൂല്യങ്ങള് ലഭിക്കുന്നു. അവ ബോര് സിദ്ധാന്തമനുസരിച്ച് ലഭിച്ച മൂല്യങ്ങളോട് സമാനം തന്നെ:
നിര്ദേശാങ്കം. അതിനാല് തരംഗസമവാക്യം H ψ (r1, r2) = E ψ (r1, r2) ഇതിന്റെ നിര്ധാരണത്തില് നിന്ന് ഊര്ജമൂല്യങ്ങള് ലഭിക്കുന്നു. അവ ബോര് സിദ്ധാന്തമനുസരിച്ച് ലഭിച്ച മൂല്യങ്ങളോട് സമാനം തന്നെ:
En = -ER/n2; ER ഒരു സ്ഥിരാങ്കമാണ്. n = 1, 2, 3... പക്ഷേ അതിനോടനുബന്ധിച്ച തരംഗഫലനത്തെ സൂചിപ്പിക്കുവാന് l, m എന്നീ രണ്ടു ക്വാണ്ടസംഖ്യകള് കൂടി ആവശ്യമാണ്. ബോര് സിദ്ധാന്തത്തി n = 1 എന്നത് വ്യക്തമായ ഒരു ഭ്രമണരേഖയാണ്. ഇവിടെ അതിനു സമാനമായി ψ100 എന്ന ഒരു തരംഗഫലനമാണുള്ളത്. ഇലക്ട്രോണ് ഒരു തരംഗമായതിനാല് അതിനു വ്യക്തമായ ഒരു ഭ്രമണപഥം കല്പിക്കാനാകില്ല. ഇലക്ട്രോണ് തരംഗം അണുകേന്ദ്രത്തെ പൊതിഞ്ഞിരിക്കുകയാണ്. അതിന്റെ സ്ഥാനം കണ്ടെത്തുന്നതിന് സഹായകമായിട്ടുള്ളത് തരംഗഫലനം മാത്രമാണ്. n = 1 എന്ന ക്വാണ്ടം സംഖ്യയ്ക്ക് തരംഗഫലനം:
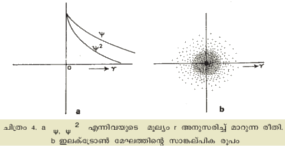
എന്നാകുന്നു. a0 എന്നത് ബോര് സിദ്ധാന്തത്തിലെ ഇലക്ട്രോണ് ഭ്രമണപഥത്തിന്റെ വ്യാസാര്ഥമാണ് (Bohr radius), r, കേന്ദ്രത്തില്നിന്നുള്ള ദൂരം സൂചിപ്പിക്കുന്നു; a0 സ്ഥിരാങ്കമാണ്. ഇതനുസരിച്ച് ഏതു ദിശയിലായാലും r ദൂരത്തിലുള്ള ബിന്ദുക്കളില് തരംഗഫലനം തുല്യമാണ് . അതായത് തരംഗഫലനത്തിന് ഗോളീയമായ സമമിതി (spherical symmetry) ഉണ്ട്. ദൂരം കൂടുന്തോറും അതിന്റെ മൂല്യം ക്ഷയിക്കുകയും ചെയ്യുന്നു (ചിത്രം 4). ഇലക്ട്രോണിനെ ഏതെങ്കിലും സ്ഥാനത്തു കണ്ടെത്താനുള്ള സംഭാവ്യതയും ഇതുപോലെ ക്ഷയിക്കുന്നു. ഇലക്ട്രോണിന്റെ വൈദ്യുതചാര്ജ് ഇതനുസരിച്ച് കേന്ദ്രത്തിനു ചുറ്റും വ്യാപിച്ചിരിക്കുന്നതായി കരുതാം. ഒരു ഇലക്ട്രോണ് മേഘമാണ് പ്രോട്ടോണിനെ വലയം ചെയ്തിട്ടുള്ളത്.
ബോറിന്റെ സങ്കല്പത്തോട് ഇതിനെ താരതമ്യം ചെയ്യണമെങ്കില് ഇലക്ട്രോണ് ചാര്ജിന്റെ ഏറ്റവുമധികം അംശം ഏതു ദൂരത്തിലാണ് നിലകൊള്ളുന്നതെന്ന് കണക്കാക്കണം. ഈ സ്ഥാനം കേന്ദ്രത്തിലല്ല. r, r + dr എന്നീ ദൂരങ്ങള്ക്കിടയിലുള്ള വ്യാപ്തം 4 π r2dr ആകുന്നു. ഇതിനെ സംഭാവ്യതകൊണ്ടു ഗുണിച്ചാല് ചിത്രം 5-ല് കൊടുത്തിട്ടുള്ള രേഖ കിട്ടുന്നു.
രേഖയുടെ ഉച്ചതമം, a0 എന്ന ദൂരത്തിലാണ്. ബോര് സിദ്ധാന്തത്തില് ഇലക്ട്രോണ് സഞ്ചരിക്കുന്ന ഭ്രമണപഥത്തിന്റെ സ്ഥാനത്തിന് തുല്യമാണിത്. ഇത് ഒന്നാം ഭ്രമണപഥത്തിന്റെ (n = 1) കാര്യമാണ്. പക്ഷേ മേലോട്ടുള്ള ഭ്രമണപഥങ്ങള് നോക്കുമ്പോള് ഇത്തരത്തിലുള്ള സാദൃശ്യമില്ല (ചിത്രം 5). ആദ്യത്തേത് ഹൈഡ്രജന്റെ (Is) അവസ്ഥയുടെ (Is state) ഫലനത്തെ കാണിക്കുന്നു. n=2 എന്ന ക്വാണ്ടം സംഖ്യയ്ക്ക് രണ്ട് അവസ്ഥകളുണ്ട്; 2s, 2p. n = 3 ആകുമ്പോള് ,s, p, d എന്നീ ഉള്പ്പിരിവുകള് വരുന്നു. ഈ അവസ്ഥാന്തരങ്ങള്ക്കനുസൃതമായി തരംഗഫലനവും രൂപാന്തരപ്പെടുന്നു. ചിത്രം 6-ല് ഇത്തരം ചില ഫലനങ്ങളെ ആവിഷ്കരിച്ചിരിക്കുന്നു. ഓരോ അവസ്ഥയെയും കുറിക്കുന്ന തരംഗഫലനത്തിന് അണുവിന്റെ 'അറ്റോമിക് ഓര്ബിറ്റല്' എന്നാണ് പേര്. ക്ലാസ്സിക്കല് സിദ്ധാന്തത്തിലെപ്പോലെ വ്യക്തമായ ഭ്രമണപഥങ്ങളല്ല ഇവ. വൈദ്യുതചാര്ജിന്റെ പ്രത്യേകാകൃതിയിലുള്ള, 'മേഘ'ങ്ങളായി ഇവയെ സങ്കല്പിക്കാം.
അനേകം ഇലക്ട്രോണുകളുള്ള അണുക്കളിലും തന്മാത്രകളിലും മേല്പറഞ്ഞ വൈദ്യുതമേഘങ്ങള് കൂടുതല് സങ്കീര്ണമായിത്തീരുന്നു.
ബോര് സിദ്ധാന്തമനുസരിച്ച് ഇലക്ട്രോണിന് ഒരു പഥത്തില് നിന്നു മറ്റൊന്നിലേക്കു ചാടാന് എപ്പോഴും സാധിക്കും. ഭ്രമണപഥത്തിന്റെ പ്രകൃതവുമായി ഇതിനു ബന്ധമൊന്നുമില്ല. തന്മൂലം ചില സ്പെക്ട്രരേഖകള് തീവ്രമായും ചിലതു മങ്ങിയും കാണപ്പെടാനുള്ള കാരണങ്ങളെപ്പറ്റി ആ സിദ്ധാന്തത്തില്നിന്നു വ്യക്തമാകുന്നില്ല. പക്ഷേ ഇലക്ട്രോണ് സംക്രമണം നടക്കാനുള്ള സംഭാവ്യത അതിനുമുമ്പും പിമ്പുമുള്ള ഇലക്ട്രോണ് മേഘത്തിന്റെ രൂപത്തെ ആശ്രയിച്ചാണിരിക്കുന്നത് എന്ന് ക്വാണ്ടം ബലതന്ത്രം പറയുന്നു. രണ്ടു മേഘങ്ങള് തമ്മില് ചേര്ന്നു നില്ക്കുകയോ ഒന്നു മറ്റൊന്നിലേക്കു തള്ളി നില്ക്കുകയോ ചെയ്താല് ഇവയ്ക്കു തമ്മില് ഒരു ഇലക്ട്രോണ് സംക്രമണമുണ്ടാകാനുള്ള സാധ്യത കൂടുതലാവുന്നു. ഈ രീതിയില് ഇലക്ട്രോണ് മേഘങ്ങളുടെ രൂപമനുസരിച്ച് സംക്രമണസാധ്യതകള് എങ്ങനെ മാറുന്നുവെന്നു കണക്കാക്കിയിട്ടുണ്ട്. സംക്രമണങ്ങളെ കൂടുതല് സംഭാവ്യമെന്നും കുറച്ചു സംഭാവ്യമെന്നുമായി വിഭജിക്കുന്ന നിയമങ്ങള് വരണനിയമങ്ങള് (selection rules) എന്ന പേരിലറിയപ്പെടുന്നു. കൂടുതല് സംഭാവ്യതയുള്ള സംക്രമണങ്ങള് കൂടുതല് തീവ്രതയുള്ള പ്രകാശതരംഗം ഉത്പാദിപ്പിച്ചിരിക്കുന്നതിന് കാരണമാകുന്നു. മങ്ങിയ തരംഗങ്ങള് അവയെ ഉത്പാദിപ്പിക്കുന്ന ഇലക്ട്രോണ് സംക്രമണത്തിന്റെ സംഭാവ്യത കുറവാണെന്നും സൂചിപ്പിക്കുന്നു.
തീവ്രതയിലുള്ള ഏറ്റക്കുറച്ചിലിനു പുറമേ രേഖകള്ക്കു കാണപ്പെടുന്ന പരപ്പും (breadth) വര്ണരാജിയിലെ ഒരു പ്രത്യേകതയാണ്. അതായത്, ഓരോ രേഖയും പ്രതിനിധാനം ചെയ്യുന്ന പ്രകാശതരംഗത്തിന്റെ ആവൃത്തിക്കു നിഷ്കൃഷ്ടമായ ഒരൊറ്റമൂല്യമല്ല ഉള്ളത്. അല്പം അനിശ്ചിതത്വം അതിനുള്ളതിനാല് തരംഗം തികച്ചും ഏകവര്ണ (monochromatic)മാകുന്നില്ല.
ഉപകരണത്തിന്റെ വിഭേദനക്ഷമതയിലുള്ള അപര്യാപ്തതകൊണ്ടല്ല ഈ അനിശ്ചിതത്വം സംഭവിക്കുന്നത് എന്ന് ക്വാണ്ടം ബലതന്ത്രം തെളിയിച്ചു. സുപ്രധാനമായ ഒരു തത്ത്വം ഇതിലുണ്ട്. ചില പ്രതിഭാസ നിരീക്ഷണങ്ങളില് അനിശ്ചിതത്വം സഹജമായി വര്ത്തിക്കുന്നു. ഈ തത്ത്വം ഹൈസന്ബെര്ഗ് ആണ് ആവിഷ്കരിച്ചത്. 'അനിശ്ചിതത്വസിദ്ധാന്തം' (Uncertainty principle) എന്ന പേരില് ഇതറിയപ്പെടുന്നു.
അനിശ്ചിതത്വസിദ്ധാന്തം
ക്ലാസ്സിക്കല് സിദ്ധാന്തമനുസരിച്ച് മാപനങ്ങളില് സഹജമായ അനിശ്ചിതത്വം എന്നൊന്നില്ല. മാപനങ്ങളെ കഴിവനുസരിച്ച് എത്രത്തോളമെങ്കിലും കണിശമാക്കാം. പക്ഷേ ഇതിനു സഹജമായ പരിമിതികളുണ്ടെന്നു മേല്പറഞ്ഞ സിദ്ധാന്തം സ്ഥാപിച്ചു. ഒരു വസ്തുവിന്റെ അവസ്ഥയെ കുറിക്കുന്ന ചില രാശികള് അളന്നു തിട്ടപ്പെടുത്തുമ്പോഴാണ് അനിശ്ചിതത്വം പ്രകടമാവുന്നത്. ഉദാ. ചലിക്കുന്ന വസ്തുവിന്റെ സ്ഥാനവും അതിനുള്ള സംവേഗവും. ഇവയില് ഏതെങ്കിലുമൊന്നിനെ എത്രത്തോളം കൃത്യമായി നിര്ണയിക്കാന് ശ്രമിക്കുന്നുവോ അത്രത്തോളം അനിശ്ചിതത്വം മറ്റേതിന്റെ നിര്ണയനത്തില് സംഭവിക്കും. രണ്ടുംകൂടി ഒരുമിച്ച് കൃത്യമായി അളന്നു വ്യവച്ഛേദിക്കാന് സാധ്യമല്ല. സ്ഥാനനിര്ണയനത്തിലെ അനിശ്ചിതത്വം (Δx ) -ഉം സംവേഗത്തിലേത് (Δp) -യും ആണെങ്കില്, (Δx) X (Δp ) ≈ h (പ്ലാങ്ക്സ്ഥിരാങ്കം). ഇതുപോലെ തന്നെ പ്രസക്തമായ മറ്റൊരു ജോടിയാണ് ഊര്ജവും സമയവും. ഒരു വസ്തുവിന്റെ ഊര്ജാവസ്ഥയും ആ അവസ്ഥ നിലനില്ക്കുന്ന സമയവും അളക്കുമ്പോള് അനിശ്ചിതത്വം യഥാക്രമം (ΔE) -യും (Δt) ̨-യുമാണെങ്കില് രണ്ടിന്റെയും ഗുണിതം ഏകദേശം പ്ലാങ്ക് സ്ഥിരാങ്കത്തിന് തുല്യമായിരിക്കും. അഥവാ (ΔE)(Δt) ≈ h. ഈ സമയവും വര്ണരാജിക്കു നിദാനമായ ഇലക്ട്രോണിന്റെ കാര്യത്തില് പ്രയോഗിക്കാവുന്നതാണ്. അണുവില് ഇലക്ട്രോണിന് ക്ളിപ്തമായ ഊര്ജമുണ്ട്. സ്ഥാനഭ്രംശം സംഭവിക്കുന്നതിനു മുമ്പും പിമ്പും അതിനുള്ള ഊര്ജം സുവ്യക്തമാണെങ്കിലും സമയത്തെ ക്ളിപ്തപ്പെടുത്തുന്ന സാഹചര്യം വരുമ്പോള് ഊര്ജമൂല്യങ്ങള് അവ്യക്തമായിത്തീരുന്നു. ഇലക്ട്രോണ് ഒരേ ഊര്ജസ്തരത്തില് സ്ഥിരമായി നില്ക്കുകയല്ല. മറ്റൊന്നിലേക്കു മാറുകയാണ്. ചാട്ടങ്ങള്ക്കിടയ്ക്കുള്ള ഇലക്ട്രോണിന്റെ ആയുസ് (Δt)ആണെങ്കില്, പ്രകാശതരംഗത്തിന്റെ ഊര്ജത്തിലുള്ള അനിശ്ചിതത്വം ![]() അതായത് തരംഗത്തിന്റെ ആവൃത്തിയിലും ഒരനിശ്ചിതത്വമുണ്ടാകുന്നു. ഇതാണ് വര്ണരേഖകളുടെ പരപ്പിനുള്ള കാരണം.
അതായത് തരംഗത്തിന്റെ ആവൃത്തിയിലും ഒരനിശ്ചിതത്വമുണ്ടാകുന്നു. ഇതാണ് വര്ണരേഖകളുടെ പരപ്പിനുള്ള കാരണം.
ഇലക്ട്രോണിന്റെ ചക്രണം
വര്ണരാജിയിലെ രേഖകളുടെ മറ്റൊരു പ്രത്യേകതയാണ് അവയുടെ സൂക്ഷ്മഘടന (fine structure). ഇതു വിശദീകരിക്കുവാന്, ഇലക്ട്രോണിന്റെ മേല്പറഞ്ഞ വിധത്തിലുള്ള ചലനം മാത്രം പോരാ എന്നും സ്വന്തം അക്ഷത്തില് ഒരു ചക്രണംകൂടി സങ്കല്പിക്കാമെന്നും പൗളി (Pauli) സിദ്ധാന്തിച്ചു. ഇതനുസരിച്ച് ഒരു ക്വാണ്ടംസംഖ്യകൂടി ഇലക്ട്രോണിനു ചേര്ക്കേണ്ടതുണ്ട്. ഈ സംഖ്യ m8= ± 1⁄2 ആകുന്നു. അങ്ങനെ ഇലക്ട്രോണിന്റെ ഊര്ജത്തെ പ്രതിനിധാനം ചെയ്യുവാന് n, l, m1, m8 എന്നീ നാലു ക്വാണ്ടം സംഖ്യകള് ആവശ്യമാണ്. ക്വാണ്ടം ബലതന്ത്രത്തെ അടിസ്ഥാനമാക്കി ചക്രണം എന്ന പ്രതിഭാസത്തെ ഡിറാക് പിന്നീട് സ്ഥാപിക്കുകയുണ്ടായി.
ഒരണുവില്ത്തന്നെയുള്ള ഏതെങ്കിലും രണ്ട് ഇലക്ട്രോണുകള്ക്ക് ഒരേ ക്വാണ്ടസംഖ്യകള് ഉണ്ടാവാന് പാടില്ലെന്ന സുപ്രധാന തത്ത്വം (പൗളി അപവര്ജനനിയമം-Pauli's Exclusion Principle) തരംഗഫലനത്തിന്റെ സമമിതിയെ സംബന്ധിക്കുന്ന പ്രശ്നങ്ങളില്നിന്നു തെളിയുന്നു. ഈ തത്ത്വത്തെ അടിസ്ഥാനപ്പെടുത്തിയാണ് അണുക്കളുടെ ഇലക്ട്രോണിക ഘടന ആവിഷ്കരിക്കപ്പെട്ടിട്ടുള്ളത്.
ഒരു ഇലക്ട്രോണ് മാത്രമുള്ള ഹൈഡ്രജന്റെ തരംഗഫലനത്തെപ്പറ്റിയാണ് മുകളില് പ്രസ്താവിച്ചത്. ഇലക്ട്രോണുകളുടെ എണ്ണം കൂടുതലുള്ള മൂലകങ്ങളുടെ തരംഗഫലനം കൂടുതല് സങ്കീര്ണവും ക്ലിപ്തമായ നിര്ധാരണം അസാധ്യവുമായിത്തീരുന്നു. ചില ഏകദേശനങ്ങള് ഉപയോഗിച്ചാണ് ഇവയുടെ ഊര്ജസ്തരങ്ങള് നിര്ണിയിക്കുന്നത്.
തന്മാത്രകള്
അണുക്കളുടെ സംയോജകതയും അവ തമ്മില് ചേര്ന്നുണ്ടാകുന്ന തന്മാത്രകളുടെ ആകൃതിയും ഘടനയും ഊര്ജവിതാനവും അടിസ്ഥാനപരമായി മനസ്സിലാക്കുന്നതിനു ക്വാണ്ടം ബലതന്ത്രം മാത്രമേ സഹായകമായിട്ടുള്ളൂ.
രണ്ടണുക്കള് തമ്മിലടുത്തുവരുമ്പോള്, അവയുടെ ബാഹ്യമണ്ഡലത്തിലുള്ള ഇലക്ട്രോണ് മേഘങ്ങള് കൂടിക്കലരുകയും രണ്ടിനുംകൂടി പ്രസക്തമായ ഒരു ചാര്ജ് വിന്യസനം ഉണ്ടാവുകയും ചെയ്യുന്നു. ഇതോടെ തന്മാത്രയുടെ രൂപീകരണം പൂര്ത്തിയാവുന്നു. ഓരോ അണുവിനും സംയോജനത്തിനു മുമ്പുണ്ടായിരുന്ന തരംഗഫലനം-അറ്റോമിക് ഓര്ബിറ്റല്-പിന്നീട് നിലനില്ക്കുന്നില്ല. ആ ഫലനങ്ങളെ ഭേദഗതികളോടെ ഉള്പ്പെടുത്തിക്കൊണ്ടുള്ള ഒരു പൊതു തന്മാത്രീയ ഫലനം ആണുണ്ടാവുന്നത്. ഈ പൊതുഫലനം കണ്ടെത്തുന്നതിന് ക്വാണ്ടം ബലതന്ത്രത്തില് ചില ഗണിതരീതികള് ആവിഷ്കരിച്ചിട്ടുണ്ട്. വിപുലമായ ആ വിഷയത്തിലേക്ക് ആമുഖമായി, ഏറ്റവും ലളിതമായ ഹൈഡ്രജന് തന്മാത്രാഅയോണിനെപ്പറ്റി (H2+) പ്രതിപാദിക്കാം.
രണ്ടു പ്രോട്ടോണും ഒരു ഇലക്ട്രോണുമാണ് ഈ അയോണിലുള്ളത്. ഇലക്ട്രോണ് രണ്ടു പ്രോട്ടോണിനോടും ബന്ധപ്പെട്ടിരിക്കുന്നു. A, B എന്നിവയാണ് പ്രോട്ടോണുകളെങ്കില്, സ്വതന്ത്രമായ ഹൈഡ്രജന് അണുവിന്റെ ഫലനങ്ങളെ ψA , ψB എന്നു നിര്ദേശിക്കാം. തന്മാത്രയുടെ (അയോണ്) ഫലനം ഇവയുടെ ഒരു സമ്മിശ്രമായി കരുതുകയാണെങ്കില്, ψ = C A ψA + CB ψB എന്നെഴുതാം. CA, CB എന്നിവ സ്ഥിരാങ്കങ്ങള്. ഗണിതപരമായി വിശകലനം ചെയ്യുമ്പോള്, ψ -ക്ക് ഇവിടെ രണ്ടുമൂല്യങ്ങള് സിദ്ധിക്കുന്നു:
ഇവയ്ക്കനുസരിച്ചുള്ള ഐഗന് മൂല്യങ്ങള് കണക്കാക്കുമ്പോള് സമമിതിയുള്ള ആണ് തന്മാത്രയുടെ ഊര്ജത്തോടു യോജിച്ചത് എന്നുകാണാം. ഇലക്ട്രോണിന്റെ സാന്ദ്രത രണ്ടു പ്രോട്ടോണുകളുടെയും നടുവില് കൂടുതലായി കേന്ദ്രീകരിക്കുകയും ചെയ്യുന്നു. ഈ അയോണിനെ ഒരു ഹൈഡ്രജന് അണുവും (HA) അതിനോടുചേര്ന്ന ഒരു പ്രോട്ടോണും (HB +) ആയി (HAHB +) സങ്കല്പിച്ച് ഊര്ജം കണക്കാക്കിയാല്, അവ തമ്മില് വികര്ഷണമാണു സംഭവിക്കുക. അല്ലെങ്കില് HB എന്ന അണുവും HA+ എന്ന അയോണും പരിഗണിച്ചാലും ഇങ്ങനെതന്നെ സംഭവിക്കുന്നു. പക്ഷേ രണ്ടു ഘടനാവിശേഷങ്ങളും (HAHB + . HA+HB ) ഒരുമിച്ചു പരിഗണിച്ചാല് മേല്പറഞ്ഞ സങ്കലനഫലനം കിട്ടുന്നു. അതായത് ഇലക്ട്രോണ് ഏതെങ്കിലും ഒരു പ്രോട്ടോണിനോടു മാത്രം ചേര്ന്നു നില്ക്കുന്നില്ല. രണ്ടും ഇലക്ട്രോണിനെ പരസ്പരം കൈമാറുന്ന രീതിയിലാണ് ഘടന ഉരുത്തിരിയുന്നത്. രണ്ടു ഘടനാവിശേഷങ്ങള് തമ്മിലുള്ള അനുനാദം (resonance) എന്ന പേരിലാണ് ഈ തന്മാത്ര വിശേഷിപ്പിക്കപ്പെടുന്നത്. തന്മാത്രകള്ക്കു പൊതുവേയുള്ള പ്രത്യേകതയാണിത്. ഓരോ തന്മാത്രയ്ക്കും വിവിധ ഇലക്ട്രോണ് വിന്യാസങ്ങള്ക്കു സാധ്യത കല്പിച്ചുകൊണ്ട് വിവിധ ഘടനകളുണ്ടെന്നും അവയുടെ ഒരു അനുനാദഫലമാണ് തന്മാത്രയ്ക്കു കാണപ്പെടുന്ന ഊര്ജമെന്നും ക്വാണ്ടം ബലതന്ത്രം ചൂണ്ടിക്കാട്ടുന്നു. ദൃഢവും സ്ഥിരവുമായ ഒരു രൂപശില്പം തന്മാത്രകള്ക്കില്ല.
തന്മാത്രകളുടെ രൂപീകരണത്തെ ക്വാണ്ടംബലതന്ത്രം എങ്ങനെ സമീപിക്കുന്നു എന്നതിന്റെ ഉദാഹരണമാണ് മുകളില് കൊടുത്തത്. ഇതുപോലെ ഖരപദാര്ഥങ്ങളുടെ ഘടനയെയും വൈദ്യുതചാലകത, വിശിഷ്ടതാപം (specefic heat), സമ്മര്ദനീയത (compressibility) മുതലായ വസ്തുധര്മങ്ങളെയും വ്യാഖ്യാനിക്കുന്നതില് ക്വാണ്ടം ബലതന്ത്രം വിജയിച്ചിട്ടുണ്ട്. ഇലക്ട്രോണ്, പ്രോട്ടോണ്, ന്യൂട്രോണ് മുതലായ കണികകള് അണുക്കളില് തട്ടുമ്പോഴുണ്ടാകുന്ന പ്രകീര്ണനപഠനമാണ് മറ്റൊരു മേഖല. ദ്രവ്യവും വികിരണവും തമ്മിലുള്ള അന്യോന്യപ്രവര്ത്തനം, വര്ണപ്രകീര്ണനം (dispersion), പ്രതികണങ്ങളുടെ അസ്തിത്വം മുതലായി മറ്റനേകം പ്രതിഭാസങ്ങളിലും ക്വാണ്ടം ബലതന്ത്രമാണ് വെളിച്ചം വീശിയത്.
ക്വാണ്ടം ബലതന്ത്രം-ആപേക്ഷികീയ
ക്വാണ്ടം ബലതന്ത്രം-ആപേക്ഷികീയ (Relativistic Quantum Mechanics).
ക്ലൈന്-ഗോര്ഡന് സമവാക്യം
പ്രകാശവേഗത്തോടു തുലനം ചെയ്യാവുന്നത്ര ഗതിവേഗമുള്ള കണികകള്ക്കു പ്രസക്തമായ ക്വാണ്ടം ബലതന്ത്രമാണ് ആപേക്ഷികീയ ക്വാണ്ടം ബലതന്ത്രം. ഷ്റോഡിങ്ഗര് ആവിഷ്കരിച്ച ക്വാണ്ടം ബലതന്ത്രം ഇതിന് അപര്യാപ്തമാണ്. ആപേക്ഷികതാസിദ്ധാന്തത്തില് അതിനു പ്രയോഗക്ഷമതയില്ല. ആപേക്ഷികീയ ക്വാണ്ടം ബലതന്ത്രം ആപേക്ഷികതാസിദ്ധാന്തത്തിന്റ തത്ത്വങ്ങളോട് പൊരുത്തപ്പെട്ടിരിക്കുന്നു.
ψ എന്ന തരംഗഫലനത്തിന്റെ സമവാക്യം, E ψ = H ψഎന്നാണ്. E എന്നത് ഊര്ജസംകാരവും (energy operator) H എന്നത് ക്ലാസ്സിക്കല് ഹാമില്ട്ടോണിയന് സംകാരവും (Hamiltonian) ആകുന്നു. സാധാരണ കണികകള്ക്ക് H = p2 / 2m ആപേക്ഷികതാ പരിധിയില്പ്പെടുമ്പോള് ![]() . പക്ഷേ, ഈ സംകാരകം നേരേ ഷ്റോഡിങ്ഗര് സമവാക്യത്തില് ഉള്പ്പെടുത്തുവാന് ഗണിതപരമായി നിവൃത്തിയില്ല. കാരണം ആപേക്ഷികമായി ആ സമവാക്യം
. പക്ഷേ, ഈ സംകാരകം നേരേ ഷ്റോഡിങ്ഗര് സമവാക്യത്തില് ഉള്പ്പെടുത്തുവാന് ഗണിതപരമായി നിവൃത്തിയില്ല. കാരണം ആപേക്ഷികമായി ആ സമവാക്യം ![]() അചരമാവുന്നില്ല (invariant). ഇതിനായി നിര്ദേശിക്കപ്പെട്ടിട്ടുള്ള സമവാക്യം എന്നാകുന്നു. ക്ളൈന്-ഗോരഡന് സമവാക്യം (Klein - Gordon equation) എന്ന പേരില് ഇതറിയപ്പെടുന്നു. കണികയുടെ ചക്രണം ഇതിന്റെ പരിധിയില്പ്പെടുന്നില്ല. അതിനാല് ചക്രണം ശൂന്യ (zero)മായിട്ടുള്ള കണികകള്ക്ക് ഇത് പ്രസക്തമാണ്.
അചരമാവുന്നില്ല (invariant). ഇതിനായി നിര്ദേശിക്കപ്പെട്ടിട്ടുള്ള സമവാക്യം എന്നാകുന്നു. ക്ളൈന്-ഗോരഡന് സമവാക്യം (Klein - Gordon equation) എന്ന പേരില് ഇതറിയപ്പെടുന്നു. കണികയുടെ ചക്രണം ഇതിന്റെ പരിധിയില്പ്പെടുന്നില്ല. അതിനാല് ചക്രണം ശൂന്യ (zero)മായിട്ടുള്ള കണികകള്ക്ക് ഇത് പ്രസക്തമാണ്.
ഡിറാക് സമവാക്യം
ഡിറാക് സമവാക്യം (Dirac equation). തരംഗഫലനത്തിന് ഡിറാക് നിര്ദേശിച്ച സമവാക്യം താഴെക്കാണുന്നവിധമാണ്.
β, αi എന്നീ നാലു സ്ഥിരാങ്കങ്ങള് സംഖ്യകളല്ല. അവ 4 x 4 മാട്രിക്സുകളും, ψ എന്നത് നാലു ഘടകങ്ങളുള്ള സ്പൈനര് (spinor) എന്ന ഒരു രാശിയുമാകുന്നു. ഡിറാക്കിന്റെ സമവാക്യം നിര്ധാരണം ചെയ്യുമ്പോള്, E എന്നതിനു ആകെ നാല് ഐഗന് സ്ഥിതികളുണ്ടെന്നു കാണാം. E ധനാത്മകമായ സ്ഥിതികള് സൂചിപ്പിക്കുന്നത് ചക്രണം ½ hആയിട്ടുള്ള കണത്തിന്റെ രണ്ട് ചക്രണസ്ഥിതികളാണ്. E ഋണാത്മകമായ സ്ഥിതികള് എന്തെന്നുള്ളത് ഒരു പ്രത്യേക സങ്കല്പനത്തിലൂടെ ഡിറാക് ആവിഷ്കരിച്ചു. E ധനാത്മകമാവുമ്പോള് അതിന്റെ ഏറ്റവും ചെറിയ മൂല്യം E = mc2 ആകുന്നു. അപ്പോള് p = 0 ഏറ്റവും കൂടിയ ഊര്ജം അനന്തവുമാകുന്നു (p → ∞ ). ഇതുപോലെ E ഋണാത്മകമാവുമ്പോള് ഏറ്റവും ചെറിയ ഊര്ജം E = −mc2, (p = 0) ആകുന്നു. പിന്നീട് അനന്തതയോളം വ്യാപിക്കുന്ന ഋണാത്മക ഊര്ജമുണ്ട്. അതായത് (+ mc2) നും (−mc2)2 നും ഇടയ്ക്ക് 2mc2 വിസ്താരമുള്ള ഒരു വര്ജിതമേഖല ഊര്ജത്തിനുണ്ട്. ഡിറാക് സങ്കല്പിച്ചത് ഋണാത്മകമായ ഊര്ജസ്തരങ്ങള് മുഴുവനും ഇലക്ട്രോണുകളെക്കൊണ്ടു പൂരിതമാണെന്നും അവയ്ക്കു നിരീക്ഷണവിധേയമാക്കാവുന്ന ഗുണധര്മങ്ങളൊന്നുംതന്നെ ഇല്ലെന്നുമാണ്. ഫെര്മി-ഡിറാക് സാംഖ്യികമനുസരിച്ച്, കൂടുതല് ഇലക്ട്രോണുകളെ ആ ഊര്ജസ്തരങ്ങളിലേക്ക് കടത്തിവിടാന് സാധ്യമല്ല. അതായത് സാധാരണ ഇലക്ട്രോണുകളൊന്നും ഋണാത്മകസ്ഥാനങ്ങളിലേക്കു സംക്രമിക്കുകയില്ല. പക്ഷേ ഋണാത്മകമായ ഏതെങ്കിലും ഊര്ജസ്തരത്തില് നിന്ന് ധനാത്മകമായ ഒരു സ്തരത്തിലേക്ക് വേണ്ടത്ര ഊര്ജം നല്കപ്പെടുകയാണെങ്കില്, ഒരു ഇലക്ട്രോണ് സംക്രമിച്ചേക്കാം. ഇതിനാവശ്യമായ ഊര്ജം വര്ജിതമേഖലയെ തരണം ചെയ്യാനെങ്കിലും പര്യാപ്തമായിരിക്കണം. അതായത് ഏറ്റവും ചുരുങ്ങിയ ഊര്ജം 2mc2 ആകുന്നു. ഇപ്രകാരം ധനാത്മക ഊര്ജം ഇലക്ട്രോണ് സ്വീകരിക്കുമ്പോള്, ഋണാത്മകമേഖലയില് ഒരു ദ്വാരം (hole) അഥവാ ഒഴിഞ്ഞസ്ഥാനം സംജാതമാകുന്നു. ഈ ദ്വാരത്തിന് ഊര്ജവും വൈദ്യുതാധാനവും ധനാത്മകമായിട്ടുള്ള ഒരു കണികയുടെ ഗുണധര്മങ്ങളുണ്ട്. ഇലക്ട്രോണിന്റെ ഒരു പ്രതികണം അഥവാ പോസിട്രോണ് (positron) ആകുന്നു ഇത്. ഇത്തരത്തിലുള്ള ഒരു കണം പിന്നീട് പരീക്ഷണങ്ങളിലൂടെ കണ്ടെത്തുകയുണ്ടായി. 2mc2-ല് കൂടുതലായി ഊര്ജമുള്ള ഫോട്ടോണുകള് ചിലപ്പോള് ഇലക്ട്രോണ്-പോസിട്രോണ് യുഗ്മങ്ങളായി രൂപാന്തരപ്പെടാറുണ്ട്. ഇലക്ട്രോണുകള്-അല്ലെങ്കില് തത്തുല്യമായ ഡിറാക്കണങ്ങള്-വൈദ്യുതകാന്തമണ്ഡലത്തോടും മറ്റും അന്യോന്യക്രിയയില്പ്പെടുമ്പോള് അവയ്ക്കുണ്ടാകുന്ന സ്ഥിതിവിശേഷങ്ങളെന്തെന്നും ഡിറാക് സിദ്ധാന്തം വ്യക്തമാക്കുന്നു.
ക്വാണ്ടം സാംഖ്യികം
ക്വാണ്ടം സാംഖ്യികം (Quantum Statistics). ഒരു നിശ്ചിതവ്യൂഹത്തിന് (system) ഒട്ടാകെ ഉണ്ടാകാവുന്ന ഊര്ജം അതിലുള്ള അടിസ്ഥാനഘടകങ്ങള്ക്കിടയില് ഏതു രീതിയിലാണ് വിതരണം ചെയ്യപ്പെട്ടിരിക്കുന്നത് എന്ന് നിര്ണയിക്കുവാന് സാംഖ്യികമായ നിയമങ്ങളെയാണ് ശാസ്ത്രജ്ഞര് അവലംബിക്കുന്നത്. ഉദാ. ഒരു നിശ്ചിത വ്യാപ്തത്തിലൊതുങ്ങി നില്ക്കുന്ന ഒരു വാതകമാണ് ഈ വ്യൂഹമെങ്കില് അതിലുള്ള തന്മാത്രകളെ അടിസ്ഥാനഘടകങ്ങളായി പരിഗണിക്കാം. ഒരു വികിരണ മണ്ഡലമാണ് വ്യൂഹമെങ്കില് ഫോട്ടോണുകളായിരിക്കാം അതിന്റെ ഘടകങ്ങള്. പക്ഷേ ക്ലാസ്സിക്കല് സിദ്ധാന്തവും ക്വാണ്ടം സിദ്ധാന്തവും തമ്മില് അടിസ്ഥാന പ്രമാണങ്ങളെ സംബന്ധിച്ച് വ്യത്യാസമുള്ളതിനാല് ഊര്ജവിതരണനിയമങ്ങള് എല്ലാ വ്യൂഹങ്ങള്ക്കും തുല്യമാവുന്നില്ല. ക്വാണ്ടം പരിഗണനകള് പ്രസക്തമായിട്ടുള്ള വ്യൂഹങ്ങളുടെ സാംഖ്യികമാണ് ക്വാണ്ടം സാംഖ്യികം. ഇതില് രണ്ടു വിഭാഗങ്ങളുണ്ട്; ബോസ്-ഐന്സ്റ്റൈന് സാംഖ്യികവും ഫെര്മി-ഡിറാക് സാംഖ്യികവും.
ബോസ്-ഐന്സ്റ്റൈന് സാംഖ്യികം
പ്ലാങ്കിന്റെ വികിരണനിയമത്തെ സാംഖ്യികമായ അടിസ്ഥാനത്തില് വ്യുത്പാദിപ്പിക്കുവാന് 1924-ല് ബോസ് (S.N. Bose) നടത്തിയ പരിശ്രമത്തിലൂടെയാണ് ആദ്യമായി ക്വാണ്ടം സ്റ്റാറ്റിസ്റ്റിക്സ് രൂപംകൊണ്ടത്. അക്കൊല്ലംതന്നെ വാതകങ്ങളുടെ ഗതിക സിദ്ധാന്തം ആവിഷ്കരിക്കുവാന് ഐസ്റ്റൈന് ഉപയോഗിച്ച സങ്കല്പങ്ങളും അതിനടിസ്ഥാനമായിത്തീര്ന്നു. രണ്ടുകൊല്ലത്തിനുശേഷം ഫെര്മിയും ഡിറാക്കും മറ്റൊരു സാംഖ്യികം അവതരിപ്പിച്ചു. അതാണ് ഫെര്മി-ഡിറാക് സാംഖ്യികം.
ഈ സാംഖ്യികങ്ങളെക്കുറിച്ചു പ്രതിപാദിക്കുന്നതിനുമുമ്പ് ക്ലാസ്സിക്കല് സാംഖ്യികത്തെപ്പറ്റി ചില വസ്തുതകള് പ്രസ്താവിക്കേണ്ടതുണ്ട്. ഒരു വ്യൂഹത്തിലെ ഓരോ അംഗത്തിനും ഊര്ജത്തിന്റെയോ അല്ലെങ്കില് മറ്റേതെങ്കിലും ഗുണധര്മത്തിന്റെയോ ഒരു നിശ്ചിതമൂല്യം ഉണ്ടാകും. സാംഖ്യികഭാഷയില് ഓരോ അംഗവും ആ ഗുണധര്മത്തിന്റെ ഓരോ സെല്ലില് (കള്ളിയില്) വര്ത്തിക്കുന്നുവെന്നു പറയുന്നു. ഉദാഹരണം ലളിതമാക്കാന് ആകെ രണ്ട് അംഗങ്ങളും രണ്ടു കള്ളികളും മാത്രമേയുള്ളൂ എന്ന് കരുതുക. ഓരോ അംഗത്തിനും സ്വതന്ത്രമായ ഒരു തനിമ ഉണ്ടെന്നും ഓരോന്നും മറ്റുള്ളവയില്നിന്നു വ്യത്യസ്തമാണെന്നും ക്ലാസ്സിക്കല് സിദ്ധാന്തം കരുതുന്നു. മാത്രമല്ല, ഓരോ അംഗത്തിനും ഏതു സെല്ലില് വര്ത്തിക്കുവാനും തുല്യമായ സ്വതന്ത്യ്രവുമുണ്ട്. ഇതനുസരിച്ച്, രണ്ടംഗങ്ങളും രണ്ടു സെല്ലുകളുമുള്ളപ്പോള് ഓരോ അംഗവും ഒറ്റയ്ക്ക് ഓരോ സെല്ലിലോ അല്ലെങ്കില് രണ്ടുംകൂടി ഏതെങ്കിലും ഒരു സെല്ലിലോ ആകാം. ഈ വിതരണം താഴെക്കാണുന്ന രീതിയില് ചിത്രീകരിക്കാം (p, q) എന്നിവ അംഗങ്ങള്).
ഇതനുസരിച്ച് നാലു വ്യത്യസ്തമായ വിതരണക്രമങ്ങള് അല്ലെങ്കില് വിതരണ സംഭാവ്യതകള് (Probabilities of distribution) ഉണ്ട്.
ഒരു വാതകത്തിലെ തന്മാത്രകളെപ്പോലെ അംഗങ്ങളുടെ എണ്ണവും സെല്ലുകളുടെ എണ്ണവും അസംഖ്യമായിത്തീരുമ്പോള് വിതരണസംഭാവ്യതയും വര്ധിക്കുന്നു. ഈ സംഭാവ്യതയും എന്ട്രോപ്പി (entropy)യും തമ്മില് ബന്ധപ്പെടുത്തി തന്മാത്രകള്ക്ക് ഒട്ടാകെയുള്ള ഊര്ജം സ്ഥിരമായി നിലനില്ക്കുന്നുവെന്ന അടിസ്ഥാനത്തില്-അതായതു സന്തുലിതാവസ്ഥയില്-ഓരോ സെല്ലിലുമുള്ള അംഗങ്ങളുടെ എണ്ണവും (ns) അതില് ഓരോ അംഗത്തിനുമുള്ള ഊര്ജവും (Es) തമ്മിലുള്ള ബന്ധം കണക്കാക്കുമ്പോള് ക്ലാസ്സിക്കല് സിദ്ധാന്തപ്രകാരം
എന്നു ലഭിക്കുന്നു. f, β എന്നിവ വാതകത്തിനു പ്രസക്തമായ ചില ഫലനങ്ങളാണ്. ഈ സമവാക്യത്തില് അന്തര്ഭവിച്ചിട്ടുള്ള പ്രത്യേകത ഊര്ജം കൂടുതലാകുന്തോറും തന്മാത്രകളുടെ എണ്ണം കുറഞ്ഞുവരുന്നു എന്നതാണ്. ഏറ്റവും കുറഞ്ഞ ഊര്ജമൂല്യത്തിലാണ് ഏറ്റവും കൂടുതല് തന്മാത്രകള് കാണുക.
ബോസ്-ഐന്സ്റ്റൈന് സാംഖ്യികമനുസരിച്ച്, അംഗങ്ങള്ക്കു വെവ്വേറെ വ്യക്തിത്വമില്ല. ഒന്നിനെ മറ്റൊന്നില്നിന്നു തിരിച്ചറിയാവുന്നതല്ല. വിതരണത്തെ സംബന്ധിച്ച് ക്ലാസ്സിക്കല് സിദ്ധാന്തത്തില് നിന്ന് വ്യത്യസ്തമായ വേറെ നിബന്ധനയൊന്നുമില്ല. അതിനാല് താഴെക്കാണും പ്രകാരം മൂന്നു വിതരണങ്ങള് ലഭിക്കുന്നു. (അംഗങ്ങള് സമാനമായതിനാല് അവയെ ബിന്ദുക്കള്കൊണ്ട് സൂചിപ്പിക്കാം.)
ചിത്രത്തിലുള്ള കള്ളികള് എന്തിനെയാണ് പ്രതിനിധാനം ചെയ്യുന്നത് ? ഒരു വാതകത്തിന്റെ ഉദാഹരണമെടുത്താല് അതിലുള്ള ഓരോ തന്മാത്രയ്ക്കും, നൈമിഷികമാണെങ്കിലും, ഓരോ പ്രത്യേകസ്ഥാനവും സംവേഗവുമുണ്ട്. അതനുസരിച്ച് രണ്ടുതരത്തിലുള്ള നിര്ദേശാങ്കങ്ങള് (സ്ഥാനത്തിനും സംവേഗത്തിനും) ആവശ്യമാണ്. ഇവ രണ്ടും ചേര്ന്നുള്ള നിര്ദേശാങ്ക വ്യവസ്ഥയ്ക്ക് ഫെയ്സ് സ്പേസ് (phase space) എന്നു പറയുന്നു. അനിശ്ചിതത്വസിദ്ധാന്തപ്രകാരം സ്ഥാനവും സംവേഗവും ഒരുമിച്ച് കൃത്യമായി നിര്ണയിക്കാന് പറ്റാത്തതിനാല് ഫെയ്സ് സ്പേസിലെ നിര്ദേശാങ്കബിന്ദു ഒരു ചെറിയ 'വ്യാപ്ത'ത്തിനുള്ളില് ഉള്പ്പെടുത്തേണ്ടിവരുന്നു. ഈ വ്യാപ്തത്തെയാണ് സെല് അഥവാ കള്ളി എന്ന പദംകൊണ്ട് ഉദ്ദേശിക്കുന്നത്. അനിശ്ചിതത്വസിദ്ധാന്തമനുസരിച്ച് ഈ കള്ളിയുടെ വ്യാപ്തം ഏകദേശം h3 ആകുന്നു.
ക്വാണ്ടം സിദ്ധാന്തപ്രകാരം വ്യൂഹങ്ങള്ക്കു നിശ്ചിതമായ ഊര്ജമൂല്യങ്ങള് (E1, E2, ...Es.എന്നിങ്ങനെ) ആണുള്ളത്. ഓരോ ഊര്ജസ്തരത്തിനും പ്രസക്തമായി കള്ളികളുടെ ഒരു നിശ്ചിതസംഖ്യയുണ്ട്. Es എന്ന ഊര്ജത്തിന് As കള്ളികളും അവയില് വിതരണം ചെയ്യപ്പെട്ട ns കണികകളും ഉണ്ടെന്നു കരുതുക. മേല്പറഞ്ഞവിധം സമാനമായ കണികകളും വിതരണവും കണക്കാക്കുമ്പോള് ആകെ വിതരണത്തിന്റെ സംഭാവ്യത
വ്യൂഹം സന്തുലിതാവസ്ഥയിലാകുമ്പോള് പ്രസക്തമായ താപഗതിക തത്ത്വങ്ങള് ഇതില് ഉള്പ്പെടുത്താവുന്നതാണ്.
എന്നു ലഭിക്കുന്നു. f എന്നത് വ്യൂഹത്തിന്റെ ഒരു സ്ഥിരാങ്കമാണ്. β = 1/kT. (k = ബോള്ട്സ്മന് സ്ഥിരാങ്കം; T = താപനില). ഇതാണ് ബോസ്-ഐന്സ്റ്റൈന് സാംഖ്യികത്തിന്റെ വിതരണനിയമം.
പ്ലാങ്കിന്റെ വികിരണനിയമം
മേല്പറഞ്ഞ സമവാക്യമുപയോഗിച്ച്, കൃഷ്ണികയുടെ (black body) വികിരണത്തെ സംബന്ധിക്കുന്ന പ്ലാങ്കിന്റെ നിയമം വ്യുത്പാദിക്കുവാന് സാധിക്കും. λ യ്ക്കും ( λ +d λ )യ്ക്കും ഇടയ്ക്കു തരംഗദൈര്ഘ്യമുള്ള ഫോട്ടോണ് കള്ളികളുടെ എണ്ണം (യൂണിറ്റ് വ്യാപ്തത്തില്)
As = 8 π d λ / λ 4
ആകുന്നു. Es എന്നതു ഫോട്ടോണിന്റെ ഊര്ജം = hc/ λ അതിനാല് വികിരണ സാന്ദ്രത (f = 1 എന്നെടുത്താല്)
![]() പ്ലാങ്കിന്റെ നിയമവും ഇതുതന്നെ.
പ്ലാങ്കിന്റെ നിയമവും ഇതുതന്നെ.
ഫെര്മി-ഡിറാക് സാംഖ്യികം
ഈ സാംഖ്യികത്തില്, ഒരു കള്ളിയില് ഒന്നിലധികം കണികകള് ഉണ്ടാകുവാന് പാടില്ലെന്നതാണ് നിബന്ധന. അല്ലെങ്കില് ഒന്നും ഇല്ലെന്നും വരാം. അതിനാല് മേല്ക്കാണിച്ച വിതരണം ഒരു രീതിയില് മാത്രമാകുന്നു. As കള്ളികളും ns കണികകളുമുള്ളപ്പോള്,
വ്യത്യസ്തമായ വിതരണക്രമങ്ങളുടെ എണ്ണം AS!/nS!(AS- nS)! ആകുന്നു. എല്ലാ ഊര്ജസ്തരങ്ങളും പരിഗണിക്കുമ്പോള് ഒട്ടാകെയുള്ള വിതരണ സംഭാവ്യത P = π
s AS!/nS!(AS- nS)! ആയിരിക്കും. ഇതനുസരിച്ച് വിതരണനിയമം 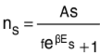 ആകുന്നു.
ആകുന്നു.
ഈ സാംഖ്യികത്തിന് അനവധി പ്രയോഗങ്ങളുണ്ട്. അവയില് ഏറ്റവും മൗലികമായിട്ടുള്ളത് ലോഹങ്ങളെ സംബന്ധിക്കുന്ന ഇലക്ട്രോണ് സിദ്ധാന്തത്തിലാണ്. ലോഹങ്ങള്ക്കുള്ളില് സ്വതന്ത്രമായ ഇലക്ട്രോണുകളുടെ ഒരു 'വാതകം' വര്ത്തിക്കുന്നുണ്ട് എന്ന സങ്കല്പത്തെ അടിസ്ഥാനപ്പെടുത്തിയാണ് അവയുടെ താപീയവും വൈദ്യുതവുമായ ചാലകത, താപീയ വൈദ്യുതി, പ്രകാശവൈദ്യുത പ്രഭാവം മുതലായ ഗുണധര്മങ്ങളെ വ്യാഖ്യാനിക്കുന്നത്. ഈ വാതകത്തെ ക്ലാസ്സിക്കല് സാംഖ്യികത്തിന്റെ രീതിയില് പരിഗണിക്കുമ്പോള് ഏറെക്കുറെ തൃപ്തികരമായ വിശദീകരണമേ മേല്പറഞ്ഞ പ്രതിഭാസങ്ങളെ സംബന്ധിച്ച് ലഭിക്കുന്നുള്ളൂ. മാത്രമല്ല, ലോഹങ്ങളുടെ വിശിഷ്ട താപത്തെ (specific heat) സംബന്ധിക്കുന്ന പ്രശ്നങ്ങളില് അത് പരാജയപ്പെടുകയും ചെയ്തു.
1928-ല് ഈ പ്രമേയത്തെ ക്വാണ്ടം സാംഖ്യികത്തിന്റെ കാഴ്ചപ്പാടില് സോമര്ഫെല്ഡ് (sommerfeld) വിശകലനം ചെയ്തു. ഇലക്ട്രോണ് സ്വതന്ത്രമാണെങ്കിലും ലോഹത്തിന്റെ സീമകള്ക്കകത്തുള്ള ഒരു പൊട്ടന്ഷ്യലില് അത് ഒതുങ്ങിനില്ക്കുകയാണെന്നും പൗളിയുടെ അപവര്ജനനിയമം അനുസരിക്കുന്ന ഇലക്ട്രോണിനു പ്രസക്തമായത് ഫെര്മി-ഡിറാക് സാംഖ്യികമാണെന്നും അദ്ദേഹം സങ്കല്പിച്ചു. ഇതനുസരിച്ച് ഒരു ലോഹത്തിലുള്ള ഇലക്ട്രോണുകള്ക്ക് താഴെ വിവരിക്കുന്ന ഗുണധര്മങ്ങളുണ്ടെന്നു സിദ്ധിക്കുന്നു.
ശൂന്യാങ്ക ഊര്ജം
ശൂന്യാങ്ക ഊര്ജം (Zero-point energy). ഫെര്മി-ഡിറാക് സാംഖ്യികമനുസരിച്ച് ഇലക്ട്രോണുകള്ക്ക് കേവല താപനില പൂജ്യമാകുന്ന അവസ്ഥയിലും ഒരു ശരാശരി ഊര്ജം ![]() ഉണ്ട്;
ഉണ്ട്;
(n = യൂണിറ്റ് വ്യാപ്തത്തിലുള്ള ഇലക്ട്രോണുകളുടെ എണ്ണം; m = ഇലക്ട്രോണിന്റെ ദ്രവ്യമാനം). ക്ലാസ്സിക്കല് സിദ്ധാന്തമനുസരിച്ച് പൂജ്യതാപനിലയില് ഊര്ജം ശൂന്യമാകുന്നു. പക്ഷേ ഇലക്ട്രോണുകളുടെ എണ്ണമനുസരിച്ച് പൂജ്യം മുതല് ഒരു പ്രത്യേക ഊര്ജസ്തരം വരെ ഇലക്ട്രോണുകള് വിതരണം ചെയ്യപ്പെട്ടിരിക്കുന്നു എന്നാണ് ഈ സാംഖ്യികം നല്കുന്ന നിഗമനം. മേല്ക്കാണുന്ന ചിത്രം ഈ വിതരണരീതി വ്യക്തമാക്കുന്നു.
ഏറ്റവും ഉയര്ന്ന ഊര്ജം E0 ആണെങ്കില് ശരാശരി ഊര്ജം,![]() ആണെന്നും സിദ്ധാന്തത്തില്നിന്നു ലഭിക്കുന്നു.
ആണെന്നും സിദ്ധാന്തത്തില്നിന്നു ലഭിക്കുന്നു.
വിശിഷ്ട താപം
വിശിഷ്ട താപം (Specefic heat). ക്ലാസ്സിക്കല് സിദ്ധാന്തമനുസരിച്ച് ലോഹങ്ങളുടെ താപം പരീക്ഷണങ്ങളില് കാണുന്നതിലുമധികം ഉയര്ന്നിരിക്കണം. പക്ഷേ ഫെര്മി-ഡിറാക് സാംഖ്യികം ഇതിനു തൃപ്തികരമായ വിശദീകരണം നല്കുന്നു. താപനില ഉയരുന്നതനുസരിച്ച് ഇലക്ട്രോണുകളുടെ ഒട്ടാകെയുള്ള ഊര്ജം സാരമായി വര്ധിക്കുന്നില്ല. അതായത് വിശിഷ്ടതാപത്തിലേക്ക് ഇലക്ട്രോണുകള് നല്കുന്ന സംഭാവന ചെറുതാണ്. ഒരു ഇലക്ട്രോണിന്റെ വിശിഷ്ടതാപം (Cv) സ്ഥിരവ്യാപ്തത്തില്,
ആകുന്നു. താപനില (T)യ്ക്ക് ആനുപാതികമാണിത്. പൂജ്യം താപനിലയില് ഇതു ശൂന്യവുമാണ്. വിശിഷ്ടതാപത്തിനു പ്രധാനമായ സംഭാവന അണുക്കളില് നിന്നാണുണ്ടാവുന്നത്. വളരെ ഉയര്ന്ന താപനിലയില് മാത്രം Cv-യുടെ മൂല്യം, നിരീക്ഷിക്കപ്പെടാവുന്ന വിധത്തില് ഉയരുന്നു. താപനില ഉയരുന്തോറും വിതരണക്രമം ക്ലാസ്സിക്കല് സാംഖ്യികത്തോടു സാദൃശ്യമുള്ളതായിത്തീരുന്നു.
അനുകാന്തത
അനുകാന്തത (Paramagnetism). പല ലോഹങ്ങള്ക്കും, പ്രത്യേകിച്ച് ക്ഷാരലോഹങ്ങള്ക്ക് (alkali metals) കാന്തശീലത (susceptibility) കുറവാണ്. മാത്രമല്ല, താപനിലയനുസരിച്ച് സാരമായ മാറ്റവും അതിനു സംഭവിക്കുന്നില്ല. ക്ലാസ്സിക്കല് സാംഖ്യികമനുസരിച്ച് വിശദീകരിക്കാനാവാത്ത ഒരു ഗുണധര്മമാണിത്. 1927-ല് ഫെര്മി-ഡിറാക് സാംഖ്യികത്തെ അടിസ്ഥാനമാക്കി പൗളി ഈ പ്രശ്നത്തിന് ഏറെക്കുറെ തൃപ്തികരമായ ഉത്തരം കണ്ടെത്തുകയുണ്ടായി. ലോഹത്തിലെ സംയോജകത (valency)യ്ക്കു നിദാനമായ ഇലക്ട്രോണുകള് സ്വതന്ത്രമാണെന്നും അവ ഒരു വാതകംപോലെ ലോഹത്തില് വ്യാപിച്ചിരിക്കുകയാണെന്നും അദ്ദേഹം കരുതി. ഈ ഇലക്ട്രോണുകള്ക്ക് അവയുടെ ചക്രണം (spin) ഹേതുവായി ഒരു കാന്തിക ആഘൂര്ണം (magnetic moment) ഉണ്ട്. പൂജ്യതാപനിലയില്, ഓരോ ഫേസ് (phase) കള്ളിയിലും ഈ രണ്ട് ഇലക്ട്രോണുകള് വര്ത്തിക്കുന്നു. അവയുടെ ചക്രണങ്ങള് വിപരീതദിശയിലായതിനാല്, കാന്തിക ആഘൂര്ണങ്ങള് സന്തുലിതമാണ്. പക്ഷേ ഒരു കാന്തികക്ഷേത്രം പ്രയോഗിക്കുമ്പോള്, ഇലക്ട്രോണുകളുടെ ചക്രണങ്ങള്ക്ക് ആ ക്ഷേത്രത്തിനു സമാന്തരമായ ദിശയിലേക്കു മാറാനുള്ള പ്രവണതയുണ്ടാവുന്നു. ഒരേ കള്ളിയില് സമാനമായ രണ്ടു ഇലക്ട്രോണുകള് വര്ത്തിക്കുവാന് സാധ്യമല്ലാത്തതുകൊണ്ട് രണ്ട് ഇലക്ട്രോണിനും ഒരേ ദിശയിലുള്ള ചക്രണം സാധ്യമല്ല. അതിനാല് ഒരു ഇലക്ട്രോണ് പൂരിതമല്ലാത്തതും ഉയര്ന്ന ഊര്ജസ്തരമുള്ളതുമായ ഏതെങ്കിലും കള്ളിയിലേക്കു നീങ്ങുന്നു. ഇതുകൊണ്ട് പദാര്ഥത്തിന് ചെറിയതോതിലുള്ള കാന്തത ലഭിക്കുന്നു. താപനില ഉയരുമ്പോഴും ഈ പ്രക്രിയതന്നെയാണുണ്ടാവുന്നത്. എങ്കിലും കാന്തത ഗണ്യമായി വര്ധിക്കുന്നില്ല. ഇലക്ട്രോണ് വാതകത്തിനു പൗളി കണ്ടെത്തിയ കാന്തശീലത.
(n = യൂണിറ്റ് വ്യാപ്തത്തിലുള്ള ഇലക്ട്രോണുകളുടെ എണ്ണം) കാന്തശീലത താപനിലയോടു ബന്ധപ്പെടുന്നതല്ലെന്ന് ഈ സമവാക്യം വ്യക്തമാക്കുന്നു.
മേല് കാണിച്ച ചില ഉദാഹരണങ്ങള്ക്കു പുറമേ ഫെര്മി-ഡിറാക് സാംഖ്യികം വസ്തുക്കളുടെ മറ്റനേകം ഗുണധര്മങ്ങളെയും വിശദമാക്കുവാന് സഹായകമായിട്ടുണ്ട്.
ക്വാണ്ടം സാംഖ്യികവും അണുകേന്ദ്രവും
മൗലികകണങ്ങളെ അവയുടെ സാംഖ്യികമനുസരിച്ച് രണ്ടായി തിരിച്ചിട്ടുണ്ട്; ബോസ് ഐന്സ്റ്റൈന് സാംഖ്യികം അനുസരിക്കുന്നവയെ ബോസോണുകള് (Bosons)എന്നും ഫെര്മി-ഡിറാക് സാംഖ്യികം അനുസരിക്കുന്നവയെ ഫെര്മിയോണുകള് (Fermions) എന്നും പറയുന്നു. ഫെര്മി സാംഖ്യികത്തെ അനുസരിക്കുന്ന മൗലികകണങ്ങളുടെ ഒരു വ്യൂഹം ഏതു സാംഖ്യികത്തെ അനുസരിക്കുമെന്നുള്ളത് ആ വ്യൂഹത്തിലുള്ള കണങ്ങളുടെ എണ്ണംകൊണ്ടാണ് നിര്ണയിക്കേണ്ടത്. ഇത് ഇരട്ട (even number) ആണെങ്കില് ബോസ് സാംഖ്യികവും ഒറ്റ (odd) ആണെങ്കില് ഫെര്മി സാംഖ്യികവുമാണ്. കണങ്ങളെ തമ്മില്ത്തമ്മില് മാറ്റിയാല്, വ്യൂഹത്തിലെ തരംഗഫലനത്തിന്റെ ചിഹ്നം (sign) മാറുമോ ഇല്ലയോ എന്നുള്ളതാണ് സാംഖ്യികനിര്ണയനത്തിന്റെ അടിസ്ഥാനം. ഒരണുകേന്ദ്രത്തിലെ പ്രോട്ടോണുകളുടെ എണ്ണം Z-ഉം ന്യൂട്രോണുകളുടെ എണ്ണം A - Z-ഉം ആണെന്നിരിക്കട്ടെ. പരീക്ഷണങ്ങളില്നിന്ന് പ്രോട്ടോണുകള്ക്ക് ഫെര്മി സാംഖ്യികമാണുള്ളത് എന്ന് മനസ്സിലാക്കാം. ഒരു പ്രോട്ടോണും ഒരു ന്യൂട്രോണും കൂടിച്ചേരുമ്പോള്, കണങ്ങളുടെ എണ്ണം ഇരട്ടസംഖ്യയായതിനാല് ബോസ് സാംഖ്യികം ലഭിക്കുന്നു. ഇതുപോലെ പ്രോട്ടോണ്-ന്യൂട്രോണ് കണങ്ങളുടെ, അതായത് അണുവിന്റെ ദ്രവ്യമാനസംഖ്യ (A) ഇരട്ടയായാല് ബോസ് സാംഖ്യികവും ഒറ്റയായാല് ഫെര്മി സാംഖ്യികവുമാണ് അണുകേന്ദ്രത്തിനുള്ളത്. വ്യൂഹത്തിന്റെ തരംഗഫലനം സമമിതം (symmetric)ആണെങ്കില് ബോസ് സാംഖ്യികവും പ്രതിസമമിതം (antisymmetric) ആണെങ്കില് ഫെര്മി സാംഖ്യികവും ആയിരിക്കും എന്നതാണ് നിയമം. ഒരു കണത്തിന്റെ ചക്രണം പൂര്ണസംഖ്യയാണെങ്കില് ബോസ് സാംഖ്യികവും പൂര്ണസംഖ്യയല്ലെങ്കില് ഫെര്മി സാംഖ്യികവുമാണ് ആ കണത്തിന് പ്രസക്തമായിട്ടുള്ളത്.
ക്വാണ്ടം ഭൗതികത്തിലെ പുതിയ പരീക്ഷണങ്ങള് (2012) ഏറെ ശ്രദ്ധേയമായ വസ്തുതയാണ്. 'ഏകമായ ക്വാണ്ടം സിസ്റ്റ'ത്തിന്റെ (individual quantum system) നിയന്ത്രണ-നിരീക്ഷണ - മാപന പഠനസഹായകമായ പുതിയ സാങ്കേതികരീതികള് കണ്ടെത്തിയത് 2012-ലെ ഭൗതികശാസ്ത്രത്തിനുള്ള നോബല് സമ്മാനത്തിന് ഫ്രഞ്ച് ശാസ്ത്രജ്ഞനായ സെര്ജ് ഹരോഷിനെയും (1944 -) അമേരിക്കന് ശാസ്ത്രജ്ഞനായ ഡേവിഡ് ജെ. വൈന്ലാന്ഡിനെയും (1944 -) അര്ഹരാക്കി. ഇന്നുള്ള അറ്റോമിക ഘടികാരങ്ങള് നല്കുന്ന കൃത്യതയെക്കാള് കൂടുതല് കൃത്യതയാര്ന്ന അറ്റോമിക ക്ളോക്കുകള് നിര്മ്മിക്കാനും 'ഷോഡിംഗര് ക്യാറ്റ്' (schrodinger cat) സമാന അവസ്ഥകളുടെ അസംസക്ത (decoherence) പഠനത്തിനും ക്വാണ്ടം കംപ്യൂട്ടര് വികസിപ്പിച്ചെടുക്കാനും ഈ കണ്ടുപിടുത്തം സഹായകമാണ്.
(ഡോ. സി.പി. മേനോന്, പ്രൊഫ. കെ. പാപ്പുട്ടി., സ.പ)