This site is not complete. The work to converting the volumes of സര്വ്വവിജ്ഞാനകോശം is on progress. Please bear with us
Please contact webmastersiep@yahoo.com for any queries regarding this website.
Reading Problems? see Enabling Malayalam
കാര്ബണിക ലോഹസംയുക്തങ്ങള്
സര്വ്വവിജ്ഞാനകോശം സംരംഭത്തില് നിന്ന്
കാര്ബണിക ലോഹസംയുക്തങ്ങള്
Organometallic Compounds
കാര്ബണ് അണുവും ലോഹ അണുവും തമ്മില് രാസബന്ധം നിലനില്ക്കുന്ന യൗഗികങ്ങള്. ലോഹകാര്ബണേറ്റുകള് പോലെയുള്ള അകാര്ബണിക ലവണങ്ങള് ഈ വിഭാഗത്തില്പ്പെടുന്നില്ല. കാര്ബണിക, അകാര്ബണിക സംയുക്തങ്ങളുടേതില്നിന്നു വ്യത്യസ്തമായ സ്വഭാവവിശേഷങ്ങള് കാര്ബണിക ലോഹസംയുക്തങ്ങള്ക്കുണ്ട്.
സംയുക്തത്തിലെ ലോഹസ്വഭാവത്തെയും കാര്ബണ്ലോഹബന്ധനത്തെയും ആധാരമാക്കി മൂന്നുതരത്തിലുള്ള വിഭജനം കല്പിച്ചുപോരുന്നുണ്ട്:
(i) ആവര്ത്തനപ്പട്ടികയില് ഒന്നും രണ്ടും ഗ്രൂപ്പുകളില്പ്പെടുന്ന ധനവിദ്യുത്ലോഹങ്ങള് നിര്മിക്കുന്ന അയോണിക സംയുക്തങ്ങള്. ഉദാ. മീഥൈല് സോഡിയം, ഡൈഫിനൈല് മഗ്നീഷ്യം. ഈ സംയുക്തങ്ങള്ക്ക് ബാഷ്പീകരണ ശീലമില്ല. കാര്ബണിക ലായകങ്ങളില് കഷ്ടിച്ചു മാത്രമേ ഇവ ലയിക്കൂ. വളരെയധികം ക്രിയാശീലത പ്രകടിപ്പിക്കുന്നു. ഈ സംയുക്തങ്ങള് ജ്വലനശീലമുള്ളവയും ജലാപഘടനത്തിനു വിധേയമാകുന്നവയുമാണ്. ഈ വിഭാഗത്തില്പ്പെടുന്ന കാര്ബണിക ലോഹസംയുക്തങ്ങളില് ലിഥിയം, ബെറിലിയം, മഗ്നീഷ്യം തുടങ്ങിയവയുടെ അയോണിക സ്വഭാവം മറ്റുള്ളവയുടേതില്നിന്ന് താരതമ്യേന കുറവാണ്;
(ii) സംക്രമണലോഹങ്ങള് (Transition metals)ഒഴികെയുള്ള ലോഹങ്ങളും III, IV, V, VI ഗ്രൂപ്പുകളിലെ ഉപലോഹങ്ങളും (metalloids) നിര്മിക്കുന്ന സഹസംയോജക കാര്ബണിക സംയുക്തങ്ങള്. ഉദാ. ഡൈമീഥൈല് മെര്ക്കുറി, ട്ര ഈഥൈല് അലുമിനിയം, ടെട്രാമീഥൈല് ടിന്. ഇവ ബാഷ്പശീലമുള്ളവയും കാര്ബണിക ലായകങ്ങളില് ലയിക്കുന്നവയുമാണ്. ഇവ ജലത്തില് അലേയമാണ്.
(iii) സംക്രമണ ലോഹങ്ങളുടെ കാര്ബണിക സംയുക്തങ്ങള്. ആരോമാറ്റിക ഗ്രൂപ്പുകളുമായോ അവയോടു സാദൃശ്യമുള്ള ഗ്രൂപ്പുകളുമായോ ഉണ്ടാക്കുന്ന "സാന്വിച്ച്' (sandwich) പ്രരൂപത്തിലുള്ള ബന്ധനമാണ് ഈ വിഭാഗം സംയുക്തങ്ങളുടെ പ്രത്യേകത. ഉദാ. ഫെറോസിന്
കാര്ബണിക ലോഹ സംയുക്തത്തിലെ കാര്ബണ് വിഭാഗം പ്രകൃതത്തിലും സ്വഭാവത്തിലും വിഭിന്നങ്ങളായിരിക്കും. ലഘുഹൈഡ്രാ കാര്ബണുകള്, അപൂരിത ഹൈഡ്രാ കാര്ബണുകള്, ആരോമാറ്റിക ഹൈഡ്രാ കാര്ബണുകള്, കാര്ബണും ഹൈഡ്രജനും ഒഴികെയുള്ള അണുകങ്ങള് അടങ്ങിയ ഗ്രൂപ്പുകള്, ലോഹകാര്ബണൈലുകള്, ലോഹ ഐസോസയനൈഡുകള് തുടങ്ങിയവയെല്ലാം കാര്ബണിക ലോഹസംയുക്തങ്ങളില്പ്പെടുന്നു.
ചരിത്രം. കാര്ബണിക ലോഹസംയുക്തങ്ങളെപ്പറ്റി ആദ്യം അറിയുന്നത് 19-ാം നൂറ്റാണ്ടിലാണ്. 1827ല് ഡാനിഷ് രസതന്ത്രജ്ഞനായ ഡബ്ല്യു. സി. സീസ് KCI. P Cl2.C2H4. H2O എന്ന സംയോഗമുള്ള ഒരു സംയുക്തത്തെ നിര്മിക്കുകയുണ്ടായി. പ്ലാറ്റിനം ക്ലോറൈഡ് ഈഥൈല് ആല്ക്കഹോളില് തിളപ്പിച്ചുണ്ടാക്കിയ മിശ്രിതത്തില് പൊട്ടാസിയം ക്ലോറൈഡ് ചേര്ത്താണ് ഇത് നിര്മിച്ചത്. കാര്ബണ് ലോഹബന്ധമുള്ള ഒരു സംയുക്തമാണിതെന്ന് [K (C2H4Pt Cl3). H2O] നൂറുവര്ഷങ്ങള്ക്കുശേഷമാണ് സ്ഥാപിക്കപ്പെട്ടത്. 1842ല് തന്നെ ജര്മന് രസതന്ത്രജ്ഞനായ റോബര്ട്ട് ബുണ്സണ് "കാക്കൊഡൈല്' എന്ന കാര്ബണിക ആര്സെനിക് സംയുക്തവും [(CH3)2 As As (CH3)2] 1849ല് ഇംഗ്ലീഷ് രസതന്ത്രജ്ഞനായ സര് എഡ്വേഡ് ഫ്രാങ്ക്ലാന്റ് കാര്ബണിക സിങ്ക് സംയുക്തങ്ങളും നിര്മിക്കുകയുണ്ടായി. കാര്ബണിക ലോഹസംയുക്തങ്ങളുടെ ചരിത്രത്തിലെ സുപ്രധാനമായ ഒരു കണ്ടെത്തലാണ് ഗ്രിഗ്നാര്ഡ് റിയേജന്റുകള് എന്ന പേരില് പ്രശസ്തമായ കാര്ബണിക മഗ്നീഷ്യം സംയുക്തങ്ങള്. 1900ല് ഫ്രഞ്ചു രസതന്ത്രജ്ഞനായ വിക്ടര് ഗ്രിഗ്നാര്ഡ് ആണ് ഇവ വികസിപ്പിച്ചെടുത്തത്. 1912ല് ഇദ്ദേഹം പ്രസ്തുത കണ്ടെത്തലിലൂടെ നോബല് സമ്മാനിതനാവുകയും ചെയ്തു. 1909ല് പോള് എര്ലിഖ് "സല്വര്സാന്' എന്ന പേരില് ഒരു കാര്ബണിക ആര്സെനിക് സംയുക്തം, സിഫിലിസ് രോഗചികിത്സയിലുപയോഗിക്കാമെന്ന് കണ്ടെത്തി. ഫെറോസിന് കണ്ടെത്തിയതിനു (1951) ശേഷമാണ് കാര്ബണിക ലോഹരസതന്ത്രശാഖയില് കാര്യമായ ഗവേഷണങ്ങള് നടന്നിട്ടുള്ളത്. അതുവരെ മറ്റു ചില കാര്ബണിക സംയുക്തങ്ങളുടെ നിര്മാണത്തിനുള്ള അസംസ്കൃത പദാര്ഥങ്ങള് എന്നൊരുസ്ഥാനം മാത്രമേ കാര്ബണിക ലോഹസംയുക്തങ്ങള്ക്ക് ഉണ്ടായിരുന്നുള്ളൂ. ഇതിനുശേഷം കാര്ബണിക ലോഹരസതന്ത്രമേഖലയിലുണ്ടായ ഒരു പ്രധാന കണ്ടുപിടുത്തം കാള് സീഗ്ളറും ഗിലിയോ നാറ്റയും സംയുക്തമായി കണ്ടെത്തിയ സീഗ്ളര്നാറ്റ ഉത്പ്രരകം (Zeigler-Natta Catalyst) ആണ്. 1963ല് ഈ കണ്ടുപിടുത്തത്തിന് ഇവര്ക്ക് നോബല് സമ്മാനം ലഭിക്കുകയുണ്ടായി. ഫെറോസീനിന്റെ സാന്വിച്ച് ഘടന കണ്ടെത്തിയത് ഇത്തരത്തിലുള്ള മറ്റു സംയുക്തങ്ങളുടെ കണ്ടെത്തലിലേക്ക് വഴിതെളിച്ചു. പ്രസ്തുത കണ്ടെത്തലിലൂടെ ജെഫ്രി വില്ക്കിന്സണും ഏണസ്റ്റ് ഓട്ടോഫിഷറും 1973ലെ നോബല് പുരസ്കാരത്തിന് അര്ഹനായി.
ബന്ധനരൂപങ്ങള്. പല തരത്തിലുള്ള കാര്ബണ് ലോഹബന്ധനങ്ങളാണ് കാര്ബണിക ലോഹസംയുക്തങ്ങളിലുള്ളത്.
(1) സാധാരണ സഹസംയോജക ബന്ധനങ്ങള് (covalent bonds). അണുകങ്ങളിലെ ഇലക്ട്രാണുകള് പങ്കുവച്ച് ഇത്തരം ബന്ധനം ഉണ്ടാകുന്നു. ഉദാ. ടെട്രാ ഈഥൈല് ലെഡ് (C2H5)4Pb.
(2) അയോണികബന്ധനങ്ങള്. ഇലക്ട്രാണ് ജോടികള് ഒരു ആറ്റത്തില് നിന്ന് മറ്റൊന്നിലേക്ക് നീക്കപ്പെടുന്നു. ചാര്ജുകള് രൂപംകൊള്ളുകയും ചെയ്യുന്നു. ഉദാ. ഈഥൈല് പൊട്ടാസിയം K+C2H5-).
(3) ബഹുകേന്ദ്രിത സഹസംയോജക ബന്ധനങ്ങള്. ഇതില് ബന്ധനം ഒരു പറ്റം ആറ്റങ്ങളെ ഉള്ക്കൊള്ളുന്നു. ഉദാ. ഹെക്സാമെറിക ഈഥൈല് ലിഥിയം C2H5Li)6 (4) ദാതാസ്വീകാരി (donor-acceptor) ബന്ധനങ്ങള്. ഉദാ. ഫെറോസിന്ബിസ് (p സൈക്ലോ പെന്റാഡൈയീനൈല്) അയോണ്, (p-C5H5) Fe.
നിര്മാണവിധികള്.
(i) ലോഹങ്ങളും കാര്ബണിക ഹാലൈഡുകളും തമ്മിലുള്ള പ്രതിപ്രവര്ത്തനം.
ലിഥിയം, സോഡിയം, മഗ്നീഷ്യം തുടങ്ങിയവയുടെ കാര്ബണിക സംയുക്തങ്ങളെ ഇപ്രകാരം നിര്മിക്കാം. Si, Ge എന്നിവ വാതകപ്രാവസ്ഥയിലാണ് പ്രതിപ്രവര്ത്തിക്കുന്നത്.
(ii) ഉത്തേജിത (active) ഹൈഡ്രജന് അടങ്ങിയിട്ടുള്ള ഹൈഡ്രാകാര്ബണുകളും ഉന്നത പ്രതിപ്രവര്ത്തനക്ഷമതയുള്ള ലോഹങ്ങളും തമ്മിലുള്ള പ്രതിപ്രവര്ത്തനം.
അസറ്റിലിന്, ട്രഫീനൈല് മീഥേന്, സൈക്ലോപെന്റാഡയീന് എന്നിവയുടെ കാര്ബണിക ലോഹസംയുക്തങ്ങള് ഈ രീതിയില് നിര്മിക്കുന്നു.
(iii) ഉയര്ന്ന പ്രതിപ്രവര്ത്തനക്ഷമതയുള്ള ലോഹങ്ങളുടെ കാര്ബണിക വ്യുത്പന്നങ്ങള് താരതമ്യേന കുറഞ്ഞ പ്രതിപ്രവര്ത്തനക്ഷമതയുള്ള ലോഹങ്ങളുടെ ലവണങ്ങളുമായി പ്രതിപ്രവര്ത്തിപ്പിക്കല്.
ആല്ക്കൈല് സോഡിയം യൗഗികങ്ങള്, ആല്ക്കൈല് ലിഥിയം സംയുക്തങ്ങള്, ഗ്രിഗ്നാര്ഡ് റീയേജന്റുകള് എന്നിവ III, IV, V, VI ഗ്രൂപ്പുകളിലെ മൂലകങ്ങളുമായി നടത്തുന്ന പ്രതിപ്രവര്ത്തനം. സംക്രമണ ലോഹങ്ങളുടെ സൈക്ലോപെന്റാഡൈയീനൈല് വ്യുത്പന്നങ്ങള് ഈ ക്രിയാവിധിയിലൂടെ സൗകര്യമായി ഉത്പാദിപ്പിക്കാം.
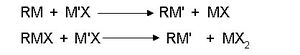
(iv) വിനിമയ പ്രതിപ്രവര്ത്തനങ്ങള്. ഉദാ.
(v) മെറ്റലേഷന്. ഒരു കാര്ബണിക ലോഹയൗഗികവും ക്രിയാശീലഹൈഡ്രജന് അടങ്ങിയ ആരോമാറ്റിക ഹൈഡ്രാകാര്ബണും തമ്മിലുള്ള പ്രതിപ്രവര്ത്തനം ![]() . ഏറ്റവും പ്രധാനപ്പെട്ട മെറ്റലേറ്റിങ് ഏജന്റാണ് n ബ്യൂട്ടൈല് ലിഥിയം (ഈഥര് ലായനിയില്). ബന്ധപ്പെട്ട ആരൈല് ഹാലൈഡുകള് n ബ്യൂട്ടൈല് ലിഥിയവുമായി പ്രതിപ്രവര്ത്തിപ്പിച്ച് ആരോമാറ്റികഹൈഡ്രാകാര്ബണുകളുടെ ഒട്ടധികം ആരോമാറ്റിക കാര്ബണിക ലോഹസംയുക്തങ്ങള് ഉത്പാദിപ്പിച്ചുവരുന്നു.
. ഏറ്റവും പ്രധാനപ്പെട്ട മെറ്റലേറ്റിങ് ഏജന്റാണ് n ബ്യൂട്ടൈല് ലിഥിയം (ഈഥര് ലായനിയില്). ബന്ധപ്പെട്ട ആരൈല് ഹാലൈഡുകള് n ബ്യൂട്ടൈല് ലിഥിയവുമായി പ്രതിപ്രവര്ത്തിപ്പിച്ച് ആരോമാറ്റികഹൈഡ്രാകാര്ബണുകളുടെ ഒട്ടധികം ആരോമാറ്റിക കാര്ബണിക ലോഹസംയുക്തങ്ങള് ഉത്പാദിപ്പിച്ചുവരുന്നു.
ഗുണധര്മങ്ങള്. രാസഭൗതിക ഗുണധര്മങ്ങളില് തികഞ്ഞ വ്യത്യസ്തത പുലര്ത്തുന്നവയാണ് കാര്ബണിക ലോഹസംയുക്തങ്ങള്. ചിലത് വായുവില് തീപിടിക്കുന്നു. വേറെ ചിലത് തികച്ചും സുസ്ഥിരങ്ങളാണ്. ഫെറോസിന് വായുവിന്റെ അസാന്നിധ്യത്തില് 470oC വരെ സുസ്ഥിരമായി നില്ക്കുന്നു. പ്രധാനമായും ഖര, ദ്രാവകരൂപങ്ങളില് ഈ യൗഗികങ്ങള് സ്ഥിതിചെയ്യുന്നു. ചിലത് കാര്ബണിക ലായകങ്ങളില് ലയിക്കും. സാമാന്യ പ്രതിപ്രവര്ത്തനക്ഷമതയുള്ള എല്ലാ കാര്ബണിക ലോഹസംയുക്തങ്ങളും എല്ലാ ക്രിയാത്മക ഗ്രൂപ്പുകളുമായും (functional group) പ്രതിപ്രവര്ത്തിക്കുന്നു. ഓക്സീകരണം, അമ്ലങ്ങളാലുള്ള വിഭജനം അഥവാ പിളര്ക്കല് എന്നിവയാണ് കാര്ബണിക ലോഹസംയുക്തങ്ങള്മൂലം ഉണ്ടാകുന്ന രണ്ടു മുഖ്യപ്രതിപ്രവര്ത്തന രീതികള്.
ചില കാര്ബണിക ലോഹസംയുക്തങ്ങളെ ആവര്ത്തനപ്പട്ടിക അടിസ്ഥാനമാക്കി പരിശോധിക്കാം.
ഒന്നാം ഗ്രൂപ്പ് യൗഗികങ്ങള്. ആല്ക്കലി ലോഹങ്ങള് ഉയര്ന്ന ക്രിയാശീലതയുള്ള കാര്ബണിക ലോഹസംയുക്തങ്ങള് ഉത്പാദിപ്പിക്കുന്നു. ലിഥിയത്തിന്റെ ഉയര്ന്ന ആല്ക്കൈല് വ്യുത്പന്നങ്ങള് ഒഴികെ (ഇവ ദ്രാവകങ്ങളാണ്) ഈ ഗ്രൂപ്പിലെ മറ്റ് എല്ലാത്തിന്റെയും ആല്ക്കൈല് വ്യുത്പന്നങ്ങള് നിറമില്ലാത്ത ഖരവസ്തുക്കളാണ്. മിക്ക ആല്ക്കൈല്സംയുക്തങ്ങളും കടുത്തനിറമുള്ള ഖരപദാര്ഥങ്ങളാണ്. ലിഥിയത്തിന്റേതൊഴികെ മിക്ക ആല്ക്കൈല് സംയുക്തങ്ങളും മിക്കവാറും എല്ലാ കാര്ബണികലോഹസംയുക്തങ്ങളിലും അലേയമാണ്. ഇവയ്ക്ക് ബാഷ്പീകരണശീലവും ഉരുകാനുള്ള പ്രവണതയും കുറവാണ്. ഈ ഗ്രൂപ്പിലെ കാര്ബണിക സംയുക്തങ്ങള്ക്ക് പൊതുവേ അയോണിക സ്വഭാവമുണ്ട്. ലിഥിയം അയോണിന്റെ ഉയര്ന്ന ധ്രുവക്ഷമതയും (polarising power) അണുകവലുപ്പവും അവയുടെ കാര്ബണിക യൗഗികങ്ങള്ക്ക് സഹസംയോജക സ്വഭാവം നല്കുന്നു. ഉയര്ന്ന പ്രതിപ്രവര്ത്തന സ്വഭാവമുള്ളതിനാല് കാര്ബണിക ക്ഷാരസംയുക്തങ്ങളുടെ നിര്മാണവും പ്രയോഗവും ഓക്സിജന്, നീരാവി, കാര്ബണ് ഡൈ ഓക്സൈഡ് മുതലായവയുടെ അസാന്നിധ്യത്തിലാണ് നടക്കുന്നത്. ഉയര്ന്ന ക്രിയാശീലമുള്ളവയാണ് കാര്ബണിക ലിഥിയം സംയുക്തങ്ങള്. സംശ്ലേഷിത കാര്ബണിക രസതന്ത്രത്തില് ഇടയൗഗികങ്ങ(intermediates)ളായി ഇവ വ്യാപകമായി ഉപയോഗിക്കുന്നു. കാര്ബണ്കാര്ബണ് ബഹുബന്ധനങ്ങളുമായി സങ്കലനം നടത്തുവാന് കഴിവുള്ളതിനാല് ഇവ, പോളിഒലിഫീനുകള്, കൃത്രിമറബ്ബര് എന്നിവയുടെ വ്യാവസായികോത്പാദനത്തില് ഉപയോഗപ്പെടുത്തുന്നു. കാര്ബണിക ലിഥിയം സംയുക്തങ്ങളെ കാര്ബണ്ഡൈ ഓക്സൈഡും ആല്ഡിഹൈഡ്/കീറ്റോണുമായി പ്രതിപ്രവര്ത്തിപ്പിച്ച് ജലാപഘടനത്തിനു വിധേയമാക്കുമ്പോള് ഉയര്ന്ന അളവില് കാര്ബോക്സിലിക് അമ്ലവും ആല്ക്കഹോളും ലഭിക്കുന്നു.
രണ്ടാം ഗ്രൂപ്പ് യൗഗികങ്ങള്. Ca, Sr, Ba എന്നിവയുടെ കാര്ബണിക ലോഹയൗഗികങ്ങളെക്കുറിച്ച് വിശദമായ പഠനം നടന്നിട്ടില്ലെങ്കിലും റേഡിയം ഒഴികെ രണ്ടാം ഗ്രൂപ്പിലെ എല്ലാ മൂലകങ്ങളും കാര്ബണിക ലോഹസംയുക്തങ്ങള് ഉണ്ടാക്കുന്നുവെന്ന് പറയാം. മെര്ക്കുറിയുടേതൊഴികെ ഗ്രൂപ്പിലെ മറ്റ് എല്ലാ മൂലകങ്ങളുടെയും കാര്ബണിക സംയുക്തങ്ങള് ഓക്സിജനിലും നീരാവിയിലും തീ പിടിക്കുന്നു. സംയോജിത (associated) ദ്രാവകങ്ങളാണെങ്കിലും ആല്ക്കൈല്ബെറിലിയം സംയുക്തങ്ങള് ബാഷ്പശീലതയുള്ളവയാണ് (ഡൈ മീഥൈല് ബെറിലിയം അപവാദം). ആരൈല് ബെറിലിയം ഏറെക്കുറെ സ്ഥിരതയുള്ളവയാണ്.
ആല്ക്കൈല്, ആരൈല് മഗ്നീഷ്യം സംയുക്തങ്ങളും (R2 Mg) കാര്ബണിക മഗ്നീഷ്യം ഹാലൈഡുകളും (RMg X) ആണ് മഗ്നീഷ്യത്തിന്റെ മുഖ്യകാര്ബണിക സംയുക്തങ്ങള്. ഇവയില് രണ്ടാമതു പറഞ്ഞവ വളരെ പ്രധാനപ്പെട്ടവയാണ്. ഇവയെ ഗ്രിഗ്നാര്ഡ് റിയേജന്റുകള് എന്നു പറയുന്നു. രസതന്ത്രത്തിലെ അതിപ്രധാനങ്ങളായ ഒരുകൂട്ടം യൗഗികങ്ങളാണിവ. മഗ്നീഷ്യവും ആല്ക്കൈല് ഹാലൈഡും ഈര്പ്പരഹിതവും ആല്ക്കഹോള് മയം ഇല്ലാത്തതുമായ ഈഥറില്വച്ച് പ്രതിപ്രവര്ത്തിപ്പിച്ചാണ് ഗ്രിഗ്നാര്ഡ് റിയേജന്റിനെ ഉത്പാദിപ്പിക്കുന്നത്.
അയൊഡൈഡ്ബ്രാമൈഡ് ക്ലോറൈഡ് എന്നതാണ് ഒരു ആല്ക്കൈല് ഹാലൈഡിന് ഏറ്റവും എളുപ്പം പ്രതിപ്രവര്ത്തിക്കാവുന്നതിന്റെ ക്രമം. അതേപോലെ തന്നെ ആല്ക്കൈല് ഗ്രൂപ്പില് കാര്ബണിന്റെ എണ്ണം കൂടുന്തോറും ഗ്രിഗ്നാര്ഡ് റിയേജന്റിന്റെ രൂപീകരണം വിഷമമാവുന്നു. ഹൈഡ്രാകാര്ബണുകള്, ആല്ഡിഹൈഡുകള്, കീറ്റോണുകള്, അമ്ലങ്ങള്, ആല്ക്കൈല് സയനൈഡുകള്, അമീനുകള് തുടങ്ങിയവയുടെ സംശ്ലേഷണത്തിന് ഗ്രിഗ്നാര്ഡ് റിയേജന്റുകള് ഉപയോഗപ്പെടുത്തിവരുന്നു.
ആല്ക്കൈല്, ആരൈല് മഗ്നീഷ്യം സംയുക്തങ്ങള് വെളുത്ത, ക്രിസ്റ്റലീകൃത ഖരപദാര്ഥങ്ങളാണ്. ബാഷ്പീകരണശീലമില്ല. ഹൈഡ്രാകാര്ബണ് ലായകങ്ങളില് അലേയമാണ്. മഗ്നീഷ്യവും കാര്ബണികഗ്രൂപ്പും തമ്മില് സഹസംയോജകബന്ധം നിലനില്ക്കുന്നതായി കരുതപ്പെടുന്നു.
ഈ ഗ്രൂപ്പിലെ സിങ്ക്, കാഡ്മിയം എന്നിവയുടെ യൗഗികങ്ങള് ആദ്യം കണ്ടെത്തിയ കാര്ബണിക ലോഹസംയുക്തങ്ങളില്പ്പെടുന്നവയാണ്. ഇവയുടെ ആല്ക്കൈല് സംയുക്തങ്ങള് ദ്രാവകങ്ങളും ആരൈല് സംയുക്തങ്ങള് ഖരങ്ങളുമാണ്. R2 Hg, RHg X എന്നീ സംഘടനങ്ങളിലുള്ള മെര്ക്കുറി സംയുക്തങ്ങളും വേര്തിരിക്കപ്പെട്ടിട്ടുണ്ട്. മെര്ക്കുറിയുടെ ആല്ക്കൈല്, ആരൈല് സംയുക്തങ്ങള് ക്രിസ്റ്റലീകൃത ഖരപദാര്ഥങ്ങളാണ്. ഇവയിലും സഹസംയോജക ബന്ധനങ്ങള് പ്രതീക്ഷിക്കുന്നു.
മൂന്നാം ഗ്രൂപ്പ് സംയുക്തങ്ങള്. ഈ ഗ്രൂപ്പിലെ മിക്കകാര്ബണിക ലോഹസംയുക്തങ്ങളും വായുസാന്നിധ്യത്തില് തീപിടിക്കുന്നവയാണ്. ബോറോണിന്റെ ആല്ക്കൈല് യൗഗികങ്ങള് നിറമില്ലാത്ത ദ്രാവകങ്ങളും ആരൈല് സംയുക്തങ്ങള് ക്രിസ്റ്റലീയ ഖരപദാര്ഥങ്ങളുമാണ്. അലുമിനിയത്തിന്റെ ആല്ക്കൈല് സംയുക്തങ്ങള് അങ്ങേയറ്റം പ്രതിപ്രവര്ത്തനക്ഷമതയുള്ള നിറമില്ലാത്ത ദ്രാവകങ്ങളാണ്. ഇവ പോളിമെറീകരണ പ്രക്രിയകളില് രാസത്വരകങ്ങളായി ഉപയോഗിച്ചുവരുന്നു. ഗാലിയം, ഇന്ഡിയം, താലിയം എന്നിവയുടെ ചില കാര്ബണിക സംയുക്തങ്ങളും അറിയപ്പെടുന്നുണ്ട്. ഈ കൂട്ടത്തില് ഏറ്റവും ആധുനികമായ ഒന്നാണ് സൈക്ലോപെന്റാഡൈയീനൈല് ഇന്ഡിയം,C2 H2 In.
നാലാം ഗ്രൂപ്പ് യൗഗികങ്ങള്. Si, Ge, Sn, Pb എന്നിവ R4 M പ്രരൂപത്തിലുള്ള കാര്ബണിക ലോഹസംയുക്തങ്ങളെ ഉത്പാദിപ്പിക്കുന്നു. എല്ലാസംയുക്തങ്ങളിലും സഹസംയോജക ബന്ധനമാണുള്ളത്. മൂലകത്തിന്റെ ലോഹസ്വഭാവം വര്ധിക്കുന്തോറും കാര്ബണ് ലോഹബന്ധനം ദുര്ബലമാകുന്നു. ഈ വിഭാഗത്തിലെ സംയുക്തങ്ങളുടെ ഒരു പ്രത്യേകത അവയില് ലോഹലോഹബന്ധനങ്ങളും നിലനില്ക്കുന്നുവെന്നതാണ്. ഈ ഗ്രൂപ്പിലെ ആല്ക്കൈല് സംയുക്തങ്ങള് ദ്രാവകങ്ങളാണ്. ആരൈല് സംയുക്തങ്ങള് ഖരങ്ങളും. ഈ രണ്ടുതരം സംയുക്തങ്ങളും ജലവുമായും വായുവുമായും പ്രതികരിക്കുന്നില്ല. എല്ലാംതന്നെ ഹൈഡ്രാകാര്ബണ് ലായകങ്ങളില് ലയിക്കുന്നു.
അഞ്ച്, ആറ് ഗ്രൂപ്പ് യൗഗികങ്ങള്. ഗ്രൂപ്പ് v മൂലകങ്ങള്, R3M, R5M എന്നീ പ്രരൂപങ്ങളിലുള്ള കാര്ബണിക ലോഹസംയുക്തങ്ങള് ഉത്പാദിപ്പിക്കുന്നു. ഗ്രൂപ്പ് ആറിലെ സെലിനിയം, ടെല്ലൂറിയം എന്നിവ R2M പ്രരൂപത്തിലുള്ള സംയുക്തങ്ങള്ക്കു രൂപംനല്കുന്നു. RM-MR പ്രരൂപത്തിലുള്ള ഏതാനും ഡൈസെലിനൈഡുകളും ഡൈടെലൂറൈഡുകളും വേര്തിരിച്ചിട്ടുണ്ട്.
സംക്രമണ ലോഹയൗഗികങ്ങള്. മറ്റു വിഭാഗം കാര്ബണിക ലോഹസംയുക്തങ്ങളില്നിന്നു വ്യത്യസ്തമാണ് സംക്രമണലോഹങ്ങളുടെ കാര്ബണിക സംയുക്തങ്ങള്. ഈ ഗ്രൂപ്പില് ആദ്യം കണ്ടെത്തിയ സംയുക്തം ഡൈസൈക്ലോപെന്റാഡൈയീനൈല് അയണ് [(C5H5)2Fe] ആണ്. ഇത് ഫെറോസിന് എന്ന് അറിയപ്പെടുന്നു. ഫെറസ് അയോണും ആരോമാറ്റിക രാസസ്വഭാവമുള്ള കാര്ബണിക ഭാഗത്തോടുകൂടിയ രണ്ടു സൈക്ലോപെന്റാഡയിന് തന്മാത്രകളും അടങ്ങിയ ഒരു കോഓര്ഡിനേഷന് (Co-ordination) സംയുക്തമാണിത്. സാന്വിച്ച് ഘടന (sandwich structure) ആണ് ഇതിന്റേത് എന്നു പറയാം. സമാന്തരമായ രണ്ടു സൈക്ലോപെന്റാഡൈയീനൈല് വലയങ്ങളും അവയുടെ നടുവിലായി എല ആറ്റവും ഉണ്ട്. വലയങ്ങളിലെ p ഓര്ബിറ്റലുകളും തമ്മില് ബന്ധനം നിലനിര്ത്തിയിരിക്കും. ഓറഞ്ചുനിറവും ക്രിസ്റ്റല് ഘടനയുമുള്ള ഖരപദാര്ഥമാണ് ഫെറോസിന്. കര്പ്പൂരത്തിന്റെ ഗന്ധമാണ് ഇതിന്. ദ്രവണാങ്കം 173-174oC. ജലത്തില് അലേയം, ബെന്സീന്, ഈഥര് എന്നിവയില് അല്പമായി ലയിക്കും. 400oC വരെ ചൂടാക്കിയാല് വിഘടനമില്ല. സംയുക്തത്തിലെ ഇരുമ്പിന്റെ അളവ് 29.430.6 ശതമാനം. വിഘടിക്കുമ്പോള് വിഷപദാര്ഥങ്ങള് ഉണ്ടാകുന്നു. അന്ഹൈഡ്രഡ് സോഡിയം ഈഥോക്സൈഡിന്റെ സാന്നിധ്യത്തില് ഫെറസ് ക്ലോറൈഡും സൈക്ലോപെന്റാഡൈയിനും തമ്മില് പ്രതിപ്രവര്ത്തിപ്പിച്ച് നിര്മിക്കാം. ഉയര്ന്ന ആരോമാറ്റിക സ്വഭാവം പ്രകടിപ്പിക്കുന്ന ഈ പദാര്ഥത്തിന്റെ കണ്ടെത്തല് ഈ പ്രകൃതത്തിലുള്ള നിരവധി സംയുക്തങ്ങളുടെ ഉത്പാദനത്തിനും അങ്ങനെ രസതന്ത്രത്തില് മെറ്റലോസീനുകള് എന്ന പേരില് ഒരു പുതിയ മേഖലതുറക്കുന്നതിനും കാരണമായി. ഒട്ടനവധി സംക്രമണലോഹങ്ങളുടെ സൈക്ലോപെന്റാഡൈയീനൈല് സംയുക്തങ്ങള് കണ്ടെത്തിക്കഴിഞ്ഞു. ഡൈബെന്സീന് ക്രാമിയം [(C6H5)2Cr], യുറാനോസീന് [(C8H8)2U] എന്നിവ ഇവയില് ചിലതാണ്. മിക്കവയ്ക്കും സാന്വിച്ച് ഘടനയാണുള്ളത്. പ്രതിഓക്സീകാരക ഉത്പ്രരകം, ഫോട്ടോ സ്റ്റബിലൈസര്, ഫ്യുവല് അഡിറ്റീവുകള് എന്നിവയായി സംക്രമണലോഹസംയുക്തങ്ങള് ഉപയോഗിക്കുന്നു.
ഉപയോഗങ്ങള്. കാര്ബണിക സംയുക്തങ്ങളുടെ സംശ്ലേഷണങ്ങളില് ഉത്പ്രരകം, അഭികാരകം എന്നീ നിലകളിലും പെട്രാളിയം അധിഷ്ഠിത വ്യവസായങ്ങളിലുമാണ് കാര്ബണിക ലോഹസംയുക്തങ്ങള് വ്യാപകമായി ഉപയോഗിക്കുന്നത്. കൂടാതെ, ഔഷധങ്ങള്, കാര്ഷിക രാസവസ്തുക്കള് എന്നിവയായും ഇവ ഉപയോഗിച്ചുവരുന്നു. ഉയര്ന്ന ക്രിയാശീലത, സ്ഥിരത, ശുദ്ധലോഹങ്ങള് പുനരുത്പാദിപ്പിക്കാനുള്ള കഴിവ് എന്നീ ഗുണങ്ങളാണ് ഉത്പ്രരകം, അഭികാരകം എന്നീ നിലകളില് ഇവയെ ശ്രഷ്ഠമാക്കുന്നത്. പോളി എഥിലീന്, പോളി പ്രാപ്പിലീന് എന്നിവയുടെ ഉത്പാദനത്തില് സീഗ്ളര്നാറ്റ ഉത്പ്രരകം [(C2H5)3Al-TiCl3] ഉപയോഗിക്കുന്നു. ആല്ക്കീനുകളുടെ ഹൈഡ്രജനീകരണത്തില് വില്ക്കിന്സണ്സ് ഉത്പ്രരക [(Ph3P)3RhCl] മാണ് ഉപയോഗിക്കുന്നത്. മോണ്സാന്റോ പ്രക്രിയയില് അസറ്റിക് അമ്ലം ഉത്പാദിപ്പിക്കുന്നത് Fe, CO, Ni എന്നിവയുടെ കാര്ബണൈലുകള് ഉത്പ്രരകമായി ഉപയോഗിച്ചാണ്. ആല്ക്കീനുകളില് നിന്ന് ആല്ഡിഹൈഡ് നിര്മിക്കുന്ന ഓക്സോ പ്രക്രിയയിലും ഉത്പ്രരകമായി വര്ത്തിക്കുന്നത് ലോഹകാര്ബണൈലാണ്. കാര്ബണിക സംശ്ലേഷണങ്ങളില് കാര്ബണ്കാര്ബണ്ബന്ധന രൂപീകരണത്തിന് ഗില്മാന് അഭികാരകം (R2CuLi) പ്രയോജനപ്പെടുത്തുന്നു. കാര്ബണിക ടിന്സംയുക്തങ്ങള് പിവിസിക്ക് സ്ഥിരത നല്കുവാനുപയോഗിക്കുന്നു. കൂടാതെ കുമിള് നാശിനിയായും ചില സസ്യരോഗങ്ങള്ക്കെതിരെ ഔഷധമായും ഉപയോഗിച്ചുവരുന്നു. ട്രബ്യൂട്ടൈല് ടിന് ഓക്സൈഡ് (C24H54OSn2) ഒരു വ്യാവസായിക ജൈവനാശിനിയും (Industrial biocide) രോഗാണുനാശിനിയുമാണ്. കാര്ബണിക മെര്ക്കുറി സംയുക്തങ്ങള് മൂത്രസംവര്ധകമായി ചികിത്സാരംഗത്ത് വ്യാപകമായി ഉപയോഗിച്ചിരുന്നുവെങ്കിലും ഉയര്ന്ന വിഷമയതമൂലം ഇവ ഇപ്പോള് ഉപയോഗിക്കുന്നില്ല. മെര്ക്കുറി സംയുക്തമായ മെര്ക്കുറോക്രാം (C20H8Br2HgNa2O6) സാധാരണയായി ഉപയോഗിക്കുന്ന ഒരു ആന്റിസെപ്റ്റിക്കാണ്.
(ചുനക്കര ഗോപാലകൃഷ്ണന്)