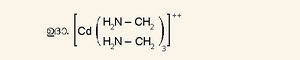This site is not complete. The work to converting the volumes of സര്വ്വവിജ്ഞാനകോശം is on progress. Please bear with us
Please contact webmastersiep@yahoo.com for any queries regarding this website.
Reading Problems? see Enabling Malayalam
കാഡ്മിയം
സര്വ്വവിജ്ഞാനകോശം സംരംഭത്തില് നിന്ന്
കാഡ്മിയം
Cadmium
ഒരു ലോഹമൂലകം. സിംബല് ഇറ, അണുസംഖ്യ 48, അണുഭാരം 112.41, ക്വഥനാങ്കം 767ºC, ദ്രവണാങ്കം 320.9ºC, ആപേക്ഷിക ഘനത്വം 8.65. പ്രധാനമായും സിങ്ക് അയിരുകളോടൊപ്പം കാണപ്പെടുന്ന കാഡ്മിയത്തിന്റെ ഭൗമോപരിതലത്തിലെ സാന്നിധ്യം വെറും 0.01 ശതമാനം ആണ്. സ്വതന്ത്ര കാഡ്മിയം, പ്രകൃതിയില് കാണപ്പെടാത്തതുകൊണ്ടും ഉള്ള ധാതുക്കളില് കാഡ്മിയത്തിന്റെ അളവ് വളരെ കുറവായതുകൊണ്ടും കാഡ്മിയം ലോഹം നമുക്കു ലഭിക്കുന്നത് പ്രധാനമായും സിങ്ക് അയിരുകളുടെ ശുദ്ധീകരണ (Refining) പ്രക്രിയയുടെയും പുടംവയ്ക്കല് (smelting) പ്രക്രിയയുടെയും ഉപോത്പന്നമായാണ്. കാഡ്മിയം വേര്തിരിച്ചെടുത്തത് (1817) എഫ്. സ്റ്റ്രാമയേര് എന്ന ശാസ്ത്രജ്ഞനാണ്.
കാഡ്മിയത്തിന്റെ ഒരു പൂര്ണധാതു ഗ്രീനൊക്കൈറ്റ് ആണ് (Cadmium sulfide) സിങ്ക് അയിരായ "കാഡ്മിയ' (Cadmia) എന്ന വാക്കില്നിന്നുമാണ് കാഡ്മിയം എന്ന സംജ്ഞ ഉണ്ടായത്. അമേരിക്കന് ഐക്യനാടുകള്, കാനഡ, മെക്സിക്കോ, ആസ്റ്റ്രലിയ ബെല്ജിയം-ലക്സംബര്ഗ്, കൊറിയന് റിപ്പബ്ലിക് എന്നിവിടങ്ങളിലാണ് പ്രധാനമായും കാഡ്മിയം നിക്ഷേപങ്ങള് കാണപ്പെടുന്നത്.
നിഷ്കര്ഷണം. സിങ്കിനെക്കാള് ബാഷ്പശീലമുള്ള ഒന്നാണ് കാഡ്മിയം. കാഡ്മിയം അടങ്ങിയ സിങ്ക് അയിരുകള് ഉരുക്കുമ്പോള് ലഭിക്കുന്ന ആദ്യഭാഗം സിങ്കില്, കാഡ്മിയം ഓക്സൈഡ് കലര്ന്ന സിങ്ക് ഓക്സൈഡ് ഉണ്ടായിരിക്കും. ധൂളീരൂപത്തിലുള്ള ഈ മിശ്രിതം കല്ക്കരിയുമായി കലര്ത്തി സ്വേദനം ചെയ്യുമ്പോള് ലഭിക്കുന്ന അസംസ്കൃത കാഡ്മിയം വീണ്ടും മരക്കരിയുമായി ചേര്ത്തു കളിമണ്ണുകൊണ്ടുള്ള റിട്ടോര്ട്ടുകളില് സ്വേദനം ചെയ്യുന്നു. അതില്നിന്നു ലഭിക്കുന്ന കാഡ്മിയം കൂടുതല് ശുദ്ധമായിരിക്കും.
CdO + C → Cd + CO
മേല്പ്രകാരം ലഭിച്ച കാഡ്മിയം വിദ്യുത്-അപഘടനംവഴി ശുദ്ധീകരിച്ചെടുക്കുന്നു. വീണ്ടും ഹൈഡ്രജന് നിറഞ്ഞ അന്തരീക്ഷത്തില് ഉത്പതനം നടത്തി പരിശുദ്ധമായ കാഡ്മിയം ഉണ്ടാക്കുന്നു.
ഭൗതിക-രാസഗുണങ്ങള്. കാഡ്മിയത്തിന്റെ നിറം ടിന്പോലെ വെളുപ്പ് (ടിന്വൈറ്റ്) ആണ്. ഈ ലോഹം മൃദുവും അടിച്ചു പരത്താവുന്നതും വലിച്ചു നീട്ടാവുന്നതും ആണ്. കാഡ്മിയം ആവര്ത്തനപ്പട്ടികയില് ഗ്രൂപ്പ് II Bയിലാണ് സ്ഥിതിചെയ്യുന്നത്. സിങ്ക്, മെര്ക്കുറി എന്നിവയാണ് ഈ ഗ്രൂപ്പിലെ മറ്റു മൂലകങ്ങള്. കാഡ്മിയത്തിന്റെ ഇലക്ട്രാണ് വിന്യാസം 4d10 552. കാഡ്മിയത്തിന്റെ സമസ്ഥാനീയങ്ങള് എട്ടെണ്ണം പ്രകൃത്യാ കാണപ്പെടുന്ന സ്ഥിരതയുള്ളവയും പതിനൊന്നെണ്ണം അസ്ഥിരവും കൃത്രിമവുമാണ്. ഇവ 104 cd മുതല് 118 cd വരെയാണ്. ഇത് വെള്ളവുമായി പ്രതിപ്രവര്ത്തിക്കുന്നില്ല. വായുവില് കാഡ്മിയം തീ പിടിപ്പിച്ചാല് കത്തുന്നു. കത്തുമ്പോള് തവിട്ടുനിറത്തിലുള്ള ഒരു പുകയുണ്ടാകുന്നു. ഇതു കാഡ്മിയത്തിന്റെ ഓക്സൈഡ് ആണ്. നേര്പ്പിച്ച ഹൈഡ്രാക്ലോറിക് ആസിഡിലും സള്ഫ്യൂരിക് ആസിഡിലും കാഡ്മിയം പതുക്കെ പ്രതിപ്രവര്ത്തിച്ച് ഹൈഡ്രജന് ഉത്പാദിപ്പിക്കുന്നു. നൈട്രിക് ആസിഡുമായി പ്രതിപ്രവര്ത്തിച്ച് നൈട്രജന്റെ വിവിധ ഓക്സൈഡുകള് ഉണ്ടാക്കുന്നു. സാധാരണ കാഡ്മിയത്തിന്റെ ലവണങ്ങള് നിറമില്ലാത്തവയും വിഷമുള്ളവയും ആണ്. കാഡ്മിയം ക്ലോറിനില് കത്തുമ്പോള് കാഡ്മിയം ക്ലോറൈഡ് ഉണ്ടാകുന്നു.
യൗഗികങ്ങള്. കാഡ്മിയത്തിന്റെ സംയോജകത 2 ആണ്. കാഡ്മിയം യൗഗികങ്ങളുടെ ലായനികള്ക്കു ചാലകത വളരെ കുറവാണ്. പ്രത്യേകിച്ചും ഹാലൈഡുകളുടെ കുറഞ്ഞ ചാലകതയ്ക്കു കാരണം അവ ഉണ്ടാക്കുന്ന ഓട്ടോ കോംപ്ലക്സുകളാണ്.
ചില പ്രധാന കാഡ്മിയം യൗഗികങ്ങള്.
i. കാഡ്മിയം ഓക്സൈഡ് (CdO). കാഡ്മിയം ലോഹം വായുവില് കത്തിച്ചോ, കാഡ്മിയം കാര്ബണേറ്റ്, കാഡ്മിയം നൈട്രറ്റ് എന്നിവ ജ്വലിപ്പിച്ചോ കാഡ്മിയം ഓക്സൈഡ് ഉണ്ടാക്കുന്നു. തവിട്ടുനിറത്തിലുള്ള ഈ പൊടിക്കു ക്ഷാരഗുണമാണുള്ളത്.
ii. കാഡ്മിയം കാര്ബണേറ്റ് (CdCO3). ഏതെങ്കിലും കാഡ്മിയം ലവണത്തിന്റെ ലായനിയില് ഒരു കാര്ബണേറ്റ് ലായനി ഒഴിച്ചാല് വെളുത്ത ഒരു അവക്ഷിപ്തമായി കാഡ്മിയം കാര്ബണേറ്റ് പുറത്തുവരുന്നു. സാധാരണയായി ഇതോടൊപ്പം അല്പം ഹൈഡ്രാക്സൈഡും ഉണ്ടായിരിക്കും. കാഡ്മിയം കാര്ബണേറ്റ് ചൂടാക്കിയാല് കാഡ്മിയം ഓക്സൈഡും കാര്ബണ് ഡൈ ഓക്സൈഡുമായി വിയോജിക്കപ്പെടുന്നു.
iii. കാഡ്മിയം ഹൈഡ്രാക്സൈഡ് (Cd(OH)2). സോഡിയത്തിന്റെയോ പൊട്ടാസിയത്തിന്റെയോ ഹൈഡ്രാക്സൈഡ് വെളുത്തനിറത്തിലുള്ള ഒരു അവക്ഷിപ്തമായി ലഭിക്കുന്നു. അമോണിയയുമായി ലയിച്ച് ഇതൊരു കോംപ്ലക്സ് അയോണ് [Cd (NS3)4]++ ആയി മാറുന്നു. കാഡ്മിയം ഹൈഡ്രാക്സൈഡ് കാര്ബണ് ഡൈ ഓക്സൈഡിനെ അവശോഷണം ചെയ്യുന്നു.
iv. കാഡ്മിയം ഹാലൈഡുകള്. കാഡ്മിയം ഫ്ളൂറൈഡ് ഒഴിച്ചുള്ള എല്ലാ ഹാലൈഡുകളും ചൂടാക്കിയാല് ബാഷ്പീകൃതമാകുന്നു. അവയുടെ വെള്ളത്തിലുള്ള ലേയത്വം ഫ്ളൂറൈഡിന് ഏറ്റവും കുറവും അയഡൈഡിന് ഏറ്റവും കൂടുതലും ആണ്. കാഡ്മിയം ഹാലൈഡുകള്ക്കു ജലത്തില് ചാലകത ഏറ്റവും കുറവാണ്. ഇതിന് കാരണം അവ ഓട്ടോ കോംപ്ലക്സ് ഉണ്ടാക്കുന്നു എന്നതാണ്.
v. കാഡ്മിയം സള്ഫൈഡ് (CdS). കാഡ്മിയം ലവണങ്ങളുടെ അമ്ലലായനികളില്ക്കൂടി ഹൈഡ്രജന് സള്ഫൈഡ് കടത്തിവിട്ടാല് കടുത്ത മഞ്ഞനിറത്തിലുള്ള കാഡ്മിയം സള്ഫൈഡ് അവക്ഷിപ്തമായി പുറത്തുവരുന്നു. കാഡ്മിയം സള്ഫൈഡ് വിലകൂടിയ മഞ്ഞവര്ണകം ആണ്. "കാഡ്മിയം യെല്ലോ' എന്ന പേരില് പ്രചാരം നേടിയ ഈ വര്ണകം ചിത്രകാരന്മാര് ധാരാളമായി ഉപയോഗിക്കുന്നുണ്ട്.
vi. കാഡ്മിയം സള്ഫേറ്റ് (CdSO4). കാഡ്മിയമോ അതിന്റെ ഓക്സൈഡോ നേര്ത്ത സള്ഫ്യൂരിക് ആസിഡില് ലയിപ്പിച്ച് കാഡ്മിയം സള്ഫേറ്റ് ഉണ്ടാക്കുന്നു. ജലത്തില്നിന്നു ക്രിസ്റ്റലീകരണംവഴി ഇവയുടെ ഏകനതാക്ഷ (monoclinic) രൂപത്തിലുള്ള ക്രിസ്റ്റലുകള് ലഭിക്കുന്നു.
vii. കാഡ്മിയം സയനൈഡ് [Cd(CN)2]. കാഡ്മിയം ലവണങ്ങളുടെ ലായനിയില് ക്ഷാരസയനൈഡുകള് ഒഴിക്കുമ്പോള് വെളുത്ത അവക്ഷിപ്തമായി കാഡ്മിയം സയനൈഡ് പ്രത്യക്ഷപ്പെടുന്നു. കൂടുതല് ക്ഷാരസയനൈഡുകള് കലര്ത്തുമ്പോള് ഇവ സങ്കരലവണമായി മാറുകയും ചെയ്യും.
viii. കാഡ്മിയം നൈട്രറ്റ് [Cd(NO3)2]. കാഡ്മിയമോ അതിന്റെ ഓക്സൈഡ്, ഹൈഡ്രാക്സൈഡ്, കാര്ബണേറ്റ് ഇവയില് ഏതെങ്കിലുമോ നൈട്രിക് അമ്ളത്തില് ലയിക്കുമ്പോള് ഇതുണ്ടാകുന്നു. നിറമില്ലാത്ത ഒരു ക്രിസ്റ്റലീയ ലവണമാണ് കാഡ്മിയം നൈട്രറ്റ്. ഈ യൗഗികം ഉന്നത ഊഷ്മാവില് വിയോജിച്ചു കാഡ്മിയം ഓക്സൈഡ് നല്കുന്നു.
ix. കാഡ്മിയം അമൈഡ് [Cd(ClO4)2]. പൊട്ടാഷ്യം അമൈഡ്, കാഡ്മിയം സയനൈഡുമായി ലിക്കര് അമോണിയയില് കലര്ത്തിയാല് കാഡ്മിയം അമൈഡ് വെളുത്ത അവക്ഷിപ്തമായി ലഭിക്കുന്നു. ഈ യൗഗികം ജലവുമായി അതിദ്രുതം പ്രതിപ്രവര്ത്തിക്കുന്നു.
x. കാഡ്മിയം പെര്ക്ലോറേറ്റ് [Cd(ClO4)2]. കാഡ്മിയം കാര്ബണേറ്റ്, ഓക്സൈഡ്, ഹൈഡ്രാക്സൈഡ് ഇവയില് ഏതെങ്കിലും ഒന്ന് പെര്ക്ലോറിക് ആസിഡുമായി കലര്ത്തിയുണ്ടാകുന്ന ലായനിയില്നിന്നു ക്രിസ്റ്റലീകരണം വഴി കാഡ്മിയം പെര്ക്ലോറേറ്റ് ലഭിക്കും.
ഇരട്ട ലവണങ്ങള് (ഡബിള് സാള്ട്ടുകള്-K2SO4. CdSO46H2O). കാഡ്മിയം സള്ഫേറ്റും പൊട്ടാസ്യം സള്ഫേറ്റും കലര്ത്തി ലഭിക്കുന്ന മിശ്രിതലായനിയില്നിന്നു ക്രിസ്റ്റ്ലീകരണംവഴി ഡബിള് സള്ഫേറ്റുകള് ലഭിക്കുന്നു.
സമ്മിശ്രയൗഗികങ്ങള്. കാഡ്മിയത്തിന്റെ സമ്മിശ്രയൗഗികങ്ങളില് കാഡ്മിയം മൂലകത്തിന്റെ കോ-ഓര്ഡിനേഷന് സംഖ്യ നാലാണ്. ഉദാ. [Cd(NH3)4 ]++ കോ-ഓര്ഡിനേഷന് സംഖ്യ 6 ഉള്ള കോ-ഓര്ഡിനേഷന് യൗഗികങ്ങളും ഉണ്ട്.
ആകലനം (എസ്റ്റിമേഷന്). ഒരു വസ്തുവില് അടങ്ങിയിരിക്കുന്ന കാഡ്മിയം കണ്ടുപിടിക്കാന് ആ വസ്തുവിലെ കാഡ്മിയം, പൊട്ടാസിയം സയനൈഡില് ലയിപ്പിക്കുക. അങ്ങനെ ലഭിക്കുന്ന ലായനി വൈദ്യുതവിശ്ലേഷണം നടത്തുമ്പോള് കാഥോഡില് പറ്റിപ്പിടിക്കുന്ന കാഡ്മിയം അളന്നു കണ്ടുപിടിക്കുന്നു.
ഉപയോഗങ്ങള്. കാഡ്മിയത്തില്നിന്ന് ഉണ്ടാക്കാവുന്ന ഉരുകുന്ന ഒരു മിശ്രലോഹം ആണ് "വുഡ്സ് മെറ്റല്'. ഇതില് നാലുഭാഗം ബിസ്മത്, രണ്ടുഭാഗം ലെഡ്, ഒരുഭാഗം ടിന്, ഒരുഭാഗം കാഡ്മിയം ഇവ അടങ്ങിയിരിക്കുന്നു. ഇതിന്റെ ദ്ര. അ. 71ºC ആണ്. മറ്റൊരു മിശ്രലോഹമായ ലിപ്പോവിറ്റ്സ് അലോയില് 15 ഭാഗം ബിസ്മത്, 8 ഭാഗം ലെഡ്, 4 ഭാഗം ടിന്, 3 ഭാഗം കാഡ്മിയം ഇവ അടങ്ങിയിരിക്കുന്നു. വേഗം ഉരുകുന്ന ഇത്തരം മിശ്രലോഹങ്ങള് ബോയിലറുകളില് സേഫ്റ്റി പ്ലഗ്ഗുകള് ആയി ഉപയോഗിക്കുന്നു.
വെള്ളിയില് കറ പുരളാതിരിക്കാന്വേണ്ടി അല്പം കാഡ്മിയം കലര്ത്താറുണ്ട്. കാഡ്മിയം ചേര്ക്കുമ്പോള് ചെമ്പിന്റെ യാന്ത്രികഗുണം മെച്ചപ്പെടും; ചെമ്പിന്റെ വൈദ്യുത ചാലകത കുറയ്ക്കാതെതന്നെ അതിന്റെ ആയുര്ദൈര്ഘ്യം വര്ധിപ്പിക്കുകയും ചെയ്യും. ആട്ടോമാറ്റിക് അഗ്നിശമന യന്ത്രങ്ങളില് ഉപയോഗിക്കുന്ന ഒരു പ്രധാന ഘടകമാണ് കാഡ്മിയം. സോള്ഡര് ചെയ്യുന്നതിനുള്ള കൂട്ടുലോഹങ്ങളിലും അച്ചടി ടൈപ്പുകളുടെ ആയുര്ദൈര്ഘ്യം കൂട്ടുവാന്വേണ്ടി അവ നിര്മിക്കുന്നതിനുള്ള കൂട്ടുലോഹങ്ങളിലും കാഡ്മിയം ചേര്ക്കുന്നു.
വെസ്റ്റണ് കാഡ്മിയം സെല്ലിലാണ് കാഡ്മിയം പ്രധാനമായും ഉപയോഗിക്കുന്നത്. ഇതിന്റെ ആനോഡില് കാഡ്മിയം അമാല്ഗം ഉപയോഗിക്കുന്നു. ഈ സെല്ലിലെ ഇലക്ട്രാലൈറ്റ് കാഡ്മിയം സള്ഫേറ്റിന്റെ ഒരു പൂരിത ലായനിയാണ്. ഈ സെല്ലിലെ E.M.F. 20ºC-ല് 1.018300 വോള്ട്ട് ആണ്.
കാഡ്മിയത്തിനു വേഗത കുറഞ്ഞ ന്യൂട്രാണുകളെ അവശോഷണം ചെയ്യാനുള്ള കഴിവ് വളരെ കൂടുതലാണ്. ന്യൂക്ലിയര് റിയാക്ടറുകളില് റേഡിയോ ആക്ടിവ് ഫിഷന്മൂലം ഉണ്ടാകുന്ന ന്യൂട്രാണുകളെ കാഡ്മിയം അവശോഷണം ചെയ്യുകയും റിയാക്ടറുകളുടെ പ്രവര്ത്തനം നിയന്ത്രണവിധേയമാക്കുകയും ചെയ്യുന്നു.
ഇരുമ്പ്, ഉരുക്ക് എന്നിവയ്ക്കു ക്ഷാരണം സംഭവിക്കാതിരിക്കാന് ഇത്തരം ലോഹങ്ങളുടെ ഉപരിതലത്തില് ഇലക്ട്രാളിസിസ് വഴി കാഡ്മിയത്തിന്റെ വളരെ കനം കുറഞ്ഞ ഒരു ആവരണം ഉണ്ടാക്കുന്നു. കാഡ്മിയം വളരെ പതുക്കെ വായുവുമായി പ്രതിപ്രവര്ത്തിച്ചുണ്ടാക്കുന്ന കാഡ്മിയം ഓക്സൈഡിന്റെ പാട ഇരുമ്പ്, ഉരുക്ക് എന്നിവയ്ക്ക് വായുവുമായി സമ്പര്ക്കമില്ലാതാക്കുന്നു. കാഡ്മിയവും അതിന്റെ യൗഗികങ്ങളും വിഷാലുത്വം കൂടിയവയായതുകൊണ്ട് അവ കൂടുതല് കാലം കൈകാര്യം ചെയ്യാന് പാടില്ല. ഭക്ഷണസാധനങ്ങളിലുള്ള അമ്ലങ്ങള് കാഡ്മിയവുമായി പ്രവര്ത്തിക്കുമെന്നതുകൊണ്ട് കാഡ്മിയം ആവരണം ചെയ്ത പാത്രങ്ങളില് ഭക്ഷണസാധനങ്ങള് സൂക്ഷിക്കുന്നത് അപകടകരമാണ്.
(പ്രാഫ. എച്ച്.എസ്. മണി)