This site is not complete. The work to converting the volumes of സര്വ്വവിജ്ഞാനകോശം is on progress. Please bear with us
Please contact webmastersiep@yahoo.com for any queries regarding this website.
Reading Problems? see Enabling Malayalam
ഇലക്ട്രോ കെമിസ്ട്രി
സര്വ്വവിജ്ഞാനകോശം സംരംഭത്തില് നിന്ന്
ഇലക്ട്രോ കെമിസ്ട്രി
Electro Chemistry
വൈദ്യുതിയും രാസപരിണാമങ്ങളും തമ്മിലുള്ള ബന്ധം പഠനവിഷയമാക്കിയിട്ടുള്ള വിജ്ഞാനശാഖ. സാധാരണ പരിതഃസ്ഥിതികളിൽ ഒരു രാസപരിണാമം നടക്കുമ്പോള് താപോർജം ആഗിരണം ചെയ്യുകയോ മോചിതമാവുകയോ ചെയ്യാറുണ്ട്. അതുപോലെ വൈദ്യുതോർജം ഉത്പാദിപ്പിക്കുന്ന രാസപരിണാമങ്ങളും ഏറെയുണ്ട്. നേരേമറിച്ച്, വൈദ്യുതോർജമുപയോഗിച്ച് നടക്കുന്ന രാസപരിണാമങ്ങളുമുണ്ട്. ആദ്യത്തെ പ്രക്രിയയിൽ രാസോർജം നേരിട്ട് വൈദ്യുതോർജമായി പരിണമിക്കുന്നു. ഈ രീതിയിൽ വൈദ്യുതി ഉത്പാദിപ്പിക്കാനുള്ള ഉപകരണങ്ങളാണ് സെല്ലുകള് (ഉദാ. ഡാനിയൽ സെൽ). രണ്ടാമത്തെ പ്രക്രിയയിൽ വൈദ്യുതോർജം നേരിട്ടു രാസോർജമായി മാറുന്നു. ഈ പ്രക്രിയയ്ക്ക് വൈദ്യുതവിശ്ലേഷണം (electrolysis)എന്നു പറയുന്നു. സമുചിത സാഹചര്യത്തിൽ വൈദ്യുതവിശ്ലേഷണ ഫലമായുണ്ടാകുന്ന ഉത്പന്നങ്ങളെ വീണ്ടും രാസപരമായി പ്രവർത്തിപ്പിച്ച്, വിശ്ലേഷണാർഥം വ്യയംചെയ്യപ്പെട്ടിട്ടുള്ള വൈദ്യുതോർജത്തെ ഒരു വലിയ അനുപാതത്തോളം തിരിച്ചു ലഭ്യമാക്കുവാനും സാധിക്കും. ഈ തത്ത്വമാണ് സംഭരണ-സെല്ലുകളിൽ ഉപയോഗപ്പെടുത്തിയിട്ടുള്ളത്. ഇപ്പറഞ്ഞതെല്ലാം വിദ്യുത്-രാസപ്രക്രിയകളാണ്. വൈദ്യുതോർജം വഴി ആദ്യം താപോർജം ഉത്പാദിപ്പിച്ച് സാധാരണ താപനിലകളിൽ നടക്കാത്ത രാസപ്രവർത്തനങ്ങളെ സാധിപ്പിക്കുന്ന വിദ്യുത്-താപീയ പ്രക്രിയകളെയും ഇലക്ട്രോ കെമിസ്ട്രിയുടെ പഠന പരിധിയിൽപ്പെടുത്തിയിട്ടുണ്ട്. വാതകങ്ങളിലൂടെ വൈദ്യുതി പ്രവഹിപ്പിക്കുമ്പോള് സാധാരണയായി രാസപരിണാമമുണ്ടാകുന്നു. ഈ പ്രവർത്തനങ്ങളുടെ പഠനം ഇലക്ട്രോ കെമിസ്ട്രിയുടെ ഒരു പ്രത്യേകശാഖയായി പരിഗണിക്കപ്പെട്ടുവരുന്നു.
ചരിത്രം. എ.ഡി. 1800-ൽ ആണ് ഇലക്ട്രോ കെമിസ്ട്രി എന്ന വിജ്ഞാനശാഖയുടെ ആരംഭം. അലക്സാന്ദരോ വോള്ട്ട എന്ന ഇറ്റാലിയന് ശാസ്ത്രജ്ഞന് വിഖ്യാതമായ വോള്ട്ടായി-സെൽ അക്കൊല്ലം കണ്ടുപിടിച്ചു. ചെമ്പ്, നാകം എന്നിവയുടെ തകിടുകള് ഇടവിട്ടടുക്കിവച്ച് ഇടകളിൽ ലവണ ലായനിയിൽ നനച്ചതോ കുതിർത്തതോ ആയ കടലാസ് കഷണങ്ങള് നിറച്ചശേഷം അദ്ദേഹം ചെമ്പുതകിടുകളെല്ലാംകൂടി ഒരു ലോഹക്കമ്പിയിലും നാകത്തകിടുകളെല്ലാംകൂടി മറ്റൊരു ലോഹക്കമ്പിയിലും തൊടുത്ത് പിന്നീട് ഈ ലോഹക്കമ്പികള് തമ്മിൽ സമ്പർക്കമുണ്ടാക്കി. അപ്പോള് ചെമ്പിൽനിന്നു നാകത്തിലേക്ക് ഒരു വൈദ്യുതി ധാരയുണ്ടാകുന്നതായി അദ്ദേഹത്തിനു മനസ്സിലായി. അതേവർഷം തന്നെ നിക്കൊൽസണ്, കാർലൈൽ എന്നിവർ മുന്പ്രസ്താവിച്ച രീതിയിൽ വൈദ്യുതിധാരയുണ്ടാക്കി, അല്പം ആൽക്കലി ചേർത്ത ജലത്തിലൂടെ പ്രവഹിപ്പിച്ച് ഹൈഡ്രജനും ഓക്സിജനും ലഭ്യമാക്കി. വിജ്ഞാന ചരിത്രത്തിൽ ആദ്യം നടത്തപ്പെട്ട വൈദ്യുതവിശ്ലേഷണം ഇതായിരുന്നു. അതിനെത്തുടർന്ന് വൈദ്യുതവിശ്ലേഷണം ഒരു സർവസാധാരണ പരീക്ഷണമായിത്തീർന്നു. ലവണലായനികളിലൂടെ വൈദ്യുതി പ്രവേശിപ്പിച്ച് അവയിലെ ലോഹഘടകങ്ങളെ നിക്ഷേപിപ്പിക്കാമെന്ന് ക്രൂക് ഷാങ്ഖ് കണ്ടുപിടിച്ചു. ലോഹങ്ങളിലൂടെ എന്ന പോലെതന്നെ ലവണങ്ങള്, അമ്ലങ്ങള്, ബേസുകള് എന്നിവയുടെ ലായനികളിലൂടെയും വൈദ്യുതിധാര പ്രവഹിക്കുമെന്നും എന്നാൽ ലായനികളിലൂടെ ധാര കടന്നുപോകുമ്പോള് അവയ്ക്ക് വിശ്ലേഷണം ഉണ്ടാകുന്നു എന്നും അപ്പോള് അമ്ലങ്ങളും അലോഹങ്ങളും ലായനികളിലേക്ക് വൈദ്യുതിധാര പ്രവേശിക്കുന്ന ധന (positive) അഗ്രത്തിലും ഹൈഡ്രജന്, ലോഹങ്ങള്, ആൽക്കലികള് എന്നിവ ലായനിയിൽ നിന്ന് വൈദ്യുതിധാര നിർഗമിക്കുന്ന ഋണ (negative) അഗ്രത്തിലും നിക്ഷേപിക്കപ്പെടുന്നതാണെന്നും 1803-ൽ ബെർസിലിയസ്, ഹിസിംഗർ എന്നിവർ കണ്ടുപിടിച്ചു. 1806-ൽ ഹംഫ്രിഡേവി സോഡിയം, ബേരിയം മുതലായ അനേകം ലോഹങ്ങള് അവയുടെ യൗഗികങ്ങളെ വൈദ്യുതവിശ്ലേഷണത്തിനു വിധേയമാക്കി ഉത്പാദിപ്പിക്കുകയുണ്ടായി. തുടർന്ന്, ഇത്തരം വിശ്ലേഷണങ്ങളെപ്പറ്റി ഡേവിയുടെ ശിഷ്യനായ മൈക്കൽ ഫാരഡേ സുദീർഘവും സുസൂക്ഷ്മവുമായ പാരിമാണിക-പഠനം നടത്തുകയും 1833-ൽ "ഫാരഡേ-നിയമങ്ങള്' എന്നറിയപ്പെടുന്ന വിഖ്യാതങ്ങളായ രണ്ട് വൈദ്യുതവിശ്ലേഷണ നിയമങ്ങള് ആവിഷ്കരിക്കുകയും ചെയ്തു. ശ. വൈദ്യുതിധാരകൊണ്ടു നിക്ഷിപ്തമാകുന്ന പദാർഥത്തിന്റെ പരിമാണം പ്രയുക്തമായ വൈദ്യുതിയുടെ പരിമാണത്തിന് ആനുപാതികമായിരിക്കും; ശശ. ഒരു നിശ്ചിതപരിമാണം വൈദ്യുതി ഉപയോഗിച്ച് നിക്ഷിപ്തമാകുന്ന വിവിധ മൂലകങ്ങളുടെ പരിമാണങ്ങള് അവയുടെ രാസതുല്യാങ്കങ്ങള്ക്ക് ആനുപാതികമായിരിക്കും. ഏതു മൂലകത്തിന്റെയും ഗ്രാം-തുല്യാങ്കഭാരം (gram equivalent weight) നിക്ഷേപിക്കുന്നതിന് ഒരേ പരിമാണം വൈദ്യുതി ആവശ്യമാണെന്ന് ഇതിൽനിന്നനുമാനിക്കാം. അനേകം പരീക്ഷണങ്ങളിലൂടെ ഇത് 96,490 കൂളും (Coulomb) ആണെന്ന് നിർണയിക്കപ്പെട്ടു. ഒരു ഗ്രാം-തുല്യാങ്കഭാരം മൂലകം നിക്ഷേപിക്കുന്നതിന് ആവശ്യമായ ഈ പരിമാണത്തെ ഒരു "ഫാരഡേ' എന്നാണ് ഇന്ന് വ്യവഹരിക്കുന്നത്. ഈ കണ്ടുപിടിത്തങ്ങളെത്തുടർന്ന് ഇല്കട്രോളൈറ്റ്, ഇലക്ട്രോഡ്, ആനോഡ്, കാഥോഡ്, അയോണ്, അനയോണ്, കറ്റയോണ് എന്നീ സംജ്ഞകള് നിഷ്പാദിതങ്ങളാവുകയും നിർവചിക്കപ്പെടുകയും ചെയ്തു.
1834-ൽ ഫാരഡേ പ്ലാറ്റിനം ഇലക്ട്രോഡുകളുപയോഗിച്ച്, ഉരുക്കിയ സോഡിയം ക്ലോറൈഡിലൂടെ വൈദ്യുതി പ്രവഹിപ്പിക്കുകയും സോഡിയം ലോഹവും ക്ലോറിന് വാതകവും രണ്ടിലക്ട്രോഡുകളിൽ നിന്നുമായി ലഭ്യമാക്കുകയും ചെയ്തു. എന്നാൽ സോഡിയം ക്ലോറൈഡിന്റെ ലായനി വൈദ്യുതവിശ്ലേഷണവിധേയമാക്കിയാൽ ആനോഡിൽ നിന്ന് ക്ലോറിന് ലഭിക്കുന്നതാണ്. പക്ഷേ, കാഥോഡിൽ ഉന്മോചിതമാകുന്ന സോഡിയം, ലായകമായ ജലവുമായി രാസപ്രവർത്തനത്തിലേർപ്പെട്ട് സോഡിയം ഹൈഡ്രാക്സൈഡും ഹൈഡ്രജനും ഉത്പാദിപ്പിക്കുന്നു. ഈ ഹൈഡ്രജനാണ് കാഥോഡിൽ നിന്നു കിട്ടുന്ന ഉത്പന്നം. ലായനിയിൽ സോഡിയം ഹൈഡ്രാക്സൈഡിന്റെ അളവ് വർധിച്ചുവരികയും ചെയ്യും. ഇതിൽനിന്നു മനസ്സിലാകുന്നത് ഓരോ വൈദ്യുതവിശ്ലേഷണ പരീക്ഷണത്തിലും കിട്ടുന്ന ഉത്പന്നങ്ങള്, ഇലക്ട്രോളൈറ്റിന്റെ സ്വഭാവം, അതിലെ അയോണുകളുടെ സ്വഭാവം, ഇലക്ട്രോഡുകളുടെയും ലായകത്തിന്റെയും സ്വഭാവം എന്നിവയെ ആശ്രയിച്ചിരിക്കുന്നു എന്നാണ്. ഇലക്ട്രോളിസിസിനെക്കുറിച്ച് ഫാരഡേ അനേകം വിശദപഠനങ്ങള് നടത്തുകയും വ്യാഖ്യാനങ്ങള് നല്കുകയും ചെയ്തു. പക്ഷേ, ഇലക്ട്രോളൈറ്റുകള് എന്തുകൊണ്ട് അയോണുകളായിത്തീരുന്നു എന്നോ ഇലക്ട്രോളൈറ്റ് ലായനികള്ക്ക് അവയുടെ ബാഷ്പമർദം (vapour pressure), ഓസ്മോട്ടികമർദം (osmotic pressure) തുടങ്ങിയ പല ഭൗതികഗുണധർമങ്ങളിലും കാണപ്പെടുന്ന അസാധാരണത്വം എന്തുകൊണ്ടെന്നോ വിശദീകരിക്കുവാന് അദ്ദേഹത്തിനു സാധിച്ചില്ല. 1887-ൽ അരേനീയസ് (Arrhenius)എന്ന ശാസ്ത്രജ്ഞനാണ് ശ്രദ്ധേയമായ ഒരു സിദ്ധാന്തത്തിലൂടെ (അരേനീയസ്-സിദ്ധാന്തം) ഇലക്ട്രോളൈറ്റുകളുടെ സ്വഭാവത്തെക്കുറിച്ചും അവയുടെ ലായനികളുടെ പ്രത്യേകതകളെക്കുറിച്ചും ന്യായയുക്തമായ ഒരു വ്യാഖ്യാനത്തിനുള്ള അടിത്തറ പാകിയത്. പ്രബല-ഇലക്ട്രോളൈറ്റുകളുടെ സവിശേഷതകളെ പൂർണമായും വിശദീകരിക്കുവാന് ഈ സിദ്ധാന്തത്തിന് സാധിച്ചില്ല. പിന്നീട് ഡിബൈ, ഹ്വിക്കൽ, ഓണ്സാഗർ മുതലായവർ ആവിഷ്കരിച്ച സിദ്ധാന്തമാണ് ഈ പോരായ്മ പരിഹരിച്ചത്. അരേനീയസിന്റെ അയോണീകരണ സിദ്ധാന്തം ആവിഷ്കൃതമായതിനുശേഷമാണ് ഇലക്ട്രോണ് കണ്ടുപിടിക്കപ്പെട്ടത് (1897). തുടർന്ന് 20-ാം ശതകത്തിൽ ആറ്റത്തിനെപ്പറ്റിയും അയോണുകളെപ്പറ്റിയും സംരചനാപരമായി അറിവ് ലഭിച്ചു. വൈദ്യുതിധാര ഇലക്ട്രോണുകളുടെ പ്രവാഹം മാത്രമാണെന്നും വ്യക്തമാക്കുകയും ചെയ്തു.
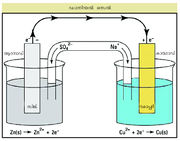
സെല്ലുകള്. രാസമാറ്റങ്ങളിലൂടെ വൈദ്യുതോർജം ഉത്പാദിപ്പിക്കുന്ന വിദ്യുത്-രാസ സെല്ലുകളുടെ വിദ്യുത്ചാലകബലം [electro motive force (emf)] അളന്ന് അവയിലെ രാസമാറ്റത്തെപ്പറ്റിയുള്ള പല സംഗതികളും കണക്കാക്കാവുന്നതാണ്. ഒരു ഇലക്ട്രോഡും അതിനനുയോജ്യമായ ഒരു ഇലക്ട്രോളൈറ്റും ചേർന്ന രണ്ട് അർധസെല്ലുകളുടെ സംഗമമാണ് ഒരു ഗാൽവനിക് സെൽ. ഓരോ ഇലക്ട്രോഡിനും അതാതിന്റേതായ വൈദ്യുത-പൊട്ടന്ഷ്യൽ ഉണ്ടായിരിക്കും. ഒന്നിന് ഓക്സീകരണ പൊട്ടന്ഷ്യലും മറ്റേതിന് നിരോക്സീകരണ പൊട്ടന്ഷ്യലുമാണുണ്ടാവുക. തന്മൂലം ഇലക്ട്രോഡുകള് തമ്മിൽ പൊട്ടന്ഷ്യൽ വ്യത്യാസമുണ്ടാകും. ഇതാണ് സെൽ പൊട്ടന്ഷ്യൽ. ഉയർന്ന പൊട്ടന്ഷ്യലുള്ള ഇലക്ട്രോഡിൽനിന്ന് മറ്റേതിലേക്ക് വൈദ്യുതിധാരയുണ്ടാകും; അതായത് പൊട്ടന്ഷ്യൽ കുറഞ്ഞ ഇലക്ട്രോഡിൽ നിന്ന് കൂടിയ ഇലക്ട്രോഡിലേക്ക് ഇലക്ട്രോണ് പ്രവാഹമുണ്ടാകും. ഡാനിയൽ സെൽ ഒരു ഉത്തമോദാഹരണമാണ്. ഒരു കോപ്പർദണ്ഡ് കോപ്പർ സള്ഫേറ്റ് ലായനിയിലും സിങ്കുദണ്ഡ് സിങ്ക് സള്ഫേറ്റ് ലായനിയിലും ഇറക്കിവയ്ക്കുന്നു. ഇവയാണ് രണ്ട് ഇലക്ട്രോഡുകള്. ഇവയെ രണ്ടും ബാഹ്യമായി ഒരു ലോഹക്കമ്പികൊണ്ട് വോള്ട്ട് മീറ്ററിലേക്ക് ഘടിപ്പിച്ചിരിക്കുന്നു. ഈ ഇലക്ട്രോഡുകള് രണ്ടുംകൂടി വിപരീതമായി തൊടുക്കുമ്പോള് ഡാനിയൽ സെൽ കിട്ടുന്നു. അഗർ-അഗർ ചൂർണം ജലത്തിൽ കലർത്തി പൊട്ടാസ്യം ക്ലോറൈഡ്, പൊട്ടാസ്യം സള്ഫേറ്റ്, അമോണിയം നൈട്രറ്റ് മുതലായവയിൽ ഏതെങ്കിലും ഒരു ഇലക്ട്രോളൈറ്റ് ചേർത്തു തിളപ്പിച്ചുകിട്ടുന്ന തെളിഞ്ഞ ലായനി ചൂടോടെ ഒരു ഡ കുഴലിൽ ഒഴിച്ച് തണുപ്പിക്കുമ്പോള് ലായനി ഉറച്ച് ഹൽവാ പോലുള്ള ദൃഢമായ ഒരു അർധഖര-ജെൽ ലഭിക്കുന്നതാണ്. കുഴൽ കമഴ്ത്തി ഓരോ അഗ്രവും ഓരോ ലായനിയിൽ മുക്കി നിർത്തുക. സെൽ പരിപഥത്തിൽ (cell circuit)ഒരു ഗാൽവനോമീറ്റർ കൂടി ഘടിപ്പിച്ചാൽ വൈദ്യുതിധാര ദൃശ്യമാകും. ഇവിടെ കോപ്പർ ധന-ഇലക്ട്രോഡും സിങ്ക് ഋണ-ഇലക്ട്രോഡും ആയിരിക്കും. സിങ്ക് ഇലക്ട്രോഡിൽ ഇലക്ട്രോണ്-ഉത്പാദനവും (ഓക്സീകരണം) കോപ്പർ ഇലക്ട്രോഡിൽ ഇലക്ട്രോണ്-ഉപഭോഗവും (നിരോക്സീകരണം) നടക്കുന്നു. അതിനാൽ ബാഹ്യപഥത്തിൽക്കൂടി ഇലക്ട്രോണുകള് സിങ്കിൽ നിന്നു കോപ്പറിലേക്കും പ്രവഹിക്കുന്നു.
കോപ്പറിനെ അപേക്ഷിച്ച് സിങ്കിന് ഓക്സീകരണശേഷി കൂടുതലാകയാലാണ് പ്രസ്തുത ഡാനിയൽ സെല്ലിൽ സിങ്ക് ഋണ-ഇലക്ട്രോഡും കോപ്പർ ധന-ഇലക്ട്രോഡും ആയത്. എന്നാൽ സിൽവർ-സിൽവർനൈട്രറ്റ്-ഇലക്ട്രോഡും കോപ്പർ-കോപ്പർ സള്ഫേറ്റ്-ഇലക്ട്രോഡും തമ്മിൽ തൊടുക്കുമ്പോള് കോപ്പർ ആണ് ഋണ-ഇലക്ട്രോഡ് ആയിത്തീരുന്നത്. ഡാനിയൽ സെല്ലിനെ ഇങ്ങനെ ചിത്രീകരിക്കാം.
ഇടയ്ക്കുള്ള ഇരട്ടവര ജെൽ-ബന്ധമാണ്. രാസപ്രക്രിയകളെ ആസ്പദമാക്കി ഡാനിയൽ സെല്ലിനു പുറമേ വേറെയും അനേകം സെല്ലുകള് സംവിധാനം ചെയ്യപ്പെട്ടിട്ടുണ്ട്. ആവശ്യങ്ങള്ക്കനുയോജ്യമായി വിവിധയിനം ഇലക്ട്രോഡുകളും നിർമിക്കപ്പെട്ടിട്ടുണ്ട്. ഇലക്ട്രോകെമിസ്ട്രിയുടെ വികാസഫലമായി സ്റ്റോറേജ് സെല്ലുകളും പല വിധത്തിൽ നിർമിക്കപ്പെട്ടു.
പ്രയോജനം. ഇലക്ട്രോകെമിസ്ട്രിയുടെ വികാസം ഒരു പരിധിവരെ ഇലക്ട്രോകെമിക്കൽ വ്യവസായങ്ങളുടെ പ്രതിഷ്ഠയ്ക്കു കാരണമായിത്തീർന്നു. അലുമിനിയം, മഗ്നീഷ്യം, സോഡിയം, സിങ്ക്, നിക്കൽ തുടങ്ങിയ ലോഹമൂലകങ്ങളെ അവയുടെ അയിരുകളിൽ നിഷ്കർഷണം ചെയ്യുന്നതിന് വൈദ്യുതവിശ്ലേഷണ പ്രക്രിയയാണ് സ്വീകരിക്കപ്പെട്ടിരിക്കുന്നത്. സ്വർണം, വെള്ളി, ചെമ്പ്, കാരീയം, വെളുത്തീയം (tin)മുതലായ ലോഹങ്ങളെ ശുദ്ധീകരിക്കുന്നതും ഈ പ്രക്രിയവഴിയാണ്. പലതരം ലോഹങ്ങളും സങ്കരലോഹങ്ങളുംകൊണ്ട് വിദ്യുല്ലേപനം (electroplating) നടത്തുന്നതിനും കാസ്റ്റിക് സോഡ, ഹൈപ്പോക്ലോറൈറ്റുകള്, ക്ലോറേറ്റുകള്, ഹൈഡ്രജന്, ഓക്സിജന് എന്നിങ്ങനെയുള്ള രാസവസ്തുക്കള് വന്തോതിൽ ഉത്പാദിപ്പിക്കുന്നതിനും വൈദ്യുതവിശ്ലേഷണത്തിന്റെ തത്ത്വംതന്നെയാണ് പ്രാവർത്തികമാക്കുന്നത്. ലോഹ-അയിരുകളുടെ പ്രഗളനം (smelting), ഫെറോ-അലോയ്കളുടെ നിർമാണം, ഉരുക്കു ശുദ്ധീകരണം, കാത്സ്യം കാർബൈഡ്, കാർബൊറണ്ടം, ഫോസ്ഫറസ് എന്നിവയുടെ ഉത്പാദനം മുതലായ വ്യവസായങ്ങളിൽ ഇലക്ട്രോ തെർമൽ-കെമിക്കൽ പ്രക്രിയകളാണ് പ്രയോഗിക്കപ്പെടുന്നത്. വൈദ്യുതപ്രവാഹംമൂലമുളവാകുന്ന രാസപ്രവർത്തനങ്ങളിൽ വളരെ പ്രമുഖമായ ഒന്നാണ് ഇലക്ട്രോഡെപ്പോസിഷന്. നിക്ഷേപിക്കേണ്ട ലോഹത്തിന്റെ ലായനി ഇലക്ട്രോലൈറ്റായി എടുക്കുന്നു. വൈദ്യുത രാസപ്രവർത്തനത്തിലൂടെ ഇലക്ട്രോലൈറ്റിൽനിന്നും ലോഹ അയോണുകള് കാഥോഡിൽ നിക്ഷേപിക്കപ്പെടുന്നു. പലരീതിയിൽ ഇലക്ട്രോഡെപ്പോസിഷനെ പ്രയോജനപ്പെടുത്താവുന്നതാണ്. ഇലക്ട്രോപ്ലേറ്റിങ് ഒരുദാഹരണമാണ്. സിൽവർ, കാഡ്മിയം, നിക്കൽ, ക്രാമിയം തുടങ്ങിയ ലോഹങ്ങളെല്ലാം മറ്റു ലോഹങ്ങളിൽ സംരക്ഷണാർഥമോ സൗന്ദര്യാർഥമോ പ്ലേറ്റിങ് ചെയ്യാറുണ്ട്. മറ്റൊരു ഇലക്ട്രോഡെപ്പോസിഷന് പ്രക്രിയയായ ഇലക്ട്രോറിഫൈനിങ് വെള്ളി, ചെമ്പ്, ലെഡ് പോലുള്ള ലോഹങ്ങളുടെ ശുദ്ധീകരണ പ്രക്രിയയായി ഉപയോഗിക്കുന്നു. ഇവിടെ ശുദ്ധീകരിക്കേണ്ട ലോഹത്തിന്റെ തകിട് ആനോഡായി ഉപയോഗിക്കുന്നു. വൈദ്യുതവിശ്ലേഷണത്തിലൂടെ ശുദ്ധമായ ലോഹം കാഥോഡിൽ നിക്ഷേപിക്കപ്പെടുന്നു. ഇലക്ട്രോഡെപ്പോസിഷന് പ്രക്രിയ ക്രിയാശീലം ഉയർന്ന മൂലകങ്ങളായ അലുമിനിയം, മഗ്നീഷ്യം, സോഡിയം എന്നിവയെ അവയുടെ ഉരുകിയ ലായനിയിൽനിന്നും കോപ്പർ, മാങ്നീസ്, ആന്റിമണി എന്നിവയെ അവയുടെ ജലീയലായനിയിൽനിന്നും നിർമിക്കുവാന് ഉപയുക്തമാണ്.
സംരക്ഷിക്കേണ്ട ലോഹത്തെ പെയിന്റടിച്ചോ, എണ്ണ, ഗ്രീസ് എന്നിവ പുരട്ടിയോ, സിങ്ക്, ക്രാമിയം, നിക്കൽ, അലുമിനിയം തുടങ്ങിയ ക്രിയാശീലമൂലകങ്ങളുപയോഗിച്ച് ഇലക്ട്രോപ്ലേറ്റിങ് നടത്തിയോ സംക്ഷാരണത്തിൽനിന്നും രക്ഷിക്കാം. വായുവിൽ നിന്ന് നൈട്രിക് ഓക്സൈഡിന്റെ ഉദ്ഗ്രഥനം, ഓസോണിന്റെ ഉത്പാദനം എന്നിവ സാധിപ്പിക്കുന്നതിന് വാതകങ്ങളിലൂടെ വൈദ്യുതി പ്രവഹിപ്പിക്കുന്നു. ഇലക്ട്രോകെമിസ്ട്രിയിലെ ഗവേഷണപുരോഗതിമൂലമാണ് ലോഹങ്ങള്ക്ക് നൈസർഗികമായി വരുന്ന ക്ഷാരണത്തെപ്പറ്റി പഠിക്കാനും അതു ഫലപ്രദമാംവണ്ണം തടയുന്നതിനുള്ള മാർഗങ്ങള് ആസൂത്രണം ചെയ്യുവാനും സാധിച്ചിട്ടുള്ളത്. അനുനിമിഷം ലോകമെമ്പാടും ക്ഷാരണവിധേയമായിക്കൊണ്ടിരിക്കുന്ന ലോഹസമ്പത്തിന്റെ പരിമാണം വളരെ ഭീമമാണ്. ഈ വന്നഷ്ടം ഒഴിവാക്കുന്നതിന് പറ്റിയ മാർഗം ക്ഷാരണത്തിനാസ്പദമായ വിദ്യുത്-രാസ പ്രക്രിയയെ വിദ്യുത്-രാസപരമായിത്തന്നെ തടുത്തുനിർത്തുക എന്നതാണ്.
പലതരം ഇലക്ട്രോഡുകളുപയോഗിച്ച് അനേകം വിശ്ലേഷണ (analytical) വിധികള് ഇന്ന് പരീക്ഷണശാലകളിൽ പ്രയോജനപ്പെടുത്തുന്നുണ്ട്. പൊട്ടന്ഷ്യോമെട്രി, വോള്ട്ടാമെട്രി, കൂളോമെട്രി, ഇലക്ട്രോഗ്രാവിമെട്രി, പോളാരൊഗ്രാഫി എന്നിവ ചില ഉദാഹരണങ്ങളാണ്. നോ. ഇലക്ട്രിക് ഫർണസ്; ഇലക്ട്രോഡ്; ഇലക്ട്രോപ്ളേറ്റിങ്; വൈദ്യുതി
(ഡോ. കെ.പി. ധർമരാജയ്യർ; ഡോ. വി.എസ്. പ്രസാദ്)