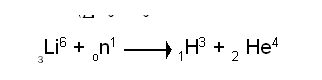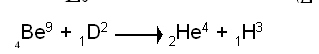This site is not complete. The work to converting the volumes of സര്വ്വവിജ്ഞാനകോശം is on progress. Please bear with us
Please contact webmastersiep@yahoo.com for any queries regarding this website.
Reading Problems? see Enabling Malayalam
ട്രിഷിയം
സര്വ്വവിജ്ഞാനകോശം സംരംഭത്തില് നിന്ന്
ട്രിഷിയം
Tritium
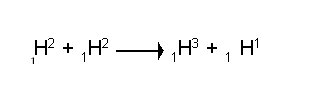
ഹൈഡ്രജന്റെ രാദശക്തിയുള്ള ഒരു സമസ്ഥാനീയം. സിം: 1H3 അഥവാ T. അ. സ. 1, അ. ഭാ. 3. ഏണസ്റ്റ് റൂഥര്ഫോര്ഡ് (Ernst Rutherford), മാര്ക്വൂസ് എല്. ഇ. ഒളിഫാന്റ് (Marcques L.E.Olefant), പോള് ഹാര്ടെക്ക് (Paul Hartek) എന്നീ ശാസ്ത്രജ്ഞരാണ് ഡ്യൂട്ടീരിയ (ഹൈഡ്രജന്റെ മറ്റൊരു സമസ്ഥാനീയം 1H2) ത്തിന്റെ അണുകേന്ദ്രീയ മൂലകാന്തരണം (nuclear transmutation) വഴി ട്രിഷിയം വേര്തിരിച്ചത് (1934).
അന്തരീക്ഷത്തിന്റെ മുകള് ഭാഗത്തുവച്ച് കോസ്മിക് രശ്മികളില്നിന്ന് ഉത്ഭവിക്കുന്ന ന്യൂട്രോണുകളും പ്രോട്ടോണുകളുമായി നൈട്രജന് അണുക്കള് കൂട്ടിമുട്ടിയാണ് ട്രിഷിയം ഉദ്ഭവിക്കുന്നത്.
7N14+9n1→1H3+6C12
പ്രകൃതിയില് ട്രിഷിയത്തിന്റെ അളവ് വളരെ കുറവാണ്. താപീയ അണുകേന്ദ്ര ആയുധങ്ങള് (thermo nuclear weapons) പ്രയോഗത്തില് വരുന്നതിനു മുമ്പ് (1954) 1018 ഹൈഡ്രജന് അണുക്കള്ക്ക് 1-10 അണുക്കള് എന്ന തോതിലാണ് അന്തരീക്ഷത്തില് ട്രിഷിയം ഉള്ക്കൊണ്ടിരുന്നത്. എന്നാല് താപീയ അണു കേന്ദ്രീയ ആയുധങ്ങളുടെ ആവിര്ഭാവത്തോടെ, അന്തരീക്ഷത്തിലെ ട്രിഷിയത്തിന്റെ അളവ് 1018 ഹൈഡ്രജന് അണുക്കള്ക്ക് 500 ട്രിഷിയം അണുക്കള് എന്ന തോതില് വര്ധിച്ചിട്ടുണ്ട്. ഡ്യൂട്ടീരിയം സംയുക്തങ്ങളെ ഉയര്ന്ന ഊര്ജ ഡ്യൂട്ടറോണുകള് ഉപയോഗിച്ചു ഭേദിച്ചാണ് കൃത്രിമ ട്രിഷിയം ആദ്യമായി ഉത്പാദിപ്പിച്ചത്.
അണുകേന്ദ്ര റിയാക്ടറുകളില് Li6 അണുക്കള്, വേഗത കുറഞ്ഞ ന്യൂട്രോണുകളെ ആഗിരണം ചെയ്യുന്നതുവഴിയും ട്രിഷിയം ഉത്പാദിപ്പിക്കപ്പെടുന്നു.
സൈക്ലോട്രോണുകളില് വച്ച് ബെറിലിയം അണുക്കളെ ഡ്യൂട്ടറോണുകള് കൊണ്ടു ഭേദിച്ചും ട്രിഷിയം ഉത്പാദിപ്പിക്കാം.
ട്രിഷിയത്തിന്റെ ഭൗതിക ഗുണധര്മങ്ങള് ഹൈഡ്രജനില്നിന്നു വളരെ വ്യത്യസ്തമാണ്.
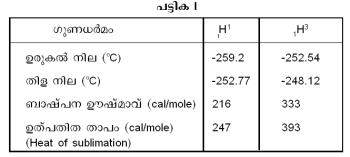
ഹൈഡ്രജനും ട്രിഷിയവും രാസപരമായി സമാനങ്ങളാണെങ്കിലും ട്രിഷിയത്തിന്റെ പ്രതിക്രിയാ നിരക്ക് ഹൈഡ്രജനെ അപേക്ഷിച്ച് വളരെ കുറവാണ് (64:1). ട്രിഷിയത്തിന്റെ ഉയര്ന്ന അണുഭാരമാണിതിന് കാരണം. ട്രിഷിയത്തിന്റെ അണുകേന്ദ്രമായ ട്രിറ്റണ് (triton) ഒരു പ്രോട്ടോണും രണ്ടു ന്യൂട്രോണും അടങ്ങുന്നതാണ്. രാദശക്തിയുള്ള ട്രിഷിയം അണുക്കള് β രശ്മികള് പുറത്തേക്ക് അയച്ച് He3 അണുക്കളുണ്ടാക്കുന്നു. ഈ പ്രക്രിയയുടെ അര്ധായുസ്സ് (T<sub1/2</sub>) 12.26 വര്ഷമാണ്. ഡ്യൂട്രോണുകള് ഉപയോഗിച്ച് ട്രിഷിയത്തിനെ ഭേദിക്കുമ്പോള് ന്യൂക്ലിയര് ഫ്യൂഷന് വഴി ഹീലിയം ഉണ്ടാവുന്നു. ഈ പ്രക്രിയയില് ഊര്ജം പുറത്തേക്ക് വരും.
താപീയ അണുകേന്ദ്ര ബോംബുകളില് ഉപയോഗിച്ചു വരുന്നത് ഈ പ്രതിക്രിയയാണ്. അണ്വായുധങ്ങളില് വളരെയേറെ ഉപയോഗക്ഷമമായതിനാലാണ് ട്രിഷിയം കൂടിയ തോതില് ഉത്പാദിപ്പിക്കപ്പെട്ടുവരുന്നത്. തിളങ്ങുന്ന ചായ (luminious paint) ങ്ങളില് ZnS ട്രിഷിയം മിശ്രിതമാണ് ഉപയോഗിക്കുന്നത്. വാച്ചിന്റെ ഡയലില് ഉപയോഗിച്ചിരുന്ന റേഡിയത്തിനു പകരമായി ഈ ചായം ഇന്നു വ്യാപകമായി ഉപയോഗിച്ചുവരുന്നു. വേഗതയേറിയ ന്യൂട്രോണുകള് ഉണ്ടാക്കുന്നതിനുള്ള ലക്ഷ്യസ്ഥാനമായി ട്രിഷിയം അവശോഷണം ചെയ്ത ലോഹങ്ങളാണ് ഉപയോഗിക്കുന്നത്. ജലത്തിന്റെ സാന്നിധ്യം കുപിടിക്കാന് ഏറ്റവും അനുയോജ്യമായ ട്രേസര് ആണ് ട്രിഷിയം. പല രാസപ്രവര്ത്തനങ്ങളിലും ഹൈഡ്രജന്റെ ട്രേസറായും ട്രിഷിയം ഉപയോഗിച്ചുവരുന്നു.
വളരെ കുറച്ചു ട്രിഷിയം സംയുക്തങ്ങള് മാത്രമേ നിര്മിക്കുവാനും പഠനവിധേയമാക്കുവാനും സാധിച്ചിട്ടുള്ളു. ട്രിഷിയം സംയുക്തങ്ങള് β രശ്മികള് വികിരണം ചെയ്ത് വളരെവേഗം വിയോജിക്കുന്നതാണ് കാരണം. ചൂടാക്കിയ കോപ്പര് ഓക്സൈഡിന്റെ (CuO) സാന്നിധ്യത്തില് ഓക്സീകരിക്കുമ്പോള് T2O ഉണ്ടാവുന്നു. ഓക്സിജന് - ട്രിഷിയം മിശ്രിതത്തിലൂടെ ഒരു വൈദ്യുതി സ്ഫുലിംഗം കടത്തിവിട്ടും T2O ഉണ്ടാക്കാം. T2O ന്റെ ഉരുകല് നില 4.49°C ആണ്; സാധാരണ ജലത്തിന്റേത് 0° ഉം. കാര്ബണിക സംയുക്തങ്ങളില് ചില ഹൈഡ്രജന് അണുക്കളെ ട്രിഷിയംകൊണ്ട് പ്രതിസ്ഥാപിക്കാറുണ്ട്. ഇത്തരം സംയുക്തങ്ങള് (Tritium labelled) ട്രേസര് പഠനങ്ങളില് വളരെ പ്രാധാന്യമര്ഹിക്കുന്നവയാണ്. രാസത്വരകമായ പ്ലാറ്റിനത്തിന്റേയോ ഗാഢ അമ്ലത്തിന്റേയോ സാന്നിധ്യത്തില് കാര്ബണിക സംയുക്തങ്ങളിലേക്ക് വളരെ നേരിയ അളവില് ട്രിഷിയം ചേര്ക്കുമ്പോള് H-T വിനിമയം നടക്കുന്നു.