This site is not complete. The work to converting the volumes of സര്വ്വവിജ്ഞാനകോശം is on progress. Please bear with us
Please contact webmastersiep@yahoo.com for any queries regarding this website.
Reading Problems? see Enabling Malayalam
ഈനോള്
സര്വ്വവിജ്ഞാനകോശം സംരംഭത്തില് നിന്ന്
Mksol (സംവാദം | സംഭാവനകള്) (പുതിയ താള്: == ഈനോള് == == Enol == കീറ്റോണിക (CO) ഗ്രൂപ്പുള്ള ചില കാർബണിക യൗഗികങ്ങള...) |
Mksol (സംവാദം | സംഭാവനകള്) (→Enol) |
||
| (ഇടക്കുള്ള 2 പതിപ്പുകളിലെ മാറ്റങ്ങള് ഇവിടെ കാണിക്കുന്നില്ല.) | |||
| വരി 3: | വരി 3: | ||
== Enol == | == Enol == | ||
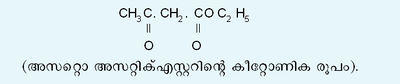
| - | കീറ്റോണിക (CO) ഗ്രൂപ്പുള്ള ചില | + | കീറ്റോണിക (CO) ഗ്രൂപ്പുള്ള ചില കാര്ബണിക യൗഗികങ്ങള് ചലാവയവത(tautomerism)യൊ്ക്കു വിധേയമാകുന്നതിന്റെ ഫലമായി ഉണ്ടാകുന്ന ആല്ക്കഹോളിക ഗ്രൂപ്പോടു കൂടിയ യൗഗികങ്ങളാണ് ഈനോള് വിഭാഗത്തില്പ്പെടുന്നത്. ആല്കീന് (alkene), ആല്ക്കഹോള് (alcohol) എന്നീ പദങ്ങളിലെ അന്ത്യഭാഗങ്ങള് യോജിപ്പിച്ചുണ്ടാക്കിയ ഈനോള് (enol) എന്ന പദം ഒരു ദ്വിബന്ധവും (double bond) ഒരു ആല്ക്കഹോളിക് ഗ്രൂപ്പും ഉള്ള പ്രത്യേക വിഭാഗം ഓര്ഗാനിക് യൗഗികങ്ങളെ വിവക്ഷിക്കുന്നു. ഈ പദത്തിനെ അപൂരിത-ആല്ക്കഹോള് എന്ന് അര്ഥമാക്കാം. അസറ്റൊ അസറ്റിക് എസ്റ്റര് എന്ന യൗഗികത്തിന്റെ ഗുണധര്മപഠനത്തില് നിന്നാണ് ഈ പ്രതിഭാസത്തെക്കുറിച്ച് ആദ്യമായി വിവരമുണ്ടായത്. പ്രസ്തുത യൗഗികം ഹൈഡ്രജന് സയനൈഡ്, ഹൈഡ്രാക്സില് അമീന്, ഫിനൈല് ഹൈഡ്രസീന് എന്നിവയുമായി പ്രതിപ്രവര്ത്തിച്ച് ക്രമത്തില് സയനൊഹൈഡ്രിന്, ഓക്സൈം, ഫിനൈല് ഹൈഡ്രസോണ് എന്നീ യൗഗികങ്ങള് ലഭ്യമാക്കുന്നതിനാല് അത് ഒരു കീറ്റോണിക യൗഗികമാണെന്നു തെളിയുന്നുണ്ട്. അതനുസരിച്ച് അതിന്റെ ഫോര്മുല ഇപ്രകാരമാണ്: |
| - | + | ||
| - | + | ||
| - | + | ||
| - | + | [[ചിത്രം:Vol4_502_1.jpg|400px]] | |
| - | + | ||
| - | + | ||
| - | + | ||
| - | + | ||
| - | + | ||
| - | + | ||
| - | + | ||
| - | + | ||
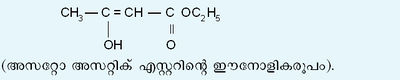
| - | + | എന്നാല് ഈ എസ്റ്റര് സോഡിയവുമായി പ്രവര്ത്തിച്ച് ഹൈഡ്രജന് ഉത്പാദിപ്പിക്കുകയും ഫെറിക് ക്ലോറൈഡുമായി പ്രവര്ത്തിച്ചു ചുവപ്പുനിറം തരികയും ബ്രാമിന് എന്ന ഹാലജനെ അനായാസമായി ആഗിരണം ചെയ്യുകയും അങ്ങനെ ഒരു അപൂരിത ആല്ക്കഹോളിക യൗഗികമായി പെരുമാറുകയും ചെയ്യുന്നു. ഇതനുസരിച്ച് അതിന്റെ ഫോര്മുല താഴെ ചേര്ത്തിരിക്കുന്നു: | |
| - | + | ||
| - | + | ||
| - | + | ||
| - | + | [[ചിത്രം:Vol4_502_2.jpg|400px]] | |
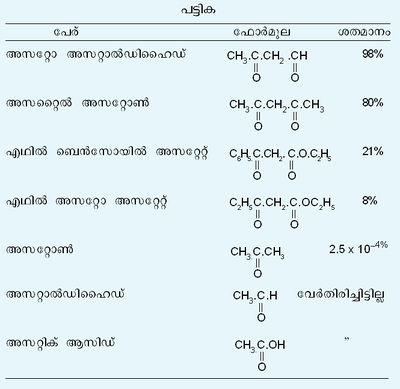
| - | + | രണ്ടു കാര്ബൊണൈല് ഗ്രൂപ്പുകളുടെ മധ്യത്തിലുള്ള കാര്ബണ് ആറ്റത്തിലെ രണ്ടു ഹൈഡ്രജനില്നിന്ന് ഒന്ന് ഒരു കാര്ബൊണൈല് ഗ്രൂപ്പിലെ ഓക്സിജനുമായി ചേര്ന്ന് OH ഗ്രൂപ്പ് ഉണ്ടാവുകയും അതേ സമയം OH ഗ്രൂപ്പുള്ള കാര്ബണ് ആറ്റത്തിനും ഹൈഡ്രജന് നഷ്ടപ്പെട്ട കാര്ബണ് ആറ്റത്തിനുമിടയ്ക്ക് ഒരു ദ്വിബന്ധമുണ്ടാവുകയുമാണ് ഈനോള് രൂപീകരണത്തിന്റെ പിന്നിലെ പ്രക്രിയ. സൂക്ഷ്മമായ പരീക്ഷണങ്ങളും പഠനങ്ങളും തുടര്ന്നതിന്റെ ഫലമായി സാധാരണ താപനിലകളില് അസറ്റൊ അസറ്റിക് എസ്റ്റര് കീറ്റോ രൂപത്തിന്റെയും ഈനോള് രൂപത്തിന്റെയും ഒരു സന്തുലിത മിശ്രിതമാണ് എന്നു തെളിഞ്ഞിട്ടുണ്ട്. ചില കാര്ബൊണൈല് യൗഗികങ്ങളും അവയുടെ ഫോര്മുലകളും അവയില് സാധാരണ പരിതഃസ്ഥിതിയില് കണ്ടുവരുന്ന ഈനോളിക രൂപത്തിന്റെ ശതമാനവും താഴെ ഒരു പട്ടികയായി കൊടുത്തരിക്കുന്നു: | |
| - | + | [[ചിത്രം:Vol4_502_3.jpg|400px]] | |
| - | + | ഡൈ കാര്ബൊണൈല് യൗഗികങ്ങളുടെ ഈനോളിക രൂപങ്ങള്ക്ക് മോണോ കാര്ബൊണൈല് യൗഗികങ്ങളുടെ ഈനോളിക രൂപങ്ങളെ അപേക്ഷിച്ചു കൂടുതല് സ്ഥിരതയുള്ളതായിക്കാണുന്നു. കാര്ബണ്-കാര്ബണ് ദ്വിബന്ധവും ഈനോളിലെ ആല്ക്കഹോളിക ഹൈഡ്രജനും രണ്ടാമത്തെ കാര്ബൊണൈല് ഗ്രൂപ്പും തമ്മിലുണ്ടാകുന്ന ചീലേഷന് (chelation) ബന്ധവും ആയിരിക്കണം ഇതിനു കാരണങ്ങളെന്നൂഹിക്കപ്പെടുന്നു. | |
| - | + | സാധാരണ കാര്ബൊണൈല് യൗഗികങ്ങള് ചലാവയവത നിമിത്തം കീറ്റോ-ഈനോള് സന്തുലിത മിശ്രിതമായിരിക്കും. എന്നാല് ഈ സന്തുലനത്തെ ലായകം, താപനില, സാന്ദ്രണം, രാസത്വരകങ്ങളുടെ സാന്നിധ്യം എന്നിങ്ങനെയുള്ള പല ഘടകങ്ങളും സ്വാധീനിക്കുന്നതാണ്. ഉദാഹരണമായി അസറ്റൊ അസറ്റിക് എസ്റ്ററിന്റെ ജലീയലായനിയില് ഈനോള് രൂപം 0.4 ശതമാനം ആണ്; ഹെക്സേന് ലായനിയില് 48 ശതമാനവും. അബ്സൊല്യൂട്ട് ആല്ക്കഹോള് കൊണ്ട് 65 ശതമാനം എസ്റ്റര്ലായനിയുണ്ടാക്കി പരിശോധിച്ചാല് ഈനോള് സു. 7.8 ശതമാനം ഉണ്ടായിരിക്കുമെങ്കില് 0.8 ശതമാനം ലായനിയില് 13 ശതമാനം ഉണ്ടായിരിക്കും. | |
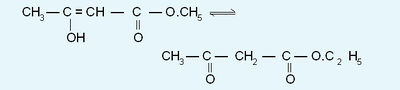
| - | അസറ്റിക് | + | അസറ്റൊ അസറ്റിക് എസ്റ്ററിന്റെ ഈനോള് രൂപം ശുദ്ധമായ നിലയില് ഉണ്ടാക്കുവാന് സാധിക്കും. ഖരസോഡിയോഅസറ്റിക് എസ്റ്റര് ഹെക്സേനില് നിലംബനം ചെയ്ത്, -78<sup>o</sup>C-ല് ശുദ്ധഹൈഡ്രജന് ക്ലോറൈഡ് വാതകം കുമിളകള് കടത്തിവിട്ട് ശുദ്ധമായ ഈനോള് ലഭ്യമാകുന്നതാണ്. -78<sup>o</sup>C-ല് ഇത് ദ്രവമാണ്. നിര്വാതത്തില് ഇത് 34<sup>o</sup>C-ല് തിളയ്ക്കും. രണ്ടാഴ്ചയ്ക്കുള്ളില് സാധാരണ താപനിലയില് ഇത് ചലാവയവതയ്ക്കു വിധേയമായി സന്തുലനത്തോടുകൂടിയ മിശ്രിതമായിത്തീരുകയും ചെയ്യും. |
| - | + | ||
| - | + | ||
| - | + | [[ചിത്രം:Vol4_503_1.jpg|400px]] | |
| - | + | ||
| - | + | ലുഡ്വിഗ് നോര് (1859-1921), കുര്ട് ഹന്സ് മേയര് (1883-1952) എന്നീ ശാസ്ത്രജ്ഞന്മാരുടെ പേരുകള് കീറ്റൊ-ഈനോള് ചലാവയവതയുടെ പഠനത്തില് പ്രത്യേകം പ്രസ്താവ്യമാണ്. ഓര്ഗാനിക് യൗഗികങ്ങളുടെ, വിശേഷിച്ചും കീറ്റോണിക യൗഗികങ്ങളുടെ, ഗുണധര്മപഠനം സമഗ്രമാകുന്നത് സംഗതങ്ങളായ ഈനോള് രൂപങ്ങളുടെ പഠനത്തോടുകൂടി മാത്രമാണ്. അടുത്ത കാലത്ത് ഈനോളുകളുടെ പഠനത്തിന് സൈദ്ധാന്തിക മേഖലയില് മാത്രമല്ല പ്രായോഗികരംഗത്തും പ്രാധാന്യം നേടിയിരിക്കുന്നു. | |
| - | + | ||
| - | + | ||
| - | + | ||
| - | + | ||
| - | + | ||
| - | ലുഡ്വിഗ് | + | |
Current revision as of 07:53, 11 സെപ്റ്റംബര് 2014
ഈനോള്
Enol
കീറ്റോണിക (CO) ഗ്രൂപ്പുള്ള ചില കാര്ബണിക യൗഗികങ്ങള് ചലാവയവത(tautomerism)യൊ്ക്കു വിധേയമാകുന്നതിന്റെ ഫലമായി ഉണ്ടാകുന്ന ആല്ക്കഹോളിക ഗ്രൂപ്പോടു കൂടിയ യൗഗികങ്ങളാണ് ഈനോള് വിഭാഗത്തില്പ്പെടുന്നത്. ആല്കീന് (alkene), ആല്ക്കഹോള് (alcohol) എന്നീ പദങ്ങളിലെ അന്ത്യഭാഗങ്ങള് യോജിപ്പിച്ചുണ്ടാക്കിയ ഈനോള് (enol) എന്ന പദം ഒരു ദ്വിബന്ധവും (double bond) ഒരു ആല്ക്കഹോളിക് ഗ്രൂപ്പും ഉള്ള പ്രത്യേക വിഭാഗം ഓര്ഗാനിക് യൗഗികങ്ങളെ വിവക്ഷിക്കുന്നു. ഈ പദത്തിനെ അപൂരിത-ആല്ക്കഹോള് എന്ന് അര്ഥമാക്കാം. അസറ്റൊ അസറ്റിക് എസ്റ്റര് എന്ന യൗഗികത്തിന്റെ ഗുണധര്മപഠനത്തില് നിന്നാണ് ഈ പ്രതിഭാസത്തെക്കുറിച്ച് ആദ്യമായി വിവരമുണ്ടായത്. പ്രസ്തുത യൗഗികം ഹൈഡ്രജന് സയനൈഡ്, ഹൈഡ്രാക്സില് അമീന്, ഫിനൈല് ഹൈഡ്രസീന് എന്നിവയുമായി പ്രതിപ്രവര്ത്തിച്ച് ക്രമത്തില് സയനൊഹൈഡ്രിന്, ഓക്സൈം, ഫിനൈല് ഹൈഡ്രസോണ് എന്നീ യൗഗികങ്ങള് ലഭ്യമാക്കുന്നതിനാല് അത് ഒരു കീറ്റോണിക യൗഗികമാണെന്നു തെളിയുന്നുണ്ട്. അതനുസരിച്ച് അതിന്റെ ഫോര്മുല ഇപ്രകാരമാണ്:
എന്നാല് ഈ എസ്റ്റര് സോഡിയവുമായി പ്രവര്ത്തിച്ച് ഹൈഡ്രജന് ഉത്പാദിപ്പിക്കുകയും ഫെറിക് ക്ലോറൈഡുമായി പ്രവര്ത്തിച്ചു ചുവപ്പുനിറം തരികയും ബ്രാമിന് എന്ന ഹാലജനെ അനായാസമായി ആഗിരണം ചെയ്യുകയും അങ്ങനെ ഒരു അപൂരിത ആല്ക്കഹോളിക യൗഗികമായി പെരുമാറുകയും ചെയ്യുന്നു. ഇതനുസരിച്ച് അതിന്റെ ഫോര്മുല താഴെ ചേര്ത്തിരിക്കുന്നു:
രണ്ടു കാര്ബൊണൈല് ഗ്രൂപ്പുകളുടെ മധ്യത്തിലുള്ള കാര്ബണ് ആറ്റത്തിലെ രണ്ടു ഹൈഡ്രജനില്നിന്ന് ഒന്ന് ഒരു കാര്ബൊണൈല് ഗ്രൂപ്പിലെ ഓക്സിജനുമായി ചേര്ന്ന് OH ഗ്രൂപ്പ് ഉണ്ടാവുകയും അതേ സമയം OH ഗ്രൂപ്പുള്ള കാര്ബണ് ആറ്റത്തിനും ഹൈഡ്രജന് നഷ്ടപ്പെട്ട കാര്ബണ് ആറ്റത്തിനുമിടയ്ക്ക് ഒരു ദ്വിബന്ധമുണ്ടാവുകയുമാണ് ഈനോള് രൂപീകരണത്തിന്റെ പിന്നിലെ പ്രക്രിയ. സൂക്ഷ്മമായ പരീക്ഷണങ്ങളും പഠനങ്ങളും തുടര്ന്നതിന്റെ ഫലമായി സാധാരണ താപനിലകളില് അസറ്റൊ അസറ്റിക് എസ്റ്റര് കീറ്റോ രൂപത്തിന്റെയും ഈനോള് രൂപത്തിന്റെയും ഒരു സന്തുലിത മിശ്രിതമാണ് എന്നു തെളിഞ്ഞിട്ടുണ്ട്. ചില കാര്ബൊണൈല് യൗഗികങ്ങളും അവയുടെ ഫോര്മുലകളും അവയില് സാധാരണ പരിതഃസ്ഥിതിയില് കണ്ടുവരുന്ന ഈനോളിക രൂപത്തിന്റെ ശതമാനവും താഴെ ഒരു പട്ടികയായി കൊടുത്തരിക്കുന്നു:
ഡൈ കാര്ബൊണൈല് യൗഗികങ്ങളുടെ ഈനോളിക രൂപങ്ങള്ക്ക് മോണോ കാര്ബൊണൈല് യൗഗികങ്ങളുടെ ഈനോളിക രൂപങ്ങളെ അപേക്ഷിച്ചു കൂടുതല് സ്ഥിരതയുള്ളതായിക്കാണുന്നു. കാര്ബണ്-കാര്ബണ് ദ്വിബന്ധവും ഈനോളിലെ ആല്ക്കഹോളിക ഹൈഡ്രജനും രണ്ടാമത്തെ കാര്ബൊണൈല് ഗ്രൂപ്പും തമ്മിലുണ്ടാകുന്ന ചീലേഷന് (chelation) ബന്ധവും ആയിരിക്കണം ഇതിനു കാരണങ്ങളെന്നൂഹിക്കപ്പെടുന്നു.
സാധാരണ കാര്ബൊണൈല് യൗഗികങ്ങള് ചലാവയവത നിമിത്തം കീറ്റോ-ഈനോള് സന്തുലിത മിശ്രിതമായിരിക്കും. എന്നാല് ഈ സന്തുലനത്തെ ലായകം, താപനില, സാന്ദ്രണം, രാസത്വരകങ്ങളുടെ സാന്നിധ്യം എന്നിങ്ങനെയുള്ള പല ഘടകങ്ങളും സ്വാധീനിക്കുന്നതാണ്. ഉദാഹരണമായി അസറ്റൊ അസറ്റിക് എസ്റ്ററിന്റെ ജലീയലായനിയില് ഈനോള് രൂപം 0.4 ശതമാനം ആണ്; ഹെക്സേന് ലായനിയില് 48 ശതമാനവും. അബ്സൊല്യൂട്ട് ആല്ക്കഹോള് കൊണ്ട് 65 ശതമാനം എസ്റ്റര്ലായനിയുണ്ടാക്കി പരിശോധിച്ചാല് ഈനോള് സു. 7.8 ശതമാനം ഉണ്ടായിരിക്കുമെങ്കില് 0.8 ശതമാനം ലായനിയില് 13 ശതമാനം ഉണ്ടായിരിക്കും.
അസറ്റൊ അസറ്റിക് എസ്റ്ററിന്റെ ഈനോള് രൂപം ശുദ്ധമായ നിലയില് ഉണ്ടാക്കുവാന് സാധിക്കും. ഖരസോഡിയോഅസറ്റിക് എസ്റ്റര് ഹെക്സേനില് നിലംബനം ചെയ്ത്, -78oC-ല് ശുദ്ധഹൈഡ്രജന് ക്ലോറൈഡ് വാതകം കുമിളകള് കടത്തിവിട്ട് ശുദ്ധമായ ഈനോള് ലഭ്യമാകുന്നതാണ്. -78oC-ല് ഇത് ദ്രവമാണ്. നിര്വാതത്തില് ഇത് 34oC-ല് തിളയ്ക്കും. രണ്ടാഴ്ചയ്ക്കുള്ളില് സാധാരണ താപനിലയില് ഇത് ചലാവയവതയ്ക്കു വിധേയമായി സന്തുലനത്തോടുകൂടിയ മിശ്രിതമായിത്തീരുകയും ചെയ്യും.
ലുഡ്വിഗ് നോര് (1859-1921), കുര്ട് ഹന്സ് മേയര് (1883-1952) എന്നീ ശാസ്ത്രജ്ഞന്മാരുടെ പേരുകള് കീറ്റൊ-ഈനോള് ചലാവയവതയുടെ പഠനത്തില് പ്രത്യേകം പ്രസ്താവ്യമാണ്. ഓര്ഗാനിക് യൗഗികങ്ങളുടെ, വിശേഷിച്ചും കീറ്റോണിക യൗഗികങ്ങളുടെ, ഗുണധര്മപഠനം സമഗ്രമാകുന്നത് സംഗതങ്ങളായ ഈനോള് രൂപങ്ങളുടെ പഠനത്തോടുകൂടി മാത്രമാണ്. അടുത്ത കാലത്ത് ഈനോളുകളുടെ പഠനത്തിന് സൈദ്ധാന്തിക മേഖലയില് മാത്രമല്ല പ്രായോഗികരംഗത്തും പ്രാധാന്യം നേടിയിരിക്കുന്നു.