This site is not complete. The work to converting the volumes of സര്വ്വവിജ്ഞാനകോശം is on progress. Please bear with us
Please contact webmastersiep@yahoo.com for any queries regarding this website.
Reading Problems? see Enabling Malayalam
കാര്ബോക്സിലിക് അമ്ലങ്ങള്
സര്വ്വവിജ്ഞാനകോശം സംരംഭത്തില് നിന്ന്
ഉള്ളടക്കം |
കാര്ബോക്സിലിക് അമ്ലങ്ങള്
Carboxylic acids
ഒന്നോ അതിലധികമോ കാര്ബോക്സില് ഗ്രൂപ്പുകള് (-COOH) അടങ്ങിയിട്ടുള്ള കാര്ബണിക സംയുക്തങ്ങള്. ഉദാ. അസറ്റിക് അമ്ലം (CH3 COOH), ഥാലിക് അമ്ലം C6H4 (COOH)2. ജൈവരസതന്ത്രത്തിലെ പ്രധാന അമ്ലങ്ങള് എല്ലാംതന്നെ കാര്ബോക്സിലിക് അമ്ലങ്ങളാണ്.
കാര്ബൊണില് ഗ്രൂപ്പ് (C = O) + ഹൈഡ്രാക്സില് ഗ്രൂപ്പ് (-OH) = കാര്ബോക്സില് ഗ്രൂപ്പ് (-COOH).
കാര്ബോക്സിലിക് അമ്ലത്തിനെ ഏറ്റവും ലളിതമായി R(C X Y)n COOH എന്ന പൊതുസൂത്രത്തില് സൂചിപ്പിക്കാം. ഇതില് R, X, Y എന്നിവ ഹൈഡ്രജനോ, പൂരിതമോ അപൂരിതമോ ആയ ഗ്രൂപ്പുകളോ, ആലിഫാറ്റികമോ ആരോമാറ്റികമോ ആയ ഗ്രൂപ്പുകളോ, ഹാലജനുകളോ മറ്റ് ഏതെങ്കിലും ഘടകങ്ങളോ ആവാം.n ന്റെ മൂല്യം പൂജ്യം മുതല് (ഉദാ. ഫോര്മിക് അമ്ലം -HCOOH) നൂറിലധികംവരെ ആകാം.
വര്ഗീകരണം
ഒരു തന്മാത്രയില് അടങ്ങിയിരിക്കുന്ന കാര്ബോക്സില് ഗ്രൂപ്പുകളുടെ എണ്ണത്തെ അടിസ്ഥാനമാക്കിയാണ് കാര്ബോക്സിലിക് അമ്ലങ്ങളെ സാധാരണയായി വര്ഗീകരിക്കുന്നത്. ഒരു കാര്ബോക്സില് ഗ്രൂപ്പ് മാത്രമുള്ളവയെ മോണോ കാര്ബോക്സിലിക് അമ്ലം എന്നും രണ്ടെണ്ണം ഉള്ളവയെ ഡൈകാര്ബോക്സിലിക് അമ്ലം എന്നും പറയുന്നു. ഇതേ ക്രമത്തില് അമ്ലങ്ങളെ ട്ര, ടെട്രാ, പെന്റാ എന്നിങ്ങനെ വിശേഷിപ്പിക്കാം. ഫോര്മിക് അമ്ലം (HCOOH), ഥാലിക് അമ്ലം -C6H4 (COOH)2, സിട്രിക് അമ്ലം, -C3H4 (COOH)3, മെല്ലൊഫാനിക് അമ്ലം അഥവാ 1,2,3,5 ബെന്സീന് ടെട്രാകാര്ബോക്സിലിക് അമ്ലം -C6H2 (COOH)4 എന്നിവ യഥാക്രമം മോണോ, ഡൈ, ട്ര, ടെട്രാകാര്ബോക്സിലിക് അമ്ലങ്ങള്ക്ക് ഉദാഹരണങ്ങളാണ്.
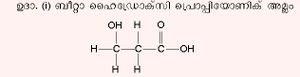
കാര്ബോക്സിലിക് അമ്ലങ്ങളില് കാര്ബോക്സിലിക് ഗ്രൂപ്പിനു പുറമേ മറ്റു ഗ്രൂപ്പുകളും അടങ്ങിയിരിക്കാം. ഹൈഡ്രാക്സില് ഗ്രൂപ്പുകൂടി അടങ്ങിയിട്ടുണ്ടെങ്കില് പ്രസ്തുത കാര്ബോക്സിലിക് അമ്ലത്തിനെ ഹൈഡ്രാക്സി കാര്ബോക്സിലിക് അമ്ലം എന്നു പറയും. ഇവയെയും മോണോഹൈഡ്രാക്സി, ഡൈ ഹൈഡ്രാക്സി, ടെട്രാ ഹൈഡ്രാക്സി എന്നിങ്ങനെ വിശേഷിപ്പിച്ചുവരുന്നു.
ഇത് ഒരു മോണോ ഹൈഡ്രാക്സി കാര്ബോക്സിലിക് അമ്ലമാണ്.
ലവണരൂപീകരണത്തിനു മുക്തമാക്കാവുന്ന ഹൈഡ്രജനുകളുടെ എണ്ണത്തെ അടിസ്ഥാനമാക്കി കാര്ബോക്സിലിക് അമ്ലങ്ങളെ വേറൊരുതരത്തിലും വര്ഗീകരിക്കാം: മോണോബേസിക് അഥവാ ഏകക്ഷാരകം (ഒരു ഹൈഡ്രജന് മാത്രമുള്ളവ); ഡൈബേസിക് അഥവാ ദ്വിക്ഷാരകം (രണ്ടു ഹൈഡ്രജന് ഉള്ളവ); പോളിബേസിക് അഥവാ ബഹുക്ഷാരകം (മൂന്നോ അതിലധികമോ ഹൈഡ്രജന് ഉള്ളവ). കാര്ബോക്സിലിക് ഗ്രൂപ്പുമായി ബന്ധിച്ചിട്ടുള്ള മറ്റു ഗ്രൂപ്പുകളുടെ സ്വഭാവത്തെ അടിസ്ഥാനമാക്കിയും ഈ അമ്ലങ്ങളെ വേര്തിരിക്കാം: ആല്ഡിഹൈഡിക് കാര്ബോക്സിലിക് അമ്ലങ്ങള് (ഉദാ. ഗ്ലയോക്സാലിക് അമ്ലം CHO. COOH); അമിനോ കാര്ബോക്സിലിക് അമ്ലങ്ങള് (ഉദാ. അമിനോ ഫോര്മിക് അമ്ലം, NH2COOH); കീറ്റോണിക് കാര്ബോക്സിലിക് അമ്ലങ്ങള് (ഉദാ. ബെന്സോയില് അസറ്റിക് അമ്ലം, C6H5 COCH2 COOH). ഘടനയെ അടിസ്ഥാനമാക്കി കാര്ബോക്സിലിക് അമ്ലത്തിനെ മൂന്നായി തിരിക്കാം.
(i) ആലിഫാറ്റിക് അമ്ലം. ഇവയെ കാര്ബോക്സില് ഗ്രൂപ്പുകളുടെ എണ്ണത്തെ അടിസ്ഥാനപ്പെടുത്തി മോണോ, ഡൈ, ട്ര എന്നിങ്ങനെ വീണ്ടും വര്ഗീകരിക്കാം. സ്രാതസ്സുകളെ ആസ്പദമാക്കി ഇവയ്ക്ക് സാധാരണനാമവും അടങ്ങിയിരിക്കുന്ന ആല്ക്കേനിനൊപ്പം "ഓയിക് അമ്ലം' എന്നുചേര്ത്ത് ഐയുപിഎസി നാമവും നല്കിവരുന്നു. ഉദാ: HCOOH ഫോര്മിക് അമ്ലം (സാധാരണനാമം) മെഥനോയിക് അമ്ലം (IUPAC നാമം).
(ii) അരോമാറ്റിക് അമ്ലം. ഒന്നോ അധിലധികമോ കാര്ബോക്സില് ഗ്രൂപ്പുകള് ഇവയിലടങ്ങിയിരിക്കും. അരോമാറ്റിക് കാര്ബോക്സിലിക് അമ്ലങ്ങള് രണ്ടുവിധത്തിലുണ്ട്.
1. കാര്ബോക്സില് ഗ്രൂപ്പ് ബെന്സീന് റിങ്ങിനോട് നേരിട്ടു ബന്ധപ്പെട്ടിരിക്കുന്നവയാണ് ഒരു വിഭാഗം. ഉദാ:
ഇവയെയും കാര്ബോക്സില് ഗ്രൂപ്പിന്റെ എണ്ണമനുസരിച്ച് മോണോ, ഡൈ, ട്ര എന്നിങ്ങനെ തരംതിരിച്ചിട്ടുണ്ട്.
2. കാര്ബോക്സില് ഗ്രൂപ്പ്, റിങ്ങിലെ ശാഖയുമായി ബന്ധിക്കപ്പെട്ടിരിക്കുന്ന വിഭാഗമാണ് രണ്ടാമത്തേത്. ഉദാ: അരൈല് ഗ്രൂപ്പുകൊണ്ട് പ്രതിസ്ഥാപിക്കപ്പെട്ട ആലിഫാറ്റിക് അമ്ലങ്ങളായി ഇവയെ പരിഗണിക്കാറുണ്ട്.
(iii) ഹെറ്ററോസൈക്ലിക് അമ്ലം. ഹെറ്ററോസൈക്ലിക് സംയുക്തങ്ങളില് കാര്ബോക്സില് ഗ്രൂപ്പു അടങ്ങിയിട്ടുള്ള സംയുക്തങ്ങളാണിവ. ഉദാ:
ഗുണധര്മങ്ങള്
കാര്ബോക്സിലിക് അമ്ലങ്ങളുടെ ഗുണധര്മങ്ങള് അവയില് അടങ്ങിയിരിക്കുന്ന ഗ്രൂപ്പുകളുടെ സ്വഭാവത്തെ ആശ്രയിച്ചിരിക്കുന്നു. കാര്ബണ് അണുക്കളുടെ എണ്ണം കുറഞ്ഞവയും COOH ഗ്രൂപ്പിന്റെ പ്രസക്തി ഏറിയവയുമായ ആലിഫാറ്റിക അമ്ലങ്ങള് തീക്ഷ്ണഗന്ധമുള്ളവയും ഉയര്ന്ന തിളനിലയുള്ളവയും ജലലേയങ്ങളും ആണ്. ഇവയുടെ ആപേക്ഷിക ഘനത്വം ഒന്നിന് അടുത്തും ആയിരിക്കും. അമ്ലത്തിന്റെ തന്മാത്രാഭാരം വര്ധിക്കുന്നതനുസരിച്ച് COOH ന്റെ പ്രാധാന്യം കുറയുന്നു. തിളനില, ഉരുകല്നില എന്നിവയും ക്രമേണ വര്ധിക്കും. ഗന്ധവും ജലലേയത്വവും കുറയുന്നു. ആപേക്ഷിക ഘനത്വം ബന്ധപ്പെട്ട ഹൈഡ്രാകാര്ബണിലേക്ക് ചുരുങ്ങുന്നു.
ഒരു പ്രാട്ടോണ് സ്വീകാരിയുടെ സാന്നിധ്യത്തില് കാര്ബോക്സിലിക് അമ്ലങ്ങള്ക്ക് അയോണീകരണം നടക്കുന്നു.
R (CXY)nCOOH + H2OšR (CXY)nCOO_ + H3O+
അയോണീകരണത്തിന്റെ വേഗത ലായകത്തിന്റെ (പ്രാട്ടോണ് സ്വീകാരി) ക്ഷാരതയ്ക്ക് നേര് ആനുപാതികവും ഹൈഡ്രാക്സില് ഗ്രൂപ്പിന്റെ O-H ബന്ധശക്തിക്ക് വിപരീതാനുപാതികവുമായിരിക്കും.
ലഘുകാര്ബോക്സിലിക് അമ്ലങ്ങള് നേരിയ തോതിലേ ജലലായനിയില് അയോണീകരിക്കൂ. അയോണീകരിക്കാത്ത COOH ഗ്രൂപ്പിന്റെ ഘടന താഴെ കൊടുക്കുന്നവയുടെ അനുനാദസങ്കരമാണെന്ന് കരുതപ്പെടുന്നു.
സ്വതന്ത്രാവസ്ഥയില് കാര്ബണുകളുടെ എണ്ണം കുറഞ്ഞ അമ്ലങ്ങള് ഡൈമറുകളായി (dimers) സ്ഥിതി ചെയ്യാനുള്ള പ്രവണത കാണിക്കുന്നു. ഈ സന്ദര്ഭത്തില് രണ്ടു തന്മാത്രകളെ തമ്മില് തികച്ചും ദുര്ബലമായ ഹൈഡ്രജന് ബന്ധങ്ങള് അടുപ്പിച്ചു നിര്ത്തുന്നു. ഈ ഹൈഡ്രജന് ബന്ധങ്ങളാണ് താഴെ സൂചിപ്പിക്കുന്ന തരത്തിലുള്ള അമ്ലങ്ങളുടെ ഉയര്ന്ന തിളനിലയ്ക്കു കാരണം. ഉയര്ന്ന കാര്ബോക്സിലിക് അമ്ലങ്ങളില് പോളിമോര്ഫിസത്തിനുള്ള (ബഹുരൂപത) പ്രവണതയാണ് കണ്ടുവരുന്നത്.
രണ്ടുതരത്തിലുള്ള ഘടനാവ്യതിചലനങ്ങള് ഈ അമ്ലങ്ങളില് കണ്ടുവരുന്നു: (i) കാര്ബോക്സില് ഗ്രൂപ്പ് ഉള്ക്കൊള്ളാത്തത്;
(ii) കാര്ബോക്സില് ഗ്രൂപ്പ് ഉള്ക്കൊള്ളുന്നത്. ആദ്യപ്രരൂപത്തില് ശാഖിത ശൃംഖലകളോടുകൂടിയ അമ്ലങ്ങളാണ്. ഉദാ. പിവാലിക്ക് അമ്ലം (CH3)3 C COOH, ആലിസൈക്ലിക് അമ്ലങ്ങള്, ഹൈഡ്രാക്സി അമ്ലങ്ങള്, ഹാലൊജനീകൃത അമ്ലങ്ങള്. രണ്ടാം പ്രരൂപത്തില് പ്രതിസ്ഥാപന പ്രക്രിയയിലൂടെയുള്ള അമ്ലവ്യുത്പന്നങ്ങളാണ്; എസ്റ്ററുകള്, അമ്ലഹാലൈഡുകള്, അമൈഡുകള്, അന്ഹൈഡ്രഡുകള് തുടങ്ങിയവ വിവിധ ഗ്രൂപ്പുകളുടെ പ്രതിസ്ഥാപനങ്ങളിലൂടെ ഉണ്ടാകുന്ന വ്യുത്പന്നങ്ങളാണ്.
പ്രധാനപ്പെട്ട കാര്ബോക്സിലിക് അമ്ലങ്ങള്
മോണോ കാര്ബോക്സിലിക് അമ്ലങ്ങള്
ഏക ക്ഷാരക അമ്ലങ്ങളാണിവ. മോണോ കാര്ബോക്സിലിക് അമ്ലങ്ങളിലെ ഉയര്ന്ന അംഗങ്ങള് (ഉദാ. സ്റ്റിയറിക് അമ്ലം (C17H35 COOH), പാമിറ്റിക് അമ്ലം (C15H31 COOH), ഒലിയിക് അമ്ലം (C17H33 COOH) എണ്ണകളിലും കൊഴുപ്പുകളിലും ഗ്ലിസറൈഡുകളായി കാണപ്പെടുന്നതിനാലും ചില ഭൗതികഗുണങ്ങളില് കൊഴുപ്പുകളോട് സമാനത പുലര്ത്തുന്നതിനാലും ഇവ കൊഴുപ്പമ്ലങ്ങള് എന്നും അറിയപ്പെടുന്നു. മോണോ കാര്ബോക്സിലിക് അമ്ലങ്ങളെ പൂരിതം, അപൂരിതം എന്നിങ്ങനെ രണ്ടായി തിരിക്കാം. സാധാരണ കൊഴുപ്പമ്ലങ്ങള് പൂരിത മോണോ കാര്ബോക്സിലിക് അമ്ലങ്ങളാണ്.
പൂരിത കാര്ബോക്സിലിക് അമ്ലങ്ങള്
മോണോ കാര്ബോക്സിലിക് അമ്ലങ്ങളിലെ ആദ്യ അംഗങ്ങളെല്ലാം ഈ വിഭാഗത്തില്പ്പെടുന്നവയാണ്. ഉദാ. ഫോര്മിക് അമ്ലം, അസറ്റിക് അമ്ലം, പ്രാപ്പിയോണിക് അമ്ലം, ബ്യൂട്ടെറിക് അമ്ലം തുടങ്ങിയവ. ആല്ക്കഹോളുകള്, ആല്ഡിഹൈഡുകള്, കീറ്റോണുകള് എന്നിവയുടെ ഓക്സീകരണം വഴിയോ ആല്ക്കൈല് സയനൈഡുകളുടെ ജലാപഘടനം വഴിയോ കാര്ബണ് ഡൈഓക്സൈഡും ഗ്രിഗ്നാര്ഡ് റിയേജന്റും തമ്മില് പ്രതിപ്രവര്ത്തിപ്പിച്ചോ പൂരിത മോണോ കാര്ബോക്സിലിക് അമ്ലങ്ങള് ഉത്പാദിപ്പിക്കാം.
R.CH2OH R.CHO R.COOH RC º N R.CO.NH2 R.COOH CO2 + RMgI R.COOMgI R.COOH
ഫോര്മിക് അമ്ലം
ഫോര്മിക് അമ്ലം (HCOOH).ഏറ്റവും ലഘുവായ മോണോ കാര്ബോക്സിലിക് അമ്ലമാണിത്. ഉറുമ്പ്, തേനീച്ച, കടന്നല് എന്നിവയില് കാണപ്പെടുന്നു. 1670ല് ചുവന്ന ഉറുമ്പുകളെ സ്വേദനം ചെയ്താണ് ഫോര്മിക് അമ്ലം ആദ്യമായി നിര്മിച്ചത്. ഉറുമ്പ് എന്നര്ഥം വരുന്ന ലാറ്റിന്വാക്കായ "ഫോര്മിക്ക'യില് നിന്നാണ് ഫോര്മിക് അമ്ലമെന്ന പേര് ലഭിച്ചത്. മൂത്രത്തിലും വിയര്പ്പിലും കുറഞ്ഞ അളവില് അടങ്ങിയിരിക്കുന്നു. ചൂടാക്കിയ NaOH ലായനിയിലൂടെ കാര്ബണ് മോണോക്സൈഡ് കടത്തിവിട്ട് ഉണ്ടാകുന്ന സോഡിയം ഫോര്മേറ്റിനെ, ഹൈഡ്രാക്ലോറിക് അമ്ലവുമായി പ്രതിപ്രവര്ത്തിപ്പിച്ച് ഫോര്മിക് അമ്ലം പരീക്ഷണശാലയില് ഉണ്ടാക്കുന്നു.
CO + NaOH HCOONa HCOOH
നിറമില്ലാത്ത രൂക്ഷഗന്ധമുള്ള ദ്രാവകമാണിത്. ഉരുകല്നില 8.4ºC. തിളനില 100.5ºC. ജലം, ആല്ക്കഹോള്, ഈഥര് എന്നിവയില് ലേയമാണ്. ത്വക്കില് ഇവ പൊള്ളലുണ്ടാക്കുന്നു. പൂരിത മോണോകാര്ബോക്സിലിക് അമ്ലങ്ങളില് രാസപരമായി ഏറ്റവും ശക്തിയേറിയ അമ്ലമാണിത്. ഫോര്മിക് അമ്ലം ഒരേസമയം ആല്ഡിഹൈഡിന്റെയും അമ്ലത്തിന്റെയും ഗുണങ്ങള് പ്രകടിപ്പിക്കുന്നു.
തുണിവ്യവസായത്തില് മോര്ഡന്റുകള് ഉണ്ടാക്കുവാഌം റബ്ബര് വ്യവസായത്തില് റബ്ബര് ലാറ്റക്സ് കൊയാഗുലീകരിക്കുന്നതിഌം ഫോര്മിക് അമ്ലം ഉപയോഗിക്കുന്നു. ഊറയ്ക്കിട്ട തുകലിലെ ചുണ്ണാമ്പ് നീക്കം ചെയ്യുവാന് ഫോര്മിക് അമ്ലം ഫലപ്രദമാണ്. പഴങ്ങള് കേടുവരാതെ സൂക്ഷിക്കുന്നതിഌം പ്ലാസ്റ്റിക്, ഔഷധങ്ങള് എന്നിവയുടെ നിര്മാണത്തിലും അണുനാശിനിയായും ഉപയോഗിക്കുന്നു.
അസറ്റിക് അമ്ലം
അസറ്റിക് അമ്ലം (CH3COOH).വിനാഗിരി എന്ന നിലയില് അസറ്റിക് അമ്ലം പണ്ടുമുതല്ക്കേ ഉപയോഗിച്ചിരുന്നു. അസറ്റിക് അമ്ലത്തിന്റെ നേര്ത്ത ലായനി (78 ശ.മാ.)യാണ് വിനാഗിരി. വിനാഗിരി എന്നര്ഥമുള്ള "അസറ്റം' എന്ന ലാറ്റിന് പദത്തില് നിന്നാണ് അസറ്റിക് അമ്ലം എന്ന പേര് ലഭിച്ചത്. നിരവധി പഴസത്തുകളില് സ്വതന്ത്രാവസ്ഥയില് ഇത് കാണപ്പെടുന്നു. ഉണങ്ങിയ മരത്തടിയുടെ ഭഞ്ജകസ്വേദനം വഴി ലഭിക്കുന്ന പൈറോലിഗ്നിയസ് അമ്ലത്തില് നിന്നും അസറ്റിക് അമ്ലം വ്യാവസായികമായി ഉത്പാദിപ്പിക്കാം. അസറ്റിലിന് വാതകത്തില്നിന്ന് താഴെപറയുന്ന പ്രതിപ്രവര്ത്തനങ്ങളിലൂടെ അസറ്റിക് അമ്ലം കൂടുതലായി ഉത്പാദിപ്പിച്ചുവരുന്നു.
HC º CH + H2O CH3CHO
CH3CHO CH3COOH
സാധാരണ ഊഷ്മാവില്, നിറമില്ലാത്ത രൂക്ഷഗന്ധമുള്ള പുളിരുചിയുള്ള ഒരു ദ്രാവകമാണിത്. 16.5ºC നുതാഴെ തണുപ്പിച്ചാല് അസറ്റിക് അമ്ലം ഖരമായി ഗ്ലേഷ്യല് അസറ്റിക് അമ്ലം രൂപീകരിക്കുന്നു. തിളനില 118ºC. ജലം, ആല്ക്കഹോള്, ഈഥര് എന്നിവയില് ലയിക്കും. ഫോസ്ഫറസ്, സള്ഫര്, അയോഡിന് എന്നിവയുടെയും നിരവധി കാര്ബണ് സംയുക്തങ്ങളുടെയും ഒരു നല്ല ലായകമാണ് അസറ്റിക് അമ്ലം. ദ്രാവകാവസ്ഥയില് ഡൈമറായി സ്ഥിതിചെയ്യുന്നു.
വിവിധ ചായങ്ങള്, പെര്ഫ്യൂമുകള്, റയോണ് എന്നിവയുടെ നിര്മാണത്തില് ഉപയോഗിച്ചുവരുന്നു. അച്ചാറുകളിലും മറ്റും വിനാഗിരി ഉപയോഗിക്കുന്നു, പല അസറ്റേറ്റുകളും ഔഷധമായി ഉപയോഗിക്കുന്നു. ഫിനാസെറ്റിന്, ആസ്പിരിന് എന്നിവയുടെ നിര്മാണത്തിലും വ്യാവസായിക പ്രാധാന്യമുള്ള അസറ്റോണ്, അസറ്റിക് അന്ഹൈഡ്രഡ് തുടങ്ങിയ രാസവസ്തുക്കളുടെ നിര്മാണത്തിലും പ്രയോജനപ്പെടുത്തുന്നു. ആല്ക്കലി അസറ്റേറ്റുകള് മൂത്രസംവര്ധകമായും ലെഡ് അസറ്റേറ്റും കോപ്പര് അസറ്റേറ്റും പെയിന്റുകളായും ഉപയോഗിച്ചുവരുന്നു.
ഫോര്മിക് അമ്ലം, അസറ്റിക് അമ്ലം എന്നിവയ്ക്കു പുറമേ പ്രാപ്പിയോണിക് അമ്ലം, ബ്യൂട്ടൈറിക് അമ്ലം എന്നിവ വേര്തിരിക്കപ്പെടുകയും പഠനവിധേയമാവുകയും ചെയ്തിട്ടുണ്ട്. പശുവിന്പാലില് സു. 10 ശതമാനം ബ്യൂട്ടൈറിക് അമ്ലം അടങ്ങിയിരിക്കുന്നു.
പൂരിത മോണോ കാര്ബോക്സിലിക് അമ്ലങ്ങളിലെ ഉയര്ന്ന അംഗങ്ങളാണ് സാധാരണ കാണപ്പെടുന്ന കൊഴുപ്പമ്ലങ്ങള്. ഇവ എണ്ണകളിലും കൊഴുപ്പുകളിലും ഗ്ലിസറൈഡുകളായും മെഴുകിലെ ഉയര്ന്ന ആല്ക്കഹോള് എസ്റ്ററുകളായും കാണപ്പെടുന്നു. പാമിറ്റിക് അമ്ലം (C15H31COOH),സ്റ്റിയറിക് അമ്ലം (C17H35COOH) എന്നിവയാണ് ഇവയില് പ്രമുഖം. കൊഴുപ്പുകളുടെ ജലാപഘടനത്തിലൂടെയാണ് ഇവ ലഭിക്കുന്നത്. മറ്റൊരു പ്രധാന അമ്ലമായ ലോറിക് അമ്ലം (C11H23COOH) വെളിച്ചെണ്ണ (4550 ശ.മാ.); പാം ഓയില് (4555 ശ.മാ.) എന്നിവയില് നിന്നും ലഭിക്കുന്നു. മേല്പ്പറഞ്ഞ അമ്ലങ്ങളെല്ലാം സോപ്പുനിര്മാണത്തില് ഉപോത്പന്നങ്ങളായി ലഭിക്കുന്നവയാണ്.
അപൂരിത മോണോകാര്ബോക്സിലിക് അമ്ലങ്ങള്
അപൂരിത മോണോകാര്ബോക്സിലിക് അമ്ലങ്ങള്. കൊഴുപ്പുകളില് കാണുന്ന ദീര്ഘശൃംഖലാ സംയുക്തങ്ങളും (ഉദാ. ഒലിയിക് അമ്ലം) ഹ്രസ്വശൃംഖലാ സംയുക്തങ്ങളു(ഉദാ. അക്രിലിക് അമ്ലം, ക്രാട്ടോണിക് അമ്ലം)മാണ് അപൂരിത മോണോകാര്ബോക്സിലിക് അമ്ലങ്ങളിലെ പ്രധാനപ്പെട്ടവ. ഇവ പ്രകൃതിയില് സുലഭമല്ല.
അക്രിലിക് അമ്ലം
അക്രിലിക് അമ്ലം (CH2=CHCOOH).അപൂരിത മോണോകാര്ബോക്സിലിക് അമ്ലങ്ങളിലെ ഏറ്റവും ലഘുവായ അമ്ലമാണിത്. അക്രാലീന് എന്ന ആല്ഡിഹൈഡില് നിന്നാണ് അക്രിലിക് അമ്ലത്തിന് ഈ പേര് ലഭിച്ചത്. നിക്കല് കാര്ബൊണൈല് ഉത്പ്രരകത്തിന്റെ സാന്നിധ്യത്തില് അസറ്റിലീന്, കാര്ബണ് മോണോക്സൈഡ്, ജലം എന്നിവ തമ്മില് പ്രതിപ്രവര്ത്തിപ്പിച്ചാണ് അക്രിലിക് അമ്ലം വന്തോതില് ഉത്പാദിപ്പിക്കുന്നത്. അക്രിലോ നൈട്രലിന്റെ ജലാപഘടനം വഴിയും ഇവ ഉത്പാദിപ്പിക്കാം.
HC º CH + HCN CH2 CH.CN CH2 CHCOOH അസറ്റിലീന് അക്രലോനൈട്രല് അക്രിലിക് അമ്ലം
നിറമില്ലാത്ത രൂക്ഷഗന്ധമുള്ള ദ്രാവകമാണ് അക്രിലിക് അമ്ലം. തിളനില 142ºC. ജലവുമായി ഏതളവിലും മിശ്രണീയമാണ്. അസറ്റിക് അമ്ലത്തെക്കാള് തീവ്രത പ്രദര്ശിപ്പിക്കുന്നു. ഇവ അക്രിലേറ്റുകള് എന്ന പോളിമറുകളുടെ ഉത്പാദനത്തിലുപയോഗിക്കുന്നു.
ക്രാട്ടോണിക് അമ്ലം
ക്രാട്ടോണിക് അമ്ലം (ട്രാന്സ് 2, ബ്യൂട്ടനോയിക് അമ്ലം; CH3CH=CHCOOH).ക്രാട്ടണ് എണ്ണയില് ഗ്ലിസറൈഡായി ഇവ കാണപ്പെടുന്നു. ക്രാട്ടണാല്ഡിഹൈഡിനെ അമോണിയാക്കല് സില്വര് നൈട്രറ്റിന്റെ സാന്നിധ്യത്തില് ഓക്സീകരിച്ച് ക്രാട്ടോണിക് അമ്ലം ഉത്പാദിപ്പിക്കുന്നു. നിറമില്ലാത്ത പരലുകളായ ഇവയുടെ ഉരുകല്നില 72ºC ആണ്. സിസ്, ട്രാന്സ് ഐസോമെറിസം പ്രദര്ശിപ്പിക്കുന്നു. പ്രകൃതിയില് കാണപ്പെടുന്നത് ട്രാന്സ് ഐസോമറാണ്.
ഒലിയിക് അമ്ലം
ഒലിയിക് അമ്ലം [CH3(CH2)7CH=CH(CH2)7COOH]. ഒലീവ് എണ്ണ, ലിന്സീഡ് എണ്ണ, പരുത്തിക്കുരു എണ്ണ എന്നിവയില് ഗ്ലിസറൈഡായി കാണപ്പെടുന്നു. ഒലീവ് എണ്ണ സോഡിയം ഹൈഡ്രാക്സൈഡുമായി ജലാപഘടനത്തിനു വിധേയമാക്കുമ്പോള് ഒലിയിക് അമ്ലം, പാമിറ്റിക് അമ്ലം; സ്റ്റിയറിക് അമ്ലം എന്നിവയുടെ സോഡിയം ലവണങ്ങള് ലഭിക്കുന്നു. ജലലേയമായ ഇവ ജലീയ ലെഡ് അസറ്റേറ്റുമായി പ്രതിപ്രവര്ത്തിപ്പിച്ച് അലേയമായ ലെഡ് ലവണങ്ങളാക്കി മാറ്റുന്നു. ഉണങ്ങിയ ലെഡ് ലവണങ്ങള് ഈഥറുമായി സമ്പര്ക്കത്തില് വരുമ്പോള് ലെഡ് ഒലിയേറ്റുമാത്രം ഈഥറില് ലയിക്കുകയും മറ്റു രണ്ടെണ്ണം അലേയമായിരിക്കുകയും ചെയ്യും. ഈഥര് ലായനി അരിച്ച്, ഈഥര് ബാഷ്പീകരിക്കുമ്പോള് ലഭിക്കുന്ന അവക്ഷിപ്തം ഒരു ധാതു അമ്ലവുമായി തപിപ്പിക്കുമ്പോള് ഒലിയിക് അമ്ലം ലഭിക്കുന്നു. ഇവയെ വേര്തിരിച്ച്, ജലവിമുക്തമാക്കി സ്വേദനം ചെയ്ത് ശുദ്ധീകരിച്ചെടുക്കാം.
നിറമില്ലാത്ത എണ്ണമയമുള്ള ഒലിയിക് അമ്ലം ജലത്തില് അലേയമാണ്. തിളനില 286ºC, ഉരുകല്നില 16ºC. സോപ്പുനിര്മാണത്തിലും എയ്റോസോളുകളില് എമള്സികാരകം എന്നീ നിലകളിലും ഒലിയിക് അമ്ലം ഉപയോഗിക്കുന്നു.
കൊഴുപ്പമ്ലങ്ങളോട് പല തരത്തിലും സാദൃശ്യം ഉള്ളവയാണ് അരോമാറ്റിക കാര്ബോക്സിലിക് അമ്ലങ്ങള്. ഇവ ക്രിസ്റ്റല് രൂപത്തിലുള്ള ഖരപദാര്ഥങ്ങളാണ്. ജലത്തില് അല്പമായും ചാരായം, ഈഥര് എന്നിവയില് നല്ലവണ്ണവും ലയിക്കുന്നു. ലഘുവായ അമ്ലങ്ങളെ സ്വേദനം ചെയ്യാം. എന്നാല് സങ്കീര്ണമായവ സ്വേദനത്തില് വിഘടിക്കുന്നു. ബെന്സോയിക് അമ്ലം, ഹിപ്പ്യൂറിക് അമ്ലം, ഫീനൈല് അസറ്റിക് അമ്ലം എന്നിവ ഏകക്ഷാരക പൂരിത ആരോമാറ്റിക് അമ്ലങ്ങള്ക്കും സിന്നമിക് അമ്ലം, അട്രാപിക് അമ്ലം തുടങ്ങിയവ ഏകക്ഷാരക അപൂരിത ആരോമാറ്റിക അമ്ലങ്ങള്ക്കും ഉദാഹരണങ്ങളാണ്.
ഡൈ കാര്ബോക്സിലിക് അമ്ലങ്ങള്
രണ്ടു കാര്ബോക്സില് ഗ്രൂപ്പുകള് അടങ്ങിയിട്ടുള്ള അമ്ലങ്ങളാണിവ. ദ്വിക്ഷാരക (ഡൈബേസിക്) അമ്ലങ്ങള് എന്നും ഇവ അറിയപ്പെടുന്നു. ഇവ പൂരിതമോ അപൂരിതമോ ആവാം. പൂരിത ഡൈകാര്ബോക്സിലിക് അമ്ലങ്ങള് CnH2n(COOH)2 എന്ന ഫോര്മുല അനുസരിക്കുന്നവയാണ്. എല്ലാ ഡൈകാര്ബോക്സിലിക് അമ്ലങ്ങളും നിറമില്ലാത്ത ക്രിസ്റ്റല് ഘടനയുള്ള ഖരപദാര്ഥങ്ങളാണ്. മോണോ കാര്ബോക്സിലിക് അമ്ലങ്ങളെക്കാള് ശക്തിയേറിയ ഇവ രണ്ടുതരം ലവണങ്ങള് രൂപീകരിക്കുന്നു.
പൂരിത ഡൈകാര്ബോക്സിലിക് അമ്ലങ്ങള്
ഓക്സാലിക് അമ്ലം
ഓക്സാലിക് അമ്ലം (COOH)2 2H2O. ഡൈകാര്ബോക്സിലിക് അമ്ലങ്ങളില് ഏറ്റവും പ്രധാന അമ്ലമാണിത്. ഓക്സാലിസ് വിഭാഗത്തില്പ്പെട്ട സസ്യങ്ങളില് നിന്നു ലഭിക്കുന്നതിനാലാണ് ഈ അമ്ലത്തിന് പ്രസ്തുത നാമം ലഭിച്ചത്. കൂടാതെ റൂമെക്സ് കുടുംബത്തിലെ സസ്യങ്ങളിലും ഇരുമ്പിന്റെയും കാത്സ്യത്തിന്റെയും ഓക്സലേറ്റുകളായി ധാതുക്കളിലും കാണപ്പെടുന്നു.
കാര്ബണ്മോണോക്സൈഡ് സോഡിയം ഹൈഡ്രാക്സൈഡുമായി പ്രതിപ്രവര്ത്തിപ്പിച്ചുകിട്ടുന്ന സോഡിയം ഫോര്മേറ്റ് തപിപ്പിച്ചാണ് വ്യാവസായികമായി ഓക്സാലിക് അമ്ലം നിര്മിക്കുന്നത്. പഞ്ചസാര ഗാഢനൈട്രിക് അമ്ലവുമായി ചേര്ത്ത് ചൂടാക്കിയാണ് പരീക്ഷണശാലയില് ഓക്സാലിക് അമ്ലം ഉത്പാദിപ്പിക്കുന്നത്. ഇത് ഒരു വിഷവസ്തുവാണ്. ജലത്തിലും ആല്ക്കഹോളിലും ലേയമാണ്. ക്രിസ്റ്റലീകരണത്തിലൂടെ ഓക്സാലിക് അമ്ലത്തില് ജലാംശം അടങ്ങിയിരിക്കുന്നു. പൊട്ടാസ്യം പെര്മാംഗനേറ്റിന്റെ ചൂടാക്കിയ അമ്ലലായനി ഓക്സാലിക് അമ്ലത്തെ എളുപ്പത്തില് ഓക്സീകരിച്ച് കാര്ബണ് ഡൈഓക്സൈഡ് നല്കുന്നു.
2KMnO4+3H2SO4+5H2C2O4 K2SO4+2MnSO4+10CO2+8H2O
ചായമിടീല് പ്രക്രിയയില് മോര്ഡന്റായും കാലിക്കോ പ്രിന്റിങിലും ഓക്സാലിക് അമ്ലം ഉപയോഗിക്കുന്നു. മഷിക്കറ, ഇരുമ്പുകറ എന്നിവ നീക്കംചെയ്യുവാഌം വൈക്കോല്, തടി, തുകല് എന്നിവ ബ്ലീച്ച് ചെയ്യാഌം ഓക്സാലിക് അമ്ലം ഉപയോഗിക്കാം. ചിലയിനം ചായങ്ങളുടെയും മഷികളുടെയും നിര്മാണത്തിലും ഇതുപയോഗിക്കുന്നു. കാര്ബണ് മോണോക്സൈഡ്, ഫോര്മിക് അമ്ലം, അലൈല് ആല്ക്കഹോള് എന്നിവയുടെ നിര്മാണത്തിലും വോളുമെട്രിക പരീക്ഷണങ്ങളിലും പ്രയോജനപ്പെടുത്തിവരുന്നു. ഫെറസ് പൊട്ടാസ്യം ഓക്സലേറ്റ് [(K2C2O4)2 H2O] ഫോട്ടോഗ്രാഫിയില് ഡെവലപ്പറായി ഉപയോഗിക്കുന്നു.
മലോണിക് അമ്ലം
മലോണിക് അമ്ലം [H2C(COOH)2]. ബീറ്റ്റൂട്ടില് കാത്സ്യം ലവണമായി ഇത് കാണപ്പെടുന്നു. മാലിക് അമ്ലത്തിന്റെ ഓക്സീകരണം വഴിയാണ് ഇത് ആദ്യമായി നിര്മിച്ചത്. അസറ്റിക് അമ്ലത്തില് നിന്നും മലോണിക് അമ്ലം നിര്മിക്കുന്ന പ്രക്രിയ ചുവടെ കൊടുക്കുന്നു.
CH3COOH CH2CICOOH CH2CICOOH CH2CNCOOH H2C
മലോണിക് അമ്ല എസ്റ്ററായ ഡൈ ഈഥൈല് മലോണേറ്റ് [CH2(COOCH2CH3)2] വളരെ പ്രധാനപ്പെട്ട ഒരു സംശ്ലേഷണ അഭികാരകമാണ്. അനുനാദസ്ഥിരതയുള്ള കാര്ബാനയോണ് എളുപ്പത്തില് രൂപീകരിക്കുവാന് കഴിയുന്ന ഇവ, അസറ്റിക് അമ്ലത്തിന്റെ ഏക, ദ്വി, പ്രതിസ്ഥാപിത വ്യുത്പന്നങ്ങള്, കൊഴുപ്പമ്ലങ്ങള്, അപൂരിത അമ്ലങ്ങള്, ചാക്രിക സംയുക്തങ്ങള് എന്നിവ നിര്മിക്കുവാന് ഉപയോഗിക്കുന്നു.
സക്സിനിക് അമ്ലം
സക്സിനിക് അമ്ലം (HOOC.CH2.CH2.COOH). ആംബര് സ്വേദനം ചെയ്താണ് സക്സിനിക് അമ്ലം ആദ്യമായി ഉത്പാദിപ്പിച്ചത്. പഞ്ചസാരയുടെ കിണ്വനപ്രക്രിയയിലും സക്സിനിക് അമ്ലമുണ്ടാവുന്നുണ്ട്. മാലിക് അമ്ലത്തെയോ ടാര്ടാറിക് അമ്ലത്തെയോ ഹൈഡ്രാ അയഡിക് അമ്ലംകൊണ്ട് നിരോക്സീകരിച്ച് ഈ അമ്ലം ഉത്പാദിപ്പിക്കാം.
CH(OH).COOH +2HI CH2.COOH +H2O+I2 CH2.COOH CH2.COOH CH(OH).COOH +4HI CH2.COOH +2H2O+2I2 CH(OH).COOH CH2.COOH
ഓക്സാലിക് അമ്ലത്തില്നിന്നും മലോണിക് അമ്ലത്തില്നിന്നും വ്യത്യസ്തമായി സക്സിനിക് അമ്ലം ചൂടാക്കുമ്പോള് ജലാംശം നഷ്ടപ്പെട്ട് ഒരു ചാക്രിക അന്ഹൈഡ്രഡ് രൂപീകരിക്കുന്നു.
CH2.COOH CH2.CO O +H2O CH2.COOH CH2.CO
ആല്ക്കൈല് റെസിനുകള്, പോളി എസ്റ്റര് റെസീനുകള്, ചായങ്ങള്, പെര്ഫ്യൂമുകള് എന്നിവയുടെ നിര്മാണത്തിലും ഔഷധങ്ങളിലും വോളുമെട്രിക അഭികാരകം എന്ന നിലയിലും സക്സിനിക് അമ്ലം ഉപയോഗിക്കുന്നു.
ഗ്ലൂട്ടാറിക് അമ്ലം
ഗ്ലൂട്ടാറിക് അമ്ലം [HOOC(CH2)3.COOH]. ട്രമെഥിലീന് സയനൈഡ് ഹൈഡ്രാക്ലോറിക് അമ്ലവുമായി ജലാപഘടനം നടത്തി ഇതുത്പാദിപ്പിക്കാം.
സക്സിനിക് അമ്ലത്തെപോലെ, ഗ്ലൂട്ടാറിക് അമ്ലവും ചാക്രിക അന്ഹൈഡ്രഡ് രൂപീകരിക്കുന്നു.
H2C CH2 COOH H2C CH2 CO O +H2O
CH2 COOH CH2 CO
അഡിപിക് അമ്ലം
അഡിപിക് അമ്ലം (HOOC.(CH2)4.COOH). കൊഴുപ്പുകളുടെ ഓക്സീകരണത്തിലൂടെയാണ് അഡിപിക് അമ്ലം ആദ്യമായി ഉത്പാദിപ്പിച്ചത്. ഫിനോളിന്റെ ഉത്പ്രരിത ഹൈഡ്രജനീകരണത്തിലൂടെ ലഭിക്കുന്ന സൈക്ലോ ഹെക്സനോളിനെ ഓക്സീകരിച്ചാല് അഡിപിക് അമ്ലം ലഭിക്കും. ഹെക്സാമെഥിലീന് ഡൈ അമീനുമായി അഡിപിക് അമ്ലം സംഘനനം ചെയ്താണ് നൈലോണ് ഉത്പാദിപ്പിക്കുന്നത്. പോളി എസ്റ്ററുകളുടെ നിര്മാണത്തിലും ഇതുപയോഗിക്കുന്നു.
അപൂരിത ഡൈകാര്ബോക്സിലിക് അമ്ലങ്ങള്
മലിയിക് അമ്ലവും ഫ്യുമേറിക് അമ്ലവുമാണ് പ്രധാനപ്പെട്ടവ. ബ്യൂട്ടൈന് ഡൈ ഓയിക് അമ്ലത്തിന്റെ സിസ്, ട്രാന്സ് ഐസോമറുകളാണിവ.
മലിയിക് അമ്ലം
മലിയിക് അമ്ലം . ബ്യൂട്ടൈന് ഡൈ ഓയിക് അമ്ലത്തിന്റെ സിസ് ഐസോമറാണിത്. പ്രകൃതിയില് കാണപ്പെടുന്നില്ല. മാലിക് അമ്ലം തപിപ്പിച്ചാണ് മലിയിക് അമ്ലം ഉത്പാദിപ്പിക്കുന്നത്.
CH(OH).COOH CH.CO O HC COOH CH2. COOH CH.CO HC COOH
മലിയിക് അമ്ലം 200ºC ല് ദീര്ഘനേരം തപിപ്പിച്ചാല് ഫ്യൂമാറിക് അമ്ലം ലഭിക്കും. ഇവയിലെ തന്മാത്രാന്തര ഹൈഡ്രജന് ബന്ധനം മലിയിക് അമ്ലത്തെ ഫ്യുമാറിക് അമ്ലത്തേക്കാള് ശക്തിയേറിയതാക്കുന്നു. വാര്ണിഷുകളുടെ നിര്മാണത്തിലും പാല്പ്പൊടിയുടെ വികൃതഗന്ധീകരണം (rancidity) തടയുന്നതിഌം ഇതുപയോഗിക്കുന്നു. ഡീല്സ് ആല്ഡര് സംശ്ലേഷണത്തില് അന്ഹൈഡ്രഡായും ഇതുപയോഗിക്കുന്നു.
ഫ്യൂമാറിക് അമ്ലം
ഫ്യുമാറിക് അമ്ലം . ബ്യൂട്ടൈന് ഡൈ ഓയിക് അമ്ലത്തിന്റെ ട്രാന്സ് ഐസോമറാണിത്. നിരവധി മോള്ഡുകളിലും ഫ്യുമാറിയ ഒഫിഷ്യാനിലിസ്എന്ന ചെടിയുടെ സത്തിലും ഫ്യുമാറിക് അമ്ലം അടങ്ങിയിരിക്കുന്നു. മാലിക് അമ്ലം 150ºCല് ദീര്ഘനേരം തപിപ്പിച്ചാല് ഫ്യുമാറിക് അമ്ലം ലഭിക്കും.
HOOC CH CH COOH HOOC CH = CH COOH + H2O
പ്രതിസ്ഥാപിത കാര്ബോക്സിലിക് അമ്ലങ്ങള്
കാര്ബോക്സിലിക് അമ്ലങ്ങളിലെ ഒന്നോ അതില് കൂടുതലോ ആല്ക്കൈല് ഹൈഡ്രജന് ആറ്റങ്ങള് മറ്റു ആറ്റങ്ങളോ (ഉദാ. Cl), ഗ്രൂപ്പുകളോ (ഉദാ. OH, NH2, CH3CO) കൊണ്ട് പ്രതിസ്ഥാപിച്ചുണ്ടാകുന്ന അമ്ലങ്ങളാണിവ. ഹാലൊജന് പ്രതിസ്ഥാപിത അമ്ലങ്ങള്, മോണോ ഹൈഡ്രാക്സി അമ്ലങ്ങള്, ഹൈഡ്രാക്സി പോളി കാര്ബോക്സിലിക് അമ്ലങ്ങള് എന്നിവയാണ് പ്രധാനപ്പെട്ടവ.
ഹാലജന് പ്രതിസ്ഥാപിത കാര്ബോക്സിലിക്
അമ്ലത്തിലെ ഒന്നോ അതിലധികമോ ആല്ക്കൈല് ഹൈഡ്രജന് ആറ്റങ്ങള് ഹാലജന് ആറ്റങ്ങളാല് പ്രതിസ്ഥാപനം ചെയ്താണ് ഇവ ഉണ്ടാക്കുന്നത്. സാധാരണ താപനിലയില് നിറമില്ലാത്ത ദ്രാവകങ്ങളായോ ഖരവസ്തുക്കളായോ ആണ് ഹാലജന് പ്രതിസ്ഥാപിത അമ്ലങ്ങള് കാണപ്പെടുന്നത്. ജലത്തില് ലയിക്കുന്ന ഇവ ബന്ധപ്പെട്ട കൊഴുപ്പമ്ലങ്ങളെക്കാള് തീവ്രത കൂടിയവയാണ്. ക്ലോറോ അസറ്റിക് അമ്ലങ്ങളാണ് ഇവയില് പ്രധാനപ്പെട്ടവ.
മോണോക്ലോറോ അസറ്റിക് അമ്ലം
മോണോ ക്ലോറോ അസറ്റിക് അമ്ലം (CH2Cl COOH). ചുവന്ന ഫോസ്ഫറസിന്റെയും സൂര്യപ്രകാശത്തിന്റെയും സാന്നിധ്യത്തില് ചൂടാക്കിയ അസറ്റിക് അമ്ലത്തിലൂടെ ക്ലോറിന് കടത്തിവിട്ടാല് മോണോക്ലോറോ അസറ്റിക് അമ്ലം ലഭിക്കുന്നു.
CH3 COOH + Cl2 CH2Cl COOH + HCl
ജലത്തില് ലയിക്കുന്ന നീണ്ട പരലുകളായിട്ടാണ് ഇവ കാണപ്പെടുന്നത്. പൊട്ടാസ്യം ഹൈഡ്രാക്സൈഡ്, പൊട്ടാസ്യം സയനൈഡ്, പൊട്ടാസ്യം അയൊഡൈസ്, അമോണിയ എന്നിവ ഓരോന്നുമായി പ്രതിപ്രവര്ത്തിച്ച് യഥാക്രമം ഗ്ലൈക്കോളിക് അമ്ലം, സയനോഅസറ്റിക് അമ്ലം, അയഡോഅസറ്റിക് അമ്ലം, ഗ്ലൈസീന് എന്നിവ ഉത്പാദിപ്പിക്കുന്നു.
CH2.Cl COOH + KOH CH2OH COOH + KCl ഗ്ലൈക്കോളിക് അമ്ലം CH2 Cl COOH + KCN CH2(CN) COOH + KCl സയനോ അസറ്റിക് അമ്ലം CH2 Cl COOH + KI CH2I COOH + KCl അയഡോ അസറ്റിക് അമ്ലം CH2 Cl COOH + 2NH3 CH2 NH2 COOH + NH4Cl ഗ്ലൈസീന്
നീല(ഇന്ഡിഗോ)ത്തിന്റെയും എഥിലീന് ഡൈ അമീന് ടെട്രാ അസറ്റിക് അമ്ലം (EDTA), ജീവകങ്ങള്, കഫീന് തുടങ്ങി നിരവധി കാര്ബണിയ സംയുക്തങ്ങളുടെയും സംശ്ലേഷണത്തിന് ഉപയോഗിക്കുന്നു.
ഡൈക്ലോറോ അസറ്റിക് അമ്ലം
ഡൈക്ലോറോ അസറ്റിക് അമ്ലം (CHCl2 COOH). ക്ലോറാല്ഹൈഡ്രറ്റിനെ സോഡിയം സയനൈഡ് ചേര്ത്ത് തപിപ്പിച്ചാണ് ഡൈക്ലോറോ അസറ്റിക് അമ്ലം നിര്മിക്കുന്നത്.
Cl OH Cl OH Cl O Cl C C OH Cl C C OHCl C C Cl H H OH
നിറമില്ലാത്തതും ജലം, ആല്ക്കഹോള്, ഈഥര് എന്നിവയില് ലേയവുമായ ഒരു ദ്രാവകമാണിത്. ഔഷധങ്ങളിലുപയോഗിക്കുന്നു.
ടെട്രാക്ലോറോ അസറ്റിക് അമ്ലം
ടെട്രാക്ലോറോ അസറ്റിക് അമ്ലം (Cl3C.COOH). ക്ലോറാല് ഹൈഡ്രറ്റിനെ സാന്ദ്രനൈട്രിക് അമ്ലംകൊണ്ട് ഓക്സീകരിക്കുമ്പോള് ഇത് ലഭിക്കുന്നു. നിറമില്ലാത്ത പരലുകളായി കാണപ്പെടുന്ന ഇവയ്ക്ക് രൂക്ഷഗന്ധമാണുള്ളത്. ജലം, ആല്ക്കഹോള്, ഈഥര് എന്നിവയില് ലേയമാണ്. ജലമോ ക്ഷാരമോ ചേര്ത്ത് തിളപ്പിച്ചാല് ക്ലോറോഫോം ലഭിക്കുന്നു.
ആല്ബുമിന്റെ നിര്ണയനത്തിനുള്ള അഭികാരകമായി ഇതുപയോഗിക്കുന്നു. കാര്ബണിക സംശ്ലേഷണങ്ങളിലും ഔഷധങ്ങളിലും ഫലപ്രദമാണ്.
ഹൈഡ്രാക്സി പ്രതിസ്ഥാപിത കാര്ബോക്സിലിക് അമ്ലങ്ങള്
മോണോഹൈഡ്രാക്സി അമ്ലങ്ങള്. മോണോ കാര്ബോക്സിലിക് അമ്ലങ്ങളിലെ ഒരു ആല്ക്കൈല് ഹൈഡ്രജന് ഒരു ഹൈഡ്രാക്സില് ഗ്രൂപ്പുകൊണ്ട് പ്രതിസ്ഥാപിച്ചുണ്ടാകുന്നവയാണിവ. പ്രകൃതിയില് കാണപ്പെടുന്ന മോണോ ഹൈഡ്രാക്സി അമ്ലങ്ങളാണ് ഗ്ലൈക്കോളിക് അമ്ലം (HO.CH2.COOH), ലാക്റ്റിക് അമ്ലം [CH3 CH (OH) COOH], റിസിനോലെയിക് അമ്ലം [CH3(CH2)5 CH (OH) CH2CH = CH(CH2)7COOH] എന്നിവ. ലാക്റ്റിക് അമ്ലമാണ് ഇവയില് പ്രമുഖം. കരിമ്പ്, തക്കാളി, മുന്തിരി എന്നിവയുടെ സത്തില് ഗ്ലൈക്കോളിക് അമ്ലം അടങ്ങിയിരിക്കുന്നു. ആവണക്കെണ്ണയിലെ ഒരു പ്രമുഖ അമ്ലമാണ് റിസിനോലെയിക് അമ്ലം.
ലാക്റ്റിക് അമ്ലം (CH3.CHOH.COOH). 1780ല് പാലില് നിന്ന് ഷീലെ വേര്തിരിച്ചെടുത്ത മഹൈഡ്രാക്സി പ്രാപ്പിയോണിക് അമ്ലമാണ് ലാക്റ്റിക് അമ്ലമെന്ന പേരില് അറിയപ്പെടുന്നത്. തൈര് (Sour milk), വെള്ളരിക്ക, ആമാശയരസം എന്നിവയിലെല്ലാം ഇത് കാണപ്പെടുന്നു. ജോലി ചെയ്യുമ്പോള് ശരീരപേശികളില് ലാക്റ്റിക് അമ്ലമുണ്ടാകുന്നു. കരിമ്പിന് പഞ്ചസാരയുടെയോ, ഗ്ലൂക്കോസിന്റെയോ ലായനിയെ പുളിപ്പിച്ച പാലില് അടങ്ങിയിരിക്കുന്ന ബാസില്ലസ് അസിഡി ലാക്റ്റിറ്റി എന്ന ബാക്റ്റീരിയ ഉപയോഗിച്ച് കിണ്വനം നടത്തിയാണ് വ്യാവസായികമായി ലാക്റ്റിക് അമ്ലം ഉത്പാദിപ്പിക്കുന്നത്.
നിറമില്ലാത്ത പുളിരസമുള്ള ഒരു കൊഴുത്ത ദ്രാവകമാണ് ലാക്റ്റിക് അമ്ലം. ഉരുകല്നില 18ºC. ജലത്തില് വളരെയധികം ലയിക്കുന്നു. ലാക്റ്റിക് അമ്ലം ധ്രുവണ ഘൂര്ണകത (optical activity) പ്രദര്ശിപ്പിക്കുന്നു. ഇതിന്റെ അടിസ്ഥാനത്തില് റഹലാക്റ്റിക് അമ്ലം, റലാക്റ്റിക് അമ്ലം, ഹലാക്റ്റിക് അമ്ലം എന്നിങ്ങനെ മൂന്ന് വ്യത്യസ്ത രൂപങ്ങള് ലാക്റ്റിക് അമ്ലത്തിനുണ്ട്. തൈരില് നിന്നു ലഭിക്കുന്നത് റഹലാക്റ്റിക് അമ്ലമാണ്. പേശികളില് ഗ്ലൈക്കോജന്റെ വിഘടനം മൂലമുണ്ടാകുന്നത് റലാക്റ്റിക് അമ്ലം അഥവാ സാക്രാലാക്റ്റിക് അമ്ലമാണ്. സൂക്രാസിനെ കിണ്വനം ചെയ്യുമ്പോള് ലഭിക്കുന്നത് l- ലാക്റ്റിക് അമ്ലമാണ്.
ഫെന്റണിന്റെ അഭികാരകത്താല് (Fenton's Reagent - FeSO4+ H2O2) ഓക്സീകരിക്കപ്പെട്ട് ലാക്റ്റിക് അമ്ലം പൈറൂവിക് അമ്ലം ഉത്പാദിപ്പിക്കുന്നു.
നേര്പ്പിച്ച സള്ഫ്യൂരിക് അമ്ലവുമായി തപിപ്പിക്കുമ്പോള്, ലാക്റ്റിക് അമ്ലം അസറ്റാല്ഡിഹൈഡും ഫോര്മിക് അമ്ലവുമായി മാറുന്നു.
തുകല് ഉറയ്ക്കിടുമ്പോള് (tanning) തുകലില് നിന്നും ചുണ്ണാമ്പ് നീക്കം ചെയ്യുവാനായി ലാക്റ്റിക് അമ്ലം ഉപയോഗിക്കുന്നു. ലഘുപാനീയങ്ങളില് രുചിവര്ദ്ധകമായും ബേബിഫുഡുകളിലും വിവിധ ലാക്റ്റേറ്റുകളുടെ നിര്മാണത്തിലും ഉപയോഗിക്കുന്നു. കാല്സ്യം ലാക്റ്റേറ്റ്, കാല്സ്യം അപര്യാപ്തത പരിഹരിക്കുവാഌം ആന്റിമണി ലാക്റ്റേറ്റ് കമ്പിളി ചായം മുക്കുന്നതിലും സില്വര് ലാക്റ്റേറ്റ് അണുനാശകമായും ഉപയോഗിക്കുന്നു.
മോണോഹൈഡ്രാക്സി അമ്ലങ്ങള്
മോണോ കാര്ബോക്സിലിക് അമ്ലങ്ങളിലെ ഒരു ആല്ക്കൈല് ഹൈഡ്രജന് ഒരു ഹൈഡ്രാക്സില് ഗ്രൂപ്പുകൊണ്ട് പ്രതിസ്ഥാപിച്ചുണ്ടാകുന്നവയാണിവ. പ്രകൃതിയില് കാണപ്പെടുന്ന മോണോ ഹൈഡ്രാക്സി അമ്ലങ്ങളാണ് ഗ്ലൈക്കോളിക് അമ്ലം (HO.CH2.COOH), ലാക്റ്റിക് അമ്ലം [CH3 CH (OH) COOH], റിസിനോലെയിക് അമ്ലം [CH3(CH2)5 CH (OH) CH2CH = CH(CH2)7COOH] എന്നിവ. ലാക്റ്റിക് അമ്ലമാണ് ഇവയില് പ്രമുഖം. കരിമ്പ്, തക്കാളി, മുന്തിരി എന്നിവയുടെ സത്തില് ഗ്ലൈക്കോളിക് അമ്ലം അടങ്ങിയിരിക്കുന്നു. ആവണക്കെണ്ണയിലെ ഒരു പ്രമുഖ അമ്ലമാണ് റിസിനോലെയിക് അമ്ലം.
ഹൈഡ്രാക്സി പോളികാര്ബോക്സിലിക്
ഒന്നോ അതിലധികമോ ഹൈഡ്രാക്സില് ഗ്രൂപ്പുകളും രണ്ടോ അതിലധികമോ കാര്ബോക്സില് ഗ്രൂപ്പുകളും അടങ്ങിയിട്ടുള്ള അമ്ലങ്ങളാണിവ. ഇവയില് മുഖ്യമായവ മാലിക് അമ്ലം, ടാര്ടാറിക്അമ്ലം, സിട്രിക് അമ്ലം എന്നിവയാണ്.
മാലിക് അമ്ലം [HOOC.CH(OH).CH2.COOH]. പാകമാവാത്ത മുന്തിരി, ആപ്പിള്, ബെറി എന്നിവയിലെല്ലാം ഇതടങ്ങിയിരിക്കുന്നു. 1785ല് ഷീലേ, ആപ്പിളില്നിന്നുമാണ് ആദ്യമായി മാലിക് അമ്ലം വേര്തിരിച്ചെടുത്തത്. മ അമിനോ സക്സിനിക് അമ്ലം (അസ്പാര്ട്ടിക് അമ്ലം) നൈട്രസ് അമ്ലവുമായി പ്രതിപ്രവര്ത്തിപ്പിച്ച് മാലിക് അമ്ലം നിര്മിക്കാം.
CH(NH2).COOH +HNO2 CH(OH).COOH +N2 +H2O
CH2. COOH CH2. COOH
നിറമില്ലാത്ത പരലുകളായി കാണപ്പെടുന്ന ഇവ ജലത്തിലും ആല്ക്കഹോളിലും ലേയമാണ്. ധ്രുവണ ഘൂര്ണകത പ്രദര്ശിപ്പിക്കുന്ന ഇവ d, l, dl (റെസിമിക്) രൂപങ്ങളില് സ്ഥിതിചെയ്യുന്നു. പ്രകൃതിയില് കാണപ്പെടുന്നത് ഹമാലിക് അമ്ലമാണ്. റടാര്ടാറിക് അമ്ലത്തെ ഹൈഡ്രാ അയഡിക് അമ്ലം കൊണ്ടു നിരോക്സീകരിക്കുമ്പോള് ലഭിക്കുന്നത് റമാലിക് അമ്ലമാണ്. d, l രൂപങ്ങളുടെ ഉരുകല് നില 100ºC ഉം മാലിക് അമ്ലത്തിന്റേത് 135ºC ഉം ആണ്.
രാസപരമായി മാലിക് അമ്ലം ഒരു ദ്വിതീയ ആല്ക്കഹോളായും ദ്വിക്ഷാരക അമ്ലമായും പെരുമാറുന്നു. 150-180ºC താപനിലയില് മാലിക് അമ്ലം തപിപ്പിച്ചാല്, മലിയിക് അന്ഹൈഡ്രഡിന്റെയും ഫ്യൂമാറിക് അമ്ലത്തിന്റെയും ഒരു മിശ്രിതം ലഭിക്കുന്നു.
H C CO O CH(OH).COOH H C COOH
H C CO CH2. COOH HOOC C H
ഫോസ്ഫറസ് പെന്റാക്ലോറൈഡുമായുള്ള പ്രതിപ്രവര്ത്തനം വഴി റമാലിക് അമ്ലത്തില്നിന്ന് ഹക്ലോറോസക്സിനിക് അമ്ലവും ഹമാലിക് അമ്ലത്തില്നിന്ന് റക്ലോറോ സക്സിനിക് അമ്ലവും ലഭിക്കുന്നു. ഇപ്രകാരം ലഭിച്ച ക്ലോറോസക്സിനിക് അമ്ലങ്ങളുമായി പൊട്ടാസ്യം ഹൈഡ്രാക്സൈഡ് പ്രതിപ്രവര്ത്തിക്കുമ്പോള് വിപരീതദിശയില് പ്രതിപ്രവര്ത്തനം നടക്കുന്നു.
l-മാലിക് അമ്ലം l-ക്ലോറോ സക്സിനിക് അമ്ലം d-മാലിക് അമ്ലം d-ക്ലോറോ സക്സിനിക് അമ്ലം
എന്നാല് ക്ലോറോ സക്സിനിക് അമ്ലങ്ങള് സില്വര് ഹൈഡ്രാക്സൈഡു (AgOH) മായി പ്രതിപ്രവര്ത്തിക്കുമ്പോള് ഇപ്രകാരം സംഭവിക്കുന്നില്ല.
l-ക്ലോറോ സക്സിനിക് അമ്ലം l-മാലിക് അമ്ലം d-ക്ലോറോ സക്സിനിക് അമ്ലം d-മാലിക് അമ്ലം
പ്രസ്തുത പ്രതിഭാസം വാല്ഡന് പ്രതിലോമനം (Walden Inversion) എന്ന പേരില് അറിയപ്പെടുന്നു.
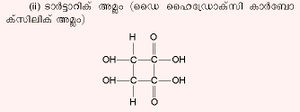
പാനീയങ്ങളില് സിട്രിക് അമ്ലത്തിനുപകരമായും വിരേചകമായും തൊണ്ടവേദനയ്ക്കുള്ള മരുന്നായും മാലിക് അമ്ലം ഉപയോഗിക്കുന്നു. ടാര്ടാറിക് അമ്ലം . രണ്ട് അസമമിത കാര്ബണ് ആറ്റങ്ങള് അടങ്ങിയതിനാല്, ടാര്ടാറിക് അമ്ലം d, l, dl, മീസോ എന്നിങ്ങനെ നാല് ഐസോമറുകളായി കാണപ്പെടുന്നു. പ്രകൃത്യാ കാണപ്പെടുന്ന ടാര്ടാറിക് അമ്ലം ഡെക്സ്ട്രാ (d) ഐസോമറാണ്. പുളിയില് സ്വതന്ത്രാവസ്ഥയിലും മുന്തിരി, പ്ലം, ബെറി എന്നിവയില് പൊട്ടാസ്യം അമ്ലലവണമായും d ടാര്ടാറിക് അമ്ലം കാണപ്പെടുന്നു. മുന്തിരിസത്തിനെ കിണ്വനം ചെയ്യുമ്പോള് അവക്ഷേപിക്കപ്പെടുന്ന തവിട്ടുനിറത്തിലുള്ള ഖരവസ്തുവായ അര്ഗോളില്നിന്ന് d ടാര്ടാറിക് അമ്ലം വേര്തിരിച്ചെടുക്കാം. ഗ്ലയോക്സാല് സയനോഹൈഡ്രിനെ ജലാപഘടനത്തിനുവിധേയമാക്കിയും ഫ്യുമേറിക് അമ്ലത്തെ ആല്ക്കലൈന് പൊട്ടാസ്യം പെര്മാംഗനേറ്റുപയോഗിച്ച് ഓക്സീകരിച്ചും dl ടാര്ടാറിക് അമ്ലം നിര്മിക്കാം.
CHO CH(OH).CN CH(OH).COOH CHO CH(OH).CN CH(OH).COOH H C COOH +H2O+O CH(OH).COOH HOOC C H CH(OH).COOH
ടാര്ടാറിക് അമ്ലം ഐസോമറുകളുടെ ഭൗതികഗുണങ്ങള് പട്ടികയില് കൊടുത്തിരിക്കുന്നു.
ടാര്ടാറിക് അമ്ലം d l മീസോ dl(റെസിമിക്) ഉരുകല് നില 167170º 167170º 140º 205 206º ധ്രുവണഘൂര്ണനം +12 12 0 0
ക്രിസ്റ്റല്രൂപം പ്രിസം പ്രിസം പാളി റോംബിക് രാസപരമായി ടാര്ടാറിക് ഡൈകാര്ബോക്സിലിക് അമ്ലത്തിന്റെയും ദ്വിതീയ ആല്ക്കഹോളിന്റെയും സ്വഭാവഗുണങ്ങള് പ്രകടമാക്കുന്നു. ഇവ അമ്ലലവണങ്ങളും നോര്മല് ലവണങ്ങളും ഉത്പാദിപ്പിക്കുന്നു. ടാര്ടാറിക് അമ്ലത്തിന്റെ പ്രധാനപ്പെട്ട ഒരു നോര്മല് ലവണമാണ് സോഡിയം പൊട്ടാസ്യം ടാര്ടറേറ്റ് . റോഷല്ലെ ലവണം (Rochelle Salt)എന്ന പേരില് ഇതറിയപ്പെടുന്നു.
ഹൈഡ്രജന് അയഡൈഡിനാല് നിരോക്സീകരിക്കപ്പെട്ട് ടാര്ടാറിക് അമ്ലം, മാലിക് അമ്ലവും സക്സിനിക് അമ്ലവും തരുന്നു.
CH(OH).COOH +2HI CH(OH).COOH CH2.COOH CH(OH).COOH CH2.COOH CH2.COOH
ശക്തികുറഞ്ഞ ഓക്സീകാരകങ്ങളാല് ഓക്സീകരിക്കപ്പെട്ട് ടാര്ടാറിക് അമ്ലം ടാര്ട്രാണിക് അമ്ലം ഉത്പാദിപ്പിക്കുന്നു. എന്നാല് ശക്തിയേറിയ ഓക്സീകാരകങ്ങള് ടാര്ടാറിക് അമ്ലത്തെ ഓക്സാലിക് അമ്ലമാക്കി മാറ്റുന്നു.
CH(OH).COOH CH(OH).COOH COOH CH(OH).COOH COOH COOH
നുരഞ്ഞുപതയുന്ന പാനീയങ്ങളില് ടാര്ടാറിക് അമ്ലം ഉപയോഗിക്കുന്നു. റോഷല്ലെ ലവണം (C4H4O6KNa.4H2) കണ്ണാടി നിര്മാണത്തിലും ഫെലിംഗ്സ് ലായനി നിര്മാണത്തിലും ഉപയോഗിക്കുന്നു. പൊട്ടാസ്യം ആന്റിമണൈല് ടാര്ടറേറ്റ് [2C4H4O6K(SbO)H2O] ഔഷധമായും ചായം മുക്കുന്നതില് മോര്ഡന്റായും കാലിക്കോ പ്രിന്റിങിലും ഉപയോഗിക്കുന്നു. സിട്രിക് അമ്ലം (HOOC.CH2.C(OH).COOH.CH2COOH). ഓറഞ്ച്, ചെറുനാരങ്ങ, തക്കാളി എന്നിവയില് കാണപ്പെടുന്ന ഒരു ട്രകാര്ബോക്സിലിക് അമ്ലമാണിത്. ചെറുനാരങ്ങാസത്തിനെ കാത്സ്യം സിട്രറ്റ് ചേര്ത്ത് ചൂടാക്കുമ്പോള് അലേയമായ കാത്സ്യം സിട്രറ്റ് അവക്ഷിപ്തപ്പെടും. അരിച്ചെടുത്തശേഷം നേര്പ്പിച്ച സള്ഫ്യൂറിക് അമ്ലം ചേര്ക്കുന്നു. അവക്ഷിപ്തപ്പെടുന്ന കാത്സ്യം സള്ഫേറ്റ് അരിച്ചുമാറ്റുമ്പോള് ലഭിക്കുന്ന കൊഴുത്ത ലായനിയെ ക്രിസ്റ്റലീകരിക്കുമ്പോള് സിട്രിക് അമ്ലത്തിന്റെ മോണോഹൈഡ്രറ്റ് പരലുകള് ലഭിക്കും.
ജലത്തിലും ആല്ക്കഹോളിലും ലയിക്കുന്ന ഇവ, മോണോഹൈഡ്രറ്റ് പരലുകളായും അന്ഹൈഡ്രറ്റ് പരലുകളായും കാണപ്പെടുന്നു. അന്ഹൈഡ്രറ്റ് പരലുകളുടെ ഉരുകല്നില 153ºC. മോണോ ഹൈഡ്രറ്റ് പരലുകളുടെ ഉരുകല്നില 101ºC. ധ്രുവണഘൂര്ണകത പ്രദര്ശിപ്പിക്കുന്നില്ല. സിട്രിക് അമ്ലം ഒരു ത്രിബേസിക അമ്ലത്തിന്റെയും ആല്ക്കഹോളിന്റെയും ഗുണങ്ങള് പ്രകടിപ്പിക്കുന്നു. സിട്രിക് അമ്ലം മൂന്നുശ്രണി ലവണങ്ങള് ഉത്പാദിപ്പിക്കുന്നു. ഉദാ.
CH2.COONa CH2.COONa CH2.COONa C(OH).COOH C(OH).COOH C(OH).COONa CH2.COOH CH2.COONa CH2.COONa
ഹൈഡ്രജന് അയഡൈഡുകൊണ്ട് നിരോക്സീകരിക്കുമ്പോള് ട്രകാര്ബലൈലിക് അമ്ലം ലഭിക്കുന്നു.
CH2.COOH CH2 COOH C(OH).COOH + 2HI š CH COOH + H2O + I2 CH2.COOH CH2 COOH
150ºC വരെ ചൂടാക്കിയാല് സിട്രിക് അമ്ലം നിര്ജലീകരിക്കപ്പെട്ട് അപൂരിത അമ്ലമായ അകോണിറ്റിക് അമ്ലമാക്കി മാറുന്നു.
H2COOH CH COOH C(OH)COOH CCOOH + H2O CH2COOH CH2 COOH
പാനീയങ്ങള് നിര്മിക്കുവാന് സിട്രിക് അമ്ലം ഉപയോഗിക്കുന്നു. ചായം മുക്കുന്നതില് മോര്ഡന്റായും പ്രിന്റിങ്ങിലും ഉപയോഗിക്കാറുണ്ട്. മഗ്നീഷ്യം സിട്രറ്റ് വിരേചകമായി പ്രയോജനപ്പെടുത്തുന്നു. ഫെറിക് അമോണിയം സിട്രറ്റ് ബ്ലൂപ്രിന്റുകള് നിര്മിക്കുന്നതിഌം ഔഷധമായും ഉപയോഗിക്കുന്നു. സോഡിയം സിട്രറ്റ് ബെനഡിക്റ്റ്സ് ലായനി (Benedict's solution) ഉണ്ടാക്കുന്നതിനുപയോഗിച്ചുവരുന്നു. നോ. കൊഴുപ്പ്, കൊഴുപ്പമ്ലങ്ങള്
(ചുനക്കര ഗോപാലകൃഷ്ണന്)