This site is not complete. The work to converting the volumes of സര്വ്വവിജ്ഞാനകോശം is on progress. Please bear with us
Please contact webmastersiep@yahoo.com for any queries regarding this website.
Reading Problems? see Enabling Malayalam
ഇന്ധനങ്ങള്
സര്വ്വവിജ്ഞാനകോശം സംരംഭത്തില് നിന്ന്
Mksol (സംവാദം | സംഭാവനകള്) (→ഇന്ധന ഘടകങ്ങള്) |
Mksol (സംവാദം | സംഭാവനകള്) (→ഖര ഇന്ധനങ്ങള്) |
||
| വരി 21: | വരി 21: | ||
==ഖര ഇന്ധനങ്ങള് == | ==ഖര ഇന്ധനങ്ങള് == | ||
| - | ഖര ഇന്ധനങ്ങളെ പ്രകൃതിദത്തമെന്നും | + | ഖര ഇന്ധനങ്ങളെ പ്രകൃതിദത്തമെന്നും നിര്മിതമെന്നും രണ്ടായി തിരിക്കാം. ആദ്യത്തേതില് ജൈവപദാര്ഥങ്ങള്, വിറക്, പീറ്റ്, കല്ക്കരി മുതലായവയും രണ്ടാമത്തേതില് ഭഞ്ജകസ്വേദനം (destructive distillation) വഴി ലഭിക്കുന്ന കോക്ക്, മരക്കരി എന്നിവയും ഉള്പ്പെടുന്നു. വായുരഹിതമായ അടച്ച പാത്രത്തില് പദാര്ഥങ്ങളെ താപശക്തികൊണ്ട് സ്വേദനംചെയ്യുന്ന പ്രക്രിയയെയാണ് ഭഞ്ജകസ്വേദനം എന്നു പറയുന്നത്. ലോഹകര്മീയകോക്കും (metallurgical coke)വാതകകോക്കും (gas coke) ഉണ്ടാക്കുവാന് ഈ പ്രക്രിയയാണ് പ്രയോജനപ്പെടുത്തുന്നത്. |
[[ചിത്രം:Vol3_138_chart.jpg|thumb|]] | [[ചിത്രം:Vol3_138_chart.jpg|thumb|]] | ||
| - | === | + | === കല്ക്കരിയും ബന്ധപ്പെട്ട ഇന്ധനങ്ങളും === |
| - | യുഗങ്ങള്ക്കുമുമ്പ് അടിഞ്ഞുകൂടിയ | + | യുഗങ്ങള്ക്കുമുമ്പ് അടിഞ്ഞുകൂടിയ സസ്യപദാര്ഥങ്ങളിലും മറ്റ് സെല്ലുലോസ് പദാര്ഥങ്ങളിലും ചൂടിന്റെയും മര്ദത്തിന്റെയും ജീവാണുക്കളുടെയും സഹായത്താല് ഉരുത്തിരിയുന്ന കാര്ബണിക പദാര്ഥങ്ങളുടെ അട്ടികളാണ് കല്ക്കരി. ഘടനയും ഗുണവും അനുസരിച്ച് അവ പലതരത്തില് കാണപ്പെടുന്നു. ഏകദേശം 1,000-ത്തിലധികം വര്ഷത്തേക്കുള്ള കല്ക്കരിശേഖരം ഭൂമുഖത്ത് അവശേഷിച്ചിട്ടുള്ളതായി കണക്കാക്കപ്പെട്ടിരിക്കുന്നു. |
| - | ==== | + | ==== വര്ഗീകരണം==== |
| - | രാസയോഗം, വ്യാവസായികോപയോഗം, | + | രാസയോഗം, വ്യാവസായികോപയോഗം, കോക്കല് സ്വഭാവം (coking properties), ജിയോളജീയ വയസ് (geological age) എന്നിവയെ അടിസ്ഥാനമാക്കി കല്ക്കരിയെ വര്ഗീകരിക്കാവുന്നതാണ്. ഇനങ്ങള്ക്ക് സ്പഷ്ടമായ വ്യത്യാസങ്ങള് ഇല്ലെങ്കിലും വിഭിന്ന സ്വഭാവവിശേഷങ്ങളുള്ള ഘടകങ്ങളടങ്ങിയ ഒരു കുടുംബമായി കല്ക്കരിയെ കണക്കാക്കാം. ഏതിനം കല്ക്കരിയുടെയും നിലവാരം നിര്ണയിക്കുന്നത് അതിന്റെ രൂപാന്തരീകരണ പ്രക്രിയയെ അടിസ്ഥാനമാക്കിയാണ്. കല്ക്കരി രൂപാന്തരീകരണപ്രക്രിയ പീറ്റ് →ലിഗ്നൈറ്റ് → ബിറ്റ്യൂമിനീയ കല്ക്കരി → ആന്ഥ്റസൈറ്റ് → ഗ്രാഫൈറ്റ് എന്ന ക്രമത്തിലാണ്. മേല്പറഞ്ഞ ഓരോ ഇനത്തിനും വ്യക്തമായ ഭൗതികവും രാസപരവുമായ സവിശേഷതകള് ഉണ്ടെങ്കിലും അവയുടെ അതിര്ത്തിരേഖകള് തുലോം ലോലമാണ്. |
| - | അമേരിക്കന് | + | അമേരിക്കന് സ്റ്റാന്ഡേര്ഡ് അസോസിയേഷന് (American Standard Association)കല്ക്കരിയെ നാല് ഇനങ്ങളായി തിരിച്ചിരിക്കുന്നു: ആന്ഥ്റസൈറ്റ്, ബിറ്റ്യൂമിനീയ കല്ക്കരി, സബ്-ബിറ്റ്യൂമിനീയ കല്ക്കരി, ലിഗ്നൈറ്റും തവിട്ടു കല്ക്കരിയും. മുകളില് കൊടുത്തിരിക്കുന്ന പട്ടിക, കാര്ബണിന്റെ വര്ധനവും ഓക്സിജന്റെ ലോപവും അനുസരിച്ച് സെല്ലുലോസില്നിന്ന് ആന്ഥ്റസൈറ്റിലേക്കുള്ള അവസ്ഥാന്തരം കാണിക്കുന്നു. |
| - | + | ||
| - | + | ||
| - | + | കല്ക്കരിയുടെ നിലവാരം നിര്ണയിക്കുന്നതില് ജലാംശത്തിന്റെ അളവിനോ അന്യഖനിജങ്ങളുടെ സാന്നിധ്യത്തിനോ ഒരു പ്രാധാന്യവുമില്ല. ഈ വസ്തുത കണ്ടെത്തിയ എസ്.ഡബ്ല്യു. പാര് ഖനിജപദാര്ഥരഹിതവും ജലാംശമുക്തവുമായ അവസ്ഥയിലുള്ള താപമൂല്യമനുസരിച്ച് കല്ക്കരിയെ വര്ഗീകരിച്ചു. ഇതനുസരിച്ച് ബാഷ്പശീലമുള്ള പദാര്ഥങ്ങളും (volatile matter) സ്ഥിര കാര്ബണും (fixed carbon) ആണ് കല്ക്കരിയുടെ പ്രധാന ഘടകങ്ങള്. ബാഷ്പശീലമുള്ള പദാര്ഥങ്ങളുടെ ശതമാനം, "യഥാര്ഥ' കല്ക്കരിയുടെ താപമൂല്യം എന്നിവയുടെ താരതമ്യപഠനം പാര് വര്ഗീകരണത്തിലൂടെ മനസ്സിലാക്കാം. | |
| + | |||
| + | ഈ വര്ഗീകരണമനുസരിച്ച് കല്ക്കരിയെ താഴെപ്പറയുന്ന വിഭാഗങ്ങളായി തിരിച്ചിരിക്കുന്നു: ആന്ഥ്റസൈറ്റ്, സെമി-ആന്ഥ്റസൈറ്റ്, ബിറ്റ്യൂമിനീയം-A, ബിറ്റ്യൂമിനീയം-B, ബിറ്റ്യൂമിനീയം-C, ബിറ്റ്യൂമിനീയം-D, ലിഗ്നൈറ്റ്, പീറ്റ്. | ||
| - | + | സി.എ. സേയ്ലറുടെയാണ് മറ്റൊരു വര്ഗീകരണം: ഇതില് ഹൈഡ്രജന്റെ അളവനുസരിച്ച് അഞ്ചു ഗ്രൂപ്പുകളായി തരംതിരിക്കുകയും വീണ്ടും അവയെ കാര്ബണിന്റെ അളവനുസരിച്ച് ഉപഗ്രൂപ്പുകളായി വിഭജിക്കുകയും ചെയ്തിരിക്കുന്നു. | |
| - | + | ||
| - | + | ||
| - | + | ||
| - | + | ||
| - | + | ||
| - | + | ||
| - | + | ||
| - | + | ||
| - | + | ||
| - | + | ||
| - | + | ||
| - | + | ||
| - | + | ||
| - | + | ||
| - | + | ||
| - | + | ||
| - | + | ||
| - | + | ==== കാര്ബണിക പദാര്ഥങ്ങള്ക്കുള്ള പരീക്ഷണങ്ങള്==== | |
| + | കല്ക്കരി, കോക്ക് മുതലായ കാര്ബണിക പദാര്ഥങ്ങളുടെ വാണിജ്യമൂല്യത്തെയും ദഹനഗുണങ്ങളെയും പ്രത്യേകാവശ്യങ്ങള്ക്കുള്ള അവയുടെ അനുയോജ്യതയെയും ബന്ധപ്പെടുത്തിയുള്ള അപഗ്രഥനപരീക്ഷണങ്ങള് ആവിഷ്കരിക്കപ്പെട്ടിട്ടുണ്ട്. ഇവയില് പല പരീക്ഷണങ്ങളും രാസവിശ്ലേഷണങ്ങള് അല്ല; അവ അടിസ്ഥാന ഭൗതിക സ്ഥിരാങ്കങ്ങളും (physical constants)തരുന്നില്ല. പദാര്ഥങ്ങളുടെ സ്വഭാവഗുണങ്ങള് പരിശോധിക്കുന്നതിനുള്ള അമേരിക്കന് സൊസൈറ്റി (American Society for Testing Materials-ASTM) കല്ക്കരിയും കോക്കും പ്രതിചയിക്കുന്നതിനും (sampling) പരീക്ഷിക്കുന്നതിനും നിഷ്കൃഷ്ടവും വിശദവുമായ ഉപകരണങ്ങളും നടപടിക്രമങ്ങളും ആവിഷ്കരിച്ചിട്ടുണ്ട്. | ||
| - | + | പദാര്ഥത്തിലെ സ്വതന്ത്രജലാംശം (free moisture)വായു ഉപയോഗിച്ച് ഉണക്കി കണ്ടുപിടിക്കാം; അതിനുശേഷം പദാര്ഥത്തെ പൊടിച്ച് 60-മെഷ് (Mesh) അരിപ്പയിലൂടെ അരിച്ച് വായുനിബദ്ധമായ അറകളില് സൂക്ഷിച്ച് പരീക്ഷണങ്ങള്ക്കുപയോഗിക്കുന്നു. വ്യത്യസ്ത രീതിയിലുള്ള പരീക്ഷണങ്ങള് വിഭിന്നങ്ങളായ ഫലങ്ങള് തരുന്നതിനാല് ഒരേ രീതിതന്നെ എല്ലാവരും ഉപയോഗിക്കേണ്ടതുണ്ട്. പരക്കെ ഉപയോഗിക്കുന്ന പരീക്ഷണ രീതികള് നാലാണ്: ഏകദേശവിശ്ലേഷണം (Approximate analysis), മൂലക വിശ്ലേഷണം(ultimate analysis), കേക്കിങ് സൂചകം (caking index), കലോറികമൂല്യം (caking index). ചൂടാക്കുന്നതിനും നീരാവിയുത്പാദിപ്പിക്കുന്നതിനും മറ്റും ഉപയോഗിക്കുന്ന ഇന്ധനങ്ങള് ചൂടാക്കുമ്പോഴോ ജ്വലിക്കുമ്പോഴോ ഉള്ള അവയുടെ പ്രവര്ത്തനരീതിയുമായി ബന്ധപ്പെട്ട മൂല്യം കണക്കാക്കുന്ന ലളിതവും സത്വരവും ആയ പരീക്ഷണം ആവിഷ്കരിക്കപ്പെട്ടിട്ടുണ്ട്. ഏകദേശവിശ്ലേഷണത്തില് ജലാംശം, ചാരം, ബാഷ്പശീലമുള്ള പദാര്ഥം (volatile matter), സ്ഥിരകാര്ബണ് (fixed carbon) എന്നിവയുടെ അളവ് നിര്ണയിക്കപ്പെടുന്നു. 60-മെഷ് അരിപ്പയിലൂടെ കടക്കുന്ന കല്ക്കരിപ്പൊടിയാണിതിന് ഉപയോഗിക്കുന്നത്. | |
| - | c. | + | a. ജലാംശം. ഒന്നോരണ്ടോ ഗ്രാം കല്ക്കരി ഒരു മണിക്കൂര് നേരത്തേക്ക് 105-110°C ഊഷ്മാവില് ചൂടാക്കുമ്പോള് നഷ്ടപ്പെടുന്ന ഭാരമായിരിക്കും അതിലുണ്ടായിരുന്ന ജലാംശം. ഓക്സീകരണപ്രക്രിയയ്ക്ക് വിധേയമാകാന് സാധ്യതയുള്ളതുകൊണ്ട് നിഷ്ക്രിയവാതകമായ നൈട്രജന്റെ സാന്നിധ്യത്തിലാണ് ചൂടാക്കേണ്ടത്. |
| + | |||
| + | b. ചാരം. ഒന്നോരണ്ടോ ഗ്രാം കല്ക്കരി പ്ലാറ്റിനമോ സിലിക്കയോ കൊണ്ടുള്ള പാത്രത്തില് ക്രമമായി 800°C വരെ ചൂടാക്കുക. ദഹനം പരിപൂര്ണമാവുമ്പോഴുള്ള അവശിഷ്ടം തണുപ്പിച്ച് കിട്ടുന്ന ഭാരം ചാരത്തിന്റെ ഭാരമായിരിക്കും. | ||
| + | |||
| + | c. ബാഷ്പശീലമുള്ള പദാര്ഥങ്ങള്. ഒരുഗ്രാം കല്ക്കരി പ്രത്യേക വിധത്തില് അടച്ച പാത്രത്തില് 7 മിനിട്ട് നേരം 925°C-ല് ചൂടാക്കുമ്പോള് നഷ്ടപ്പെടുന്ന ഭാരം ബാഷ്പശീലമുള്ള പദാര്ഥത്തിന്റെ ഭാരമായിരിക്കും. | ||
| + | |||
| + | d. സ്ഥിരകാര്ബണ്. ആകെ ഭാര(100%)ത്തില് നിന്ന് ചാരം, ബാഷ്പശീലമുള്ള പദാര്ഥം, ജലാംശം എന്നിവയുടെ ഭാരശതമാനം കുറച്ചാല് സ്ഥിരകാര്ബണിന്റെ ഭാരശതമാനം ലഭിക്കും. | ||
| + | |||
| + | e. മൂലകവിശ്ലേഷണം. ഉയര്ന്നതോതില് കല്ക്കരി ഉപയോഗിക്കുന്നവര്ക്ക് വിവിധയിനം കല്ക്കരികളെക്കുറിച്ചുള്ള കൂടുതല് വിവരം ആവശ്യമായതുകൊണ്ട് മുന്വിവരിച്ചവയില്നിന്ന് വ്യത്യസ്തമായ പരീക്ഷണം ആവശ്യമായി വന്നു. അതുകൊണ്ട് കാര്ബണ്, ഹൈഡ്രജന്, ഓക്സിജന്, നൈട്രജന്, ഗന്ധകം എന്നീ മൂലകങ്ങളും ചാരവും അടിസ്ഥാനമാക്കിയുള്ള രാസവിശ്ലേഷണം നിലവില്വന്നു. | ||
| + | |||
| + | കാര്ബണിന്റെയും ഹൈഡ്രജന്റെയും അളവ് നിശ്ചയിക്കുന്നതിന് 0.2 ഗ്രാം കല്ക്കരി ഓക്സിജന്റെ സാന്നിധ്യത്തില് കത്തിക്കുന്നു. ദഹനോത്പന്നങ്ങള് 800°C ഉള്ള കോപ്പര്ഓക്സൈഡില്ക്കൂടിയും പിന്നീട് 600°C ഉള്ള ലെഡ്ക്രോമേറ്റില്ക്കൂടിയും കടത്തിവിട്ട് സള്ഫര്സംയുക്തങ്ങളെ ആഗിരണം ചെയ്യുന്നു. ഈ പ്രക്രിയയില് ഉത്പാദിപ്പിക്കപ്പെടുന്ന കാര്ബണ്ഡൈഓക്സൈഡിന്റെയും, ജലത്തിന്റെയും ഭാരം വെവ്വേറെ കാണാവുന്നതാണ്. ഇതില്നിന്നും കല്ക്കരിയിലുള്ള കാര്ബണിന്റെയും ഹൈഡ്രജന്റെയും ഭാരശതമാനം കണ്ടുപിടിക്കാം. | ||
| + | |||
| + | ഒരുഗ്രാം കല്ക്കരി സള്ഫ്യൂറിക് അമ്ലവുമായി പ്രതിപ്രവര്ത്തിപ്പിച്ച് നൈട്രജന്റെ ഭാരം കണക്കാക്കാം. ഇതിനെ ക്യെല്ഡാല് (kjeldahl)പദ്ധതിയെന്നു പറയുന്നു. ഈ പദ്ധതിയില് കല്ക്കരിയിലുള്ള നൈട്രജന് അമോണിയയായി രൂപാന്തരപ്പെടുന്നു. ഇതിനെ സ്വേദന(distillation)ത്തിനും ഒരു പ്രമാണ (standard) ലായനിയുമായി അനുമാപനത്തിനും വിധേയമാക്കി നൈട്രജന്റെ ഭാരം കണ്ടുപിടിക്കാം. | ||
| + | |||
| + | കല്ക്കരിയെ ചുണ്ണാമ്പും മഗ്നീഷ്യംഓക്സൈഡും ചേര്ന്ന ഉരുകല്മിശ്രവുമായി ചേര്ത്ത് ചൂടാക്കുമ്പോള് സള്ഫറിനെ സള്ഫേറ്റാക്കി രൂപാന്തരപ്പെടുത്തുന്നതിലൂടെ സള്ഫറിന്റെ ഭാരം കണ്ടുപിടിക്കാം. ഇതിനെ ഏഷാക്കാ (eschakas) പദ്ധതിയെന്നു പറയാം. | ||
| + | |||
| + | f. കേക്കിങ് സൂചകം (Caking Index). ചിലതരം കല്ക്കരി ചൂടാക്കുമ്പോള് ഉരുകി കട്ടകളാകുന്നു; ഇത് സ്റ്റോക്കറിന്റെ (stoker) പ്രവര്ത്തനത്തെ തടയും. (ഇന്ധനം ക്രമമായി കൊടുത്ത് ദഹനം നടത്താനുള്ള സംവിധാനത്തെയാണ് സ്റ്റോക്കര് എന്നു പറയുന്നത്.) കല്ക്കരിയുടെ കട്ടപിടിക്കാനുള്ള പ്രവണത താഴെ പറയുന്ന പരീക്ഷണം വഴി നിര്ണയിക്കാം. | ||
| + | |||
| + | ചൂര്ണിതകല്ക്കരി സിലിക്കാക്രൂസിബിളില് വച്ച് പ്രത്യേകാവസ്ഥയില് ചൂടാക്കുമ്പോള് കോക്ക്ബട്ടണ് ഉണ്ടാകുന്നു. ഇതിന്റെ വലുപ്പം 1 മുതല് 9 വരെ അക്കങ്ങളില് അറിയപ്പെടുന്ന പ്രമാണ രൂപങ്ങളുമായി തിട്ടപ്പെടുത്തി ഏതു നമ്പര് ആണെന്നു തീരുമാനിക്കാം. കേക്കിങ്സൂചകം എന്നു പറയുന്നത് കോക്ക്ബട്ടന്റെ ഏറ്റവും കൂടിയ പരിച്ഛേദകവിസ്തീര്ണത്തോട് ബന്ധപ്പെട്ടിരിക്കുന്ന പ്രമാണപരിച്ഛേദകത്തിന്റെ അക്കമാണ്. | ||
| + | |||
| + | g. കലോറികമൂല്യം. ഇന്ധനം പ്രധാനമായി ഉപയോഗിക്കുന്നത് താപ-ഉത്പാദനത്തിന് ആയതിനാല് കലോറികമൂല്യനിര്ണയം വളരെ പ്രാധാന്യമര്ഹിക്കുന്നു. ഒരു ഏകകപിണ്ഡമുള്ള ഖര-ദ്രവ ഇന്ധനമോ, ഏകകവ്യാപ്തമുള്ള വാതകഇന്ധനമോ പരിപൂര്ണമായി ദഹിപ്പിച്ചതിനു ശേഷം അന്തരീക്ഷ ഊഷ്മാവിലേക്ക് തണുപ്പിച്ചാല് ലഭിക്കുന്ന താപത്തെയാണ് മൊത്തം കലോറികമൂല്യമെന്നു പറയുന്നത് (gross calorific value). | ||
| + | |||
| + | ഇപ്രകാരം കണക്കാക്കപ്പെടുന്ന കലോറികമൂല്യത്തില് ബാഷ്പം ദ്രവീകരിക്കപ്പെടുന്നതുകൊണ്ട് ജലത്തിന്റെ ബാഷ്പീകരണലീനതാപം (latent heat of vaporization) കൂടി അടങ്ങിയിരിക്കും. മൊത്തം കലോറികമൂല്യത്തില് നിന്ന് ബാഷ്പീകരണലീനതാപം കുറച്ചാല് അസല് കലോറികമൂല്യം (gross calorific value) ലഭിക്കുന്നു. | ||
| + | |||
| + | കലോറികമൂല്യം കൃത്യമായി നിര്ണയിക്കുന്നതിനുള്ള ഉപകരണമാണ് ബോംബ്കലോറിമീറ്റര്. ഒരു ഗ്രാം നേരിയ കല്ക്കരിപ്പൊടി ചെറിയ ഗുളികരൂപത്തിലാക്കി വായുനിബദ്ധമായ ഒരു ലോഹബോംബില് അടക്കം ചെയ്യുന്നു; 25 അന്തരീക്ഷമര്ദമുള്ള ഓക്സിജന് ബോംബില് നിറച്ചശേഷം, വെള്ളം നിറച്ച ഊഷ്മമാപി(calorimeter)യില് താഴ്ത്തുന്നു; വൈദ്യുതസ്ഫുലിംഗം ഉപയോഗിച്ച് ഇന്ധനം കത്തിക്കുന്നു. ദഹനപ്രക്രിയയില് ഉത്പാദിപ്പിക്കപ്പെടുന്ന താപം ഊഷ്മമാപിയിലെ ജലത്തിന്റെ താപവര്ധനവില്നിന്നു കണ്ടുപിടിക്കാം. വിവിധ ഇന്ധനങ്ങളുടെ കലോറികമൂല്യം അതിന്റെ തരമനുസരിച്ചും ജലാംശത്തിന്റെ തോതനുസരിച്ചും വ്യത്യാസപ്പെട്ടിരിക്കും. ഖര ഇന്ധനങ്ങളുടെ കലോറികമൂല്യം ഏകദേശം 3,000 മുതല് 15,000 വരെ BTU/റാത്തല് ആണ്. | ||
| + | ==== കല്ക്കരിയുടെ ഘടന==== | ||
| + | കല്ക്കരിയുടെ ഘടന (Constitution of Coal). ഏകദേശവിശ്ലേഷണവും മൂലകവിശ്ലേഷണവും കല്ക്കരിയുടെ രാസഘടനയെക്കുറിച്ച് വിവരങ്ങളൊന്നും തരുന്നില്ല; അതുകൊണ്ട് കല്ക്കരിയുടെ തന്മാത്രിക ഘടന (Molecular Structure) കണ്ടുപിടിക്കുന്നതിന് രാസഭൗതികക്രിയകള് ഉപയോഗപ്പെടുത്തിവരുന്നു. താഴെ പറയുന്ന പരീക്ഷണങ്ങളാണ് പ്രധാനമായി ഉപയോഗിക്കുന്നത്: | ||
| + | |||
| + | a. ലായകനിഷ്കര്ഷണം (Solvent Extraction). ഉന്നതമര്ദത്തില് ബെന്സീന് (Benzene) ഉപയോഗിച്ച് നിഷ്കര്ഷണം ചെയ്യുമ്പോള് കല്ക്കരിയെ കേക്കിങ് സ്വഭാവമുള്ളതാക്കുന്ന ഘടകങ്ങളെ വേര്തിരിച്ചെടുക്കാന് സാധിക്കുന്നു. | ||
| + | |||
| + | b. അഭികര്മക (Reagent) പ്രതിക്രിയ. നിയന്ത്രിത ഓക്സീകരണം, ഹൈഡ്രൊജനീകരണം (Hydrogenation), ക്ലോറിനീകരണം(chlorination), മെഥിലീകരണം (methylation) തുടങ്ങിയവ ഇവയില്പ്പെടുന്നു. | ||
| + | |||
| + | c. സൂക്ഷ്മദര്ശിനി ഉപയോഗിച്ചുള്ള പരിശോധന | ||
d. എക്സ്-റേ പരിശോധന | d. എക്സ്-റേ പരിശോധന | ||
| വരി 63: | വരി 79: | ||
e. സൂക്ഷ്മമായി നിയന്ത്രിക്കപ്പെട്ട ഭഞ്ജകസ്വേദനം | e. സൂക്ഷ്മമായി നിയന്ത്രിക്കപ്പെട്ട ഭഞ്ജകസ്വേദനം | ||
| - | ബെന്സീന് | + | ബെന്സീന് നിഷ്കര്ഷണത്തിനുശേഷമുള്ള അവശേഷങ്ങളെ ഓക്സീകരിച്ചപ്പോള് ബോണിന് (W.A. Bone)ഗണ്യമായ അളവില് ബെന്സീന് കാര്ബോക്സിലിക് അമ്ലവും മറ്റ് സദൃശങ്ങളായ സംയുക്തങ്ങളും ലഭിക്കുകയുണ്ടായി. ഇതില്നിന്നും കല്ക്കരിയുടെ ഒരു പ്രധാന അംശം 6-കാര്ബണ്വലയഘടനയോടുകൂടിയതാണെന്ന് അനുമാനിക്കപ്പെട്ടു. |
| - | പൈറോള് (pyrrole), ഫ്യൂറാന് (furan) തുടങ്ങിയവയുടെയോ അവയുടെ വ്യുത്പന്നങ്ങളുടെയോ | + | പൈറോള് (pyrrole), ഫ്യൂറാന് (furan) തുടങ്ങിയവയുടെയോ അവയുടെ വ്യുത്പന്നങ്ങളുടെയോ ഘടനകളാല് ബന്ധിക്കപ്പെട്ട ബെല്സിനോയ്ഡ് ഗ്രൂപ്പും ഉള്ളതായി കണ്ടു. |
==== പീറ്റ്==== | ==== പീറ്റ്==== | ||
| - | + | സെല്ലുലോസില്നിന്നുള്ള കല്ക്കരിയുടെ രൂപാന്തരണത്തിലെ ആദ്യത്തെ അവസ്ഥയാണ് പീറ്റ്. കുഴിച്ചെടുത്ത അവസ്ഥയില് 80 മുതല് 90 വരെ ശതമാനം ജലാംശം ഉണ്ടായിരിക്കും; ഉണക്കിയ പീറ്റില് 6 ശതമാനം മുതല് 15 ശതമാനം വരെയും. ജലാംശം കോശ(cell)ഘടനകളിലായി കാണപ്പെടുന്നതുകൊണ്ട് ഉണക്കുക പ്രയാസമാണെങ്കിലും, ഉണക്കിയ പീറ്റ് ഉപയോഗിക്കാന് എളുപ്പമാണ്. ഇതിന്റെ കലോറികമൂല്യം ഏകദേശം 5,000 മുതല് 10,000 വരെ BTU/റാത്തല് ആണ്; വിറകിനെക്കാള് കലോറികമൂല്യം അല്പം കൂടുമെന്നുമാത്രം. പീറ്റ് കുഴിച്ചെടുക്കലും ഉണക്കലും ചെലവേറിയതായതുകൊണ്ട് കല്ക്കരിപോലെ കുഴിച്ചെടുക്കപ്പെടുന്നില്ല; ചില രാജ്യങ്ങളില് ബ്രിക്കറ്റ് ആക്കി ഗാര്ഹികാവശ്യങ്ങള്ക്ക് ഉപയോഗിക്കുന്നുണ്ട്. | |
==== ലിഗ്നൈറ്റ്==== | ==== ലിഗ്നൈറ്റ്==== | ||
| - | പീറ്റിനും ബിറ്റ്യൂമിനീയ | + | പീറ്റിനും ബിറ്റ്യൂമിനീയ കല്ക്കരിക്കും മധ്യേയാണ് ലിഗ്നൈറ്റിന്റെ സ്ഥാനം. കുഴിച്ചെടുത്ത അവസ്ഥയില് 20 ശതമാനം മുതല് 45 ശതമാനംവരെ ജലാംശം കാണപ്പെടുന്നു. അസംസ്കൃത ലിഗ്നൈറ്റ് രണ്ടു തരത്തില് കാണപ്പെടുന്നു; തവിട്ടു കല്ക്കരി (brown coal), കറുത്ത കല്ക്കരി (black coal). ലിഗ്നൈറ്റിന് അപക്ഷയം (weathering) സംഭവിക്കുമ്പോള് ജലാംശത്തിന്റെ നല്ലൊരു പങ്ക് നഷ്ടപ്പെടുന്നു; അപ്പോള് പൊടിഞ്ഞുപോകുകയും ചെയ്യുന്നു. ദഹനസമയത്തും പൊടിഞ്ഞുപോകാന് സാധ്യതയുള്ളതുകൊണ്ട് ഗ്രേറ്റില് (grate)കൂടിയുള്ള നഷ്ടം താരതമ്യേന അധികമാണ്. ലിഗ്നൈറ്റ് സ്വതഃദഹനത്തിനു (spontaneous combustion) വിധേയമാകുന്നതുകൊണ്ട് തുറന്ന സ്ഥലത്ത് സൂക്ഷിച്ചുവയ്ക്കാറില്ല. ലിഗ്നൈറ്റിന്റെ കലോറികമൂല്യം ഏകദേശം 6,000 മുതല് 12,000 വരെ BTU/റാത്തല് ആണ്. ബ്രിക്കറ്റ് ആക്കിയും ഇത് ഉപയോഗിക്കുന്നുണ്ട്. ലോകത്തിലെ കല്ക്കരിസമ്പത്തില് പകുതിയോളം ലിഗ്നൈറ്റ് ആണെന്നു കണക്കാക്കപ്പെട്ടിരിക്കുന്നു. |
| - | ==== സബ്-ബിറ്റ്യൂമിനീയ | + | ==== സബ്-ബിറ്റ്യൂമിനീയ കല്ക്കരി==== |
| - | ലിഗ്നൈറ്റിനും ബിറ്റ്യൂമിനീയ | + | ലിഗ്നൈറ്റിനും ബിറ്റ്യൂമിനീയ കല്ക്കരിക്കും മധ്യേയുള്ള ഇനമാണിത്. ഇത് കോക്കിങ്ങിനു വിധേയമല്ലാത്തതും എളുപ്പം പൊടിഞ്ഞുപോകുന്നതും ആയ പദാര്ഥമാണ്. ലിഗ്നൈറ്റിനെക്കാള് കാഠിന്യവും സാന്ദ്രതയും ഏറിയിരിക്കും. ഏകദേശം 12 ശതമാനം മുതല് 25 ശതമാനം വരെ ജലാംശം കാണപ്പെടുന്നു. |
| - | ====ബിറ്റ്യൂമിനീയ | + | ====ബിറ്റ്യൂമിനീയ കല്ക്കരി ==== |
| - | ഏറ്റവുമധികം ഉപയോഗിക്കപ്പെടുന്ന ഇനമാണിത്; വായുവിന്റെ | + | ഏറ്റവുമധികം ഉപയോഗിക്കപ്പെടുന്ന ഇനമാണിത്; വായുവിന്റെ അസാന്നിധ്യത്തില് ചൂടാക്കുമ്പോള് "ബിറ്റ്യൂമന്'(bitumen)എന്ന പദാര്ഥത്തോട് സാദൃശ്യമുള്ള കറുത്ത ടാര് ഉണ്ടാവുന്നതുകൊണ്ടാണ് അതിന് "ബിറ്റ്യൂമിനീയ' കല്ക്കരി എന്ന പേരുണ്ടായത്. സാന്ദ്രവും കഠിനവുമായ ഈ കല്ക്കരിക്ക് വായുവില് അപക്ഷയം സംഭവിക്കുന്നില്ല. ജലാംശം ലിഗ്നൈറ്റിനെക്കാളും, സബ്-ബിറ്റ്യൂമിനീയ കല്ക്കരിയെക്കാളും കുറവാണ് (ഏകദേശം 3%). ബിറ്റ്യൂമിനീയ കല്ക്കരിയുടെ കലോറികമൂല്യം 8,000 മുതല് 15,000 വരെ BTU/റാത്തല് ആണ്. |
| - | + | ||
| + | ഇതില് കോക്കിങ്ങിനു യോജ്യമായതും അല്ലാത്തതുമായ(coking and non-coking) ഇനങ്ങളുണ്ട്. കോക്കിങ് കല്ക്കരി ലോഹകര്മീയകോക്ക് ഉണ്ടാക്കാന് ഉപയോഗിക്കുന്നു. നീരാവിയുത്പാദനത്തിനും മറ്റു വാതകങ്ങളുടെ നിര്മാണത്തിനും ബിറ്റ്യൂമിനീയ കല്ക്കരി ഉപയോഗിക്കാം. | ||
==== ആന്ഥ്റസൈറ്റ്==== | ==== ആന്ഥ്റസൈറ്റ്==== | ||
| - | + | കല്ക്കരിയുടെ രൂപവത്കരണപ്രക്രിയയില് അവസാനത്തെ അവസ്ഥയായിട്ടാണ് ഇത് അറിയപ്പെടുന്നത്. താഴ്ന്ന ജലാംശം, ബാഷ്പശീലമുള്ള ഘടകങ്ങള്, ഉയര്ന്ന കാര്ബണ് ശതമാനം എന്നിവയാണ് സവിശേഷതകള്. താരതമ്യേന പുക കുറവായതിനാലും സാവധാനം കത്തുന്നതിനാലും ഇത് ഗാര്ഹികാവശ്യങ്ങള്ക്കും നീരാവി ഉത്പാദനത്തിനും ഉപയോഗിക്കുന്നു. പുക കുറയ്ക്കുന്നതിനായി ബിറ്റ്യൂമിനീയ കല്ക്കരി ആന്ഥ്റസൈറ്റുമായി ചേര്ക്കുന്നു; കോക്ക് ഉണ്ടാക്കുന്നതിനായി കോക്കിങ്ങിന് യോജ്യമായ ബിറ്റ്യൂമിനീയ കല്ക്കരിയുമായി കൂട്ടിക്കലര്ത്തുന്നു. | |
==== കോക്ക്==== | ==== കോക്ക്==== | ||
| - | + | വായുസമ്പര്ക്കമില്ലാതെ കല്ക്കരിയെ സ്വേദനം ചെയ്യുമ്പോഴോ കാര്ബണീകരിക്കുമ്പോഴോ ലഭിക്കുന്ന അവശിഷ്ടപദാര്ഥമാണ് കോക്ക്; ഇതുകൂടാതെ ബാഷ്പശീലമുള്ള വസ്തുക്കളും ഉണ്ടാകുന്നു. കോക്കിങ്ങിനു യോജ്യമായ ബിറ്റ്യൂമിനീയ കല്ക്കരിയോ അതിന്റെ കൂട്ടോ (blend) ആണ് ഇതിനുപയോഗിക്കുന്നത്. കോക്ക് ഉത്പാദിപ്പിക്കുന്നതിന് രണ്ടുതരം പ്രക്രിയകളുണ്ട്: ഉന്നതതാപകാര്ബണീകരണവും (high temperature carbonization) നിമ്നതാപകാര്ബണീകരണവും (low temperature carbonization). | |
| - | + | ||
| - | + | കല്ക്കരിയെ 900°C-1100°C വരെയുള്ള താപനിലയില് ചൂടാക്കുന്ന പ്രക്രിയയെയാണ് ഉന്നതതാപ കാര്ബണീകരണം എന്നു പറയുന്നത്. ഈ പ്രക്രിയയില് ലഭിക്കുന്ന കോക്ക് ലോഹസംസ്കരണത്തിന് ഉപയോഗിക്കുന്നതുകൊണ്ട് ലോഹകര്മീയ കോക്ക് (meta-llurgical coke)എന്നു പറയുന്നു. വാതകച്ചൂളയില് ഉപയോഗിക്കുന്ന ഏതു ഭാരവും താങ്ങാനുള്ള കഴിവാണ് അതിന്റെ പ്രധാന ഗുണം. | |
| - | ഏകദേശം | + | |
| + | വാതകനിര്മാണത്തിനുവേണ്ടി ഉന്നതതാപത്തില് കല്ക്കരിയെ വാലുക(retort))യിലിട്ട് കാര്ബണീകരിക്കുമ്പോള് ലഭിക്കുന്ന ഉപോത്പന്നമാണ് വാതകക്കോക്ക് (gas coke). ഗാര്ഹികാവശ്യങ്ങള്ക്കും നീരാവി ഉത്പാദിപ്പിക്കാനും ലോഹസംസ്കരണ ചൂളയിലെ ഇന്ധനമായിട്ടും വാതകക്കോക്ക് ഉപയോഗിക്കാം. | ||
| + | |||
| + | ഏകദേശം 600°C-ല് കല്ക്കരി കാര്ബണീകരിക്കുന്നതിനെയാണ് നിമ്നതാപകാര്ബണീകരണമെന്നു പറയുന്നത്. ഇപ്രകാരം ലഭിക്കുന്ന കോക്കില് 10 ശതമാനം മുതല് 15 ശതമാനം വരെ ബാഷ്പശീല പദാര്ഥം കാണപ്പെടുന്നു. ലോഹകര്മീയ കോക്കിലോ വാതകക്കോക്കിലോ കാണപ്പെടുന്ന 2-3 ശതമാനത്തെക്കാള് അധികമാണിത്. അതുകൊണ്ട് ഗാര്ഹികാവശ്യങ്ങള്ക്കും ചെറുകിടവ്യാവസായികാവശ്യങ്ങള്ക്കുംവേണ്ടി, വേഗത്തില് കത്തുന്നതും താരതമ്യേന പുക കുറഞ്ഞതുമായ, ഇന്ധനങ്ങള് നിര്മിക്കുന്നതിന് നിമ്നതാപകാര്ബണീകരണം ഉപയോഗിക്കുന്നു. ലോഹകര്മീയ കോക്കിന്റെയും നിമ്നതാപ കോക്കിന്റെയും ഏകദേശവിശ്ലേഷണവും മൂലകവിശ്ലേഷണവും പട്ടിക 2-ല് ചേര്ത്തിരിക്കുന്നു. | ||
[[ചിത്രം:Vol3_141_chart.jpg|thumb|]] | [[ചിത്രം:Vol3_141_chart.jpg|thumb|]] | ||
| - | സുഷിരമയമായ കോക്കിന് ഓക്സിജനുമായി | + | സുഷിരമയമായ കോക്കിന് ഓക്സിജനുമായി ചേര്ന്ന് എളുപ്പത്തില് കത്തുവാന് കഴിയും. കല്ക്കരിയിലെ ചില അംശങ്ങള് ബാഷ്പീകരിക്കുമ്പോഴുണ്ടാകുന്ന കുമിളകളില്നിന്നാണ് സരന്ധ്രഘടന (porosity) സംഭവിക്കുക. ഇത് കല്ക്കരി എത്ര നേര്മയായി പൊടിക്കുന്നു എന്നതിനെയും ചൂടാക്കുമ്പോഴുണ്ടാകുന്ന പരിതഃസ്ഥിതിയെയും ഉപയോഗിക്കുന്ന കല്ക്കരിയുടെ തരത്തെയും ആശ്രയിച്ചിരിക്കുന്നു. |
| - | + | ||
| - | രണ്ടു പ്രക്രിയകളിലും ഉത്പാദകവസ്തുക്കള് ഒന്നുതന്നെയാണെങ്കിലും അവയുടെ അളവ് വ്യത്യസ്തങ്ങളായിരിക്കും. നിമ്നതാപത്തിലുള്ള | + | കോക്കിന്റെ പ്രകടവും യഥാര്ഥവുമായ ആപേക്ഷിക സാന്ദ്രതകളും സരന്ധ്രതയും നിര്ണയിക്കാനുള്ള പരീക്ഷണങ്ങള് ഉണ്ട്. കോക്കിന്റെ ബലം അളക്കുന്നത് ഷാറ്റര്പരീക്ഷണമുപയോഗിച്ചാണ്. 50 റാത്തല് ഭാരവും, രണ്ടിഞ്ച് വലുപ്പവുമുള്ള കോക്ക് നാലുതവണ ആറടി ഉയരത്തില്നിന്നും താഴെയുള്ള ഇരുമ്പുഷീറ്റിലേക്കിടുമ്പോള് എത്ര പങ്ക് പൊടിഞ്ഞുപോയെന്ന് കണക്കാക്കുന്നു; ഇത് അടിസ്ഥാനമാക്കിയാണ് ഷാറ്റര്സൂചകം നിര്ണയിക്കുന്നത്. |
| + | |||
| + | രണ്ടു പ്രക്രിയകളിലും ഉത്പാദകവസ്തുക്കള് ഒന്നുതന്നെയാണെങ്കിലും അവയുടെ അളവ് വ്യത്യസ്തങ്ങളായിരിക്കും. നിമ്നതാപത്തിലുള്ള നിര്മാണരീതിയില് വാതകോത്പന്നങ്ങള് കുറവും ദ്രാവകോത്പന്നങ്ങള് കൂടുതലുമായിരിക്കും; എന്നാല് ഉന്നതോഷ്മാവില് നേരേതിരിച്ചാണ്. പുകയില്ലാതെ കത്തുന്നതും ചാരത്തിന്റെ അംശം വളരെ കുറവുള്ളതുമായ ഈ ഇന്ധനത്തിന്റെ താപമൂല്യം ഏകദേശം 13,400 BTU/റാത്തല് ആണ്. | ||
==== ബ്രിക്കറ്റ്==== | ==== ബ്രിക്കറ്റ്==== | ||
| - | വളരെ | + | വളരെ നേര്ത്ത കല്ക്കരിപ്പൊടി സംബന്ധകവസ്തു(binder)ക്കളുടെ സാന്നിധ്യത്തിലോ അല്ലാതെയോ, മര്ദത്തിന്റെ സഹായത്താല് കട്ടകളാക്കുന്നതിനെയാണ് ബ്രിക്കറ്റിങ് (briquetting) എന്നു പറയുന്നത്. ഇപ്രകാരം പീറ്റ്, ലിഗ്നൈറ്റ് എന്നീ ഇനങ്ങളെ ബ്രിക്കറ്റുകളാക്കുന്നു. |
| - | പഞ്ചസാര | + | പഞ്ചസാര വ്യവസായത്തില്നിന്നു ലഭിക്കുന്ന മൊളാസസ് (molasses), സ്റ്റാര്ച്ച് ഫാക്ടറിയില്നിന്നും ലഭിക്കുന്ന ഡെക്സ്ട്രിന്പശ, കടലാസ് ഫാക്ടറിയില് നിന്നും ലഭിക്കുന്ന സള്ഫൈറ്റ് ലിക്വര് (sulphite liquor), ടാര്, അസംസ്കൃതഎണ്ണ മുതലായവ സംബന്ധകവസ്തുക്കളായി ഉപയോഗിക്കാം. ബ്രിക്കറ്റുകള് ചതുരാകൃതിയിലോ മുട്ടയുടെ ആകൃതിയിലോ ആകാം. ഏകദേശം 5 മുതല് 10 വരെ ശതമാനം സംബന്ധകവസ്തുക്കളും റോള്പ്രസ്സുകളും ഉപയോഗിച്ച് കട്ടകളാക്കുന്നു. |
| - | മുന്തിയയിനം ബ്രിക്കറ്റുകള് ബലമുള്ളതും, ജലരോധകശക്തിയുള്ളതും ആയിരിക്കും. സംബന്ധകവസ്തുവിന്റെ കലോറികമൂല്യം, ഉപയോഗിച്ച | + | മുന്തിയയിനം ബ്രിക്കറ്റുകള് ബലമുള്ളതും, ജലരോധകശക്തിയുള്ളതും ആയിരിക്കും. സംബന്ധകവസ്തുവിന്റെ കലോറികമൂല്യം, ഉപയോഗിച്ച കല്ക്കരിയുടേതിനെക്കാള് കൂടുതലാണെങ്കില്, ബ്രിക്കറ്റിന്റെ കലോറികമൂല്യവും കൂടിയിരിക്കും. ഇവ വ്യാവസായികാവശ്യങ്ങള്ക്ക് ഉപയോഗിക്കുന്നുണ്ടെങ്കിലും പ്രധാനമായും പ്രയോജനപ്പെടുത്തുന്നത് ഗാര്ഹികാവശ്യങ്ങള്ക്കാണ്. |
| - | ==== പൊടിയാക്കിയ | + | ==== പൊടിയാക്കിയ കല്ക്കരി (Pulverized coal)==== |
| - | പൊടിച്ച | + | പൊടിച്ച കല്ക്കരി വായുവുമായി കൂട്ടിക്കലര്ത്തിയാല് വേഗത്തിലും പരിപൂര്ണമായും കത്തുന്നു. അതുകൊണ്ട് കാര്യക്ഷമമായ ദഹനത്തിന് കല്ക്കരി നന്നായി പൊടിച്ച് ഉപയോഗിക്കുന്നു. ദ്രവ ഇന്ധനങ്ങളെപ്പോലെ ഇവയെ കത്തിക്കാം. |
| - | പൊടിയാക്കിയ | + | പൊടിയാക്കിയ കല്ക്കരി ഇന്ധനമായി ഉപയോഗിക്കുമ്പോള് പല ഗുണങ്ങളുമുണ്ട്. ഏതുതരം ഖര ഇന്ധനവും ഉപയോഗിക്കാം; കല്ക്കരിപ്പൊടി ഉപയോഗിക്കുന്ന ചൂളയില് ചില ചെറിയ മാറ്റങ്ങള് വരുത്തി വാതക ഇന്ധനമോ ദ്രവ ഇന്ധനമോ ഉപയോഗിക്കാം. ജ്വലനം ആരംഭിക്കാനും നിര്ത്താനും വളരെക്കുറച്ചു സമയം മാത്രമേ ആവശ്യമുള്ളൂ. |
| - | + | കല്ക്കരിപ്പൊടി സാധാരണ വായുപ്രവാഹത്തിലൂടെ ചൂളയിലേക്ക് കയറ്റുന്നു. ജ്വാലകത്തില്(burner)വച്ച് രണ്ടാംഘട്ടത്തിലുള്ള വായു(secondary air)വുമായി ചേര്ന്ന് ചൂളയിലേക്ക് വീഴുകയും അവിടെ നിലംബിത (suspended) അവസ്ഥയില് ജ്വലിക്കുകയും ചെയ്യുന്നു. | |
| - | പൊടിച്ച | + | പൊടിച്ച കല്ക്കരിയുടെ ദഹനത്തിന് സാധാരണ പരിപൂര്ണദഹനത്തിനു വേണ്ടുന്നതില് അല്പംകൂടുതല് വായുമാത്രമേ ആവശ്യമുള്ളൂ. ചൂളയിലേക്ക് നല്കുന്നതിനുമുമ്പ് ഈ വായുവിനെ ഉന്നത ഊഷ്മാവിലേക്ക് ഉയര്ത്തിയാല് ബോയിലറിന്റെ ക്ഷമത വര്ധിക്കും. പൊടിച്ച കല്ക്കരിയിലെ ചാരത്തിന്റെ അംശം അതിന്റെ സമ്പൂര്ണദഹനത്തിന് തടസ്സമാണ്. കല്ക്കരി നേരിയ പൊടിയായി ഉപയോഗിക്കുന്നതിനാല് ദഹനപ്രക്രിയയ്ക്കുശേഷം ഉണ്ടാകുന്ന ചാരം (fly ash) നിര്ഗമവാതകങ്ങളില്ക്കൂടി പുറത്തുപോകുകയും അന്തരീക്ഷത്തെ മലിനപ്പെടുത്തുകയും ചെയ്യുന്നു. അവക്ഷേപകങ്ങള് (precipitators) ഉപയോഗിച്ച് ചാരം പുറത്തുപോകുന്നത് തടയാം. |
| - | ചൂളയിലെ ഊഷ്മാവ് | + | ചൂളയിലെ ഊഷ്മാവ് വളരെയധികമാകുകയാണെങ്കില് ചാരം ഉരുകി ബോയിലര്ട്യൂബിന്റെ പുറത്തു പറ്റിപ്പിടിക്കുകയും താപപ്രസരണത്തിന് അതു തടസ്സം സൃഷ്ടിക്കുകയും ചെയ്യുന്നു. |
| - | + | ||
| - | + | ചൂള തെരഞ്ഞെടുക്കുന്നതിലും അതിന്റെ വ്യാപ്തം തീരുമാനിക്കുന്നതിലും പ്രധാന ഘടകമാണ് ചാരം ഉരുകുന്ന ഊഷ്മാവ്. വളരെ താഴ്ന്ന ഊഷ്മാവില് ഉരുകുന്ന ചാരമാണെങ്കില് ജ്വാലയില്വച്ച് ഉരുകുകയും ചൂളയുടെ ഭിത്തികളില് പറ്റിപ്പിടിക്കുകയും ചെയ്യുന്നു. ഇങ്ങനെ ഉണ്ടാകുന്ന അട്ടികള് ഭാരം കൂടുമ്പോള് അസ്തരങ്ങളുടെ (lining) കഷണങ്ങളോടുകൂടെ താഴെ വീഴുന്നു. ഇത് പരിഹരിക്കാന് ചൂളയുടെ വ്യാപ്തം കൂട്ടുകയും ട്യൂബുകളില്ക്കൂടി ജലം പ്രവഹിപ്പിച്ച് ചുമരുകളെ തണുപ്പിക്കുകയും ചെയ്യുന്നു. | |
| - | + | കല്ക്കരി നന്നായി പൊടിക്കുന്നതുപോലെ ഉണക്കുകയും ചെയ്തില്ലെങ്കില് സൈലോകളിലും മില്ലുകളിലും മറ്റും ബുദ്ധിമുട്ടുണ്ടാക്കും. ബിന്-ആന്ഡ്-ഫീഡര് (bin-and-feeder) സമ്പ്രദായമനുസരിച്ച് കല്ക്കരി ഉണക്കി പൊടിയാക്കി വലിയ ബങ്കറുകളില് സൂക്ഷിച്ചുവയ്ക്കുന്നു; പിന്നീട് അവ ആവശ്യാനുസരണം ചൂളയിലേക്കെത്തിക്കുന്നു. | |
| - | നീരാവി ഉത്പാദനത്തിനും, സിമന്റ് ഫാക്ടറികളിലും പൊടിച്ച | + | യൂണിറ്റ് (unit) സമ്പ്രദായമനുസരിച്ച് മില്ലുകളില് വച്ചുതന്നെ ഉണക്കുകയും പൊടിക്കുകയും ചെയ്യുന്നു; പിന്നീട് മുന്കൂട്ടി ചൂടാക്കിയ വായുപ്രവാഹത്തില് നേരെ ചൂളയിലേക്ക് തള്ളപ്പെടുന്നു. ഇതില് വലിയ ബങ്കറുകളുടെ ആവശ്യമില്ല. |
| + | |||
| + | നീരാവി ഉത്പാദനത്തിനും, സിമന്റ് ഫാക്ടറികളിലും പൊടിച്ച കല്ക്കരി ധാരാളമായി ഉപയോഗിക്കുന്നു. | ||
=== വിറക്=== | === വിറക്=== | ||
| - | ==== തടി ഇന്ധനമെന്ന | + | ==== തടി ഇന്ധനമെന്ന നിലയില്==== |
| - | + | വിറകില് പ്രധാനമായും സെല്ലുലോസും (cellulose) ചെറിയ അളവില് ലിഗ്നിന്, റെസിനുകള് (resins), അജൈവപദാര്ഥങ്ങള്, ജലം എന്നിവയും അടങ്ങിയിരിക്കുന്നു. വിറകിലെ ജലാംശം ഏകദേശം 25-50 ശതമാനം വരും. വിറക് എത്രമാത്രം ഉണങ്ങിയതാണ് എന്നതിനെ ആശ്രയിച്ചിരിക്കും അതിലെ ജലാംശത്തിന്റെ തോത്. ജലാംശം കൂടുന്നതനുസരിച്ച് താപമൂല്യം കുറയുന്നതിനാല് വ്യാവസായികാവശ്യങ്ങള്ക്ക് ഇത് ഉപയോഗിക്കുന്നില്ല. അറക്കപ്പൊടിയും വിറകിന്റെ മറ്റ് അവശിഷ്ടങ്ങളും ബോയിലറുകളില് ചിലപ്പോള് ഉപയോഗിക്കാറുണ്ട്. | |
==== മരക്കരി==== | ==== മരക്കരി==== | ||
| - | വിറക് | + | വിറക് വായുസമ്പര്ക്കമില്ലാതെ ഭഞ്ജകസ്വേദനം ചെയ്യുമ്പോള് ലഭിക്കുന്ന പദാര്ഥമാണ് മരക്കരി. വിറക് മണ്ണുകൊണ്ട് മൂടി ഭാഗികമായി ദഹിപ്പിച്ചാണ് ചെറിയ തോതില് മരക്കരി ഉണ്ടാക്കുന്നത്. അടയ്ക്കാവുന്ന റിട്ടോര്ട്ടിലിട്ടാണ് വ്യാവസായികാടിസ്ഥാനത്തില് മരക്കരി ഉണ്ടാക്കുന്നത്. കാഠിന്യമേറിയ (hard) മരമാണ് മരക്കരി ഉണ്ടാക്കാന് ഉത്തമം. |
| - | മരം ഭഞ്ജകസ്വേദനം ചെയ്യുമ്പോള് ബാഷ്പങ്ങളും ടാറും മറ്റും | + | |
| - | മരക്കരി ജലത്തെ | + | മരം ഭഞ്ജകസ്വേദനം ചെയ്യുമ്പോള് ബാഷ്പങ്ങളും ടാറും മറ്റും ബഹിര്ഗമിക്കുന്നു. ശേഷിക്കുന്ന ഖരപദാര്ഥമാണ് മരക്കരി. ഉണങ്ങിയ മരത്തില്നിന്ന് ഏകദേശം 30 ശതമാനം മരക്കരി ലഭിക്കുന്നു. മരക്കരിയില് ഏകദേശം 80 ശതമാനം കാര്ബണ്, 15 ശതമാനം ഓക്സിജനും നൈട്രജനും, 2 ശതമാനം ഹൈഡ്രജന്, 3 ശതമാനം ചാരം എന്നിവ അടങ്ങിയിരിക്കുന്നു. |
| + | |||
| + | മരക്കരി ജലത്തെ എളുപ്പത്തില് ആഗിരണം ചെയ്യുന്നു. ഇതില് ഏകദേശം 10-15 ശതമാനം ജലാംശം കാണും. ഇതിന്റെ കലോറികമൂല്യം 12,000 മുതല് 13,000 വരെ BTU/റാത്തല് ആണ്. താഴ്ന്ന ചാരശതമാനവും, ശുദ്ധി (purity)യുംമൂലം ലോഹകര്മീയ ഇന്ധനമായി പ്രയോജനപ്പെടുന്നു; പക്ഷേ, എളുപ്പം പൊടിഞ്ഞുപോകുന്നതുകൊണ്ട് കോക്കുപോലെ ഉപയോഗയോഗ്യമല്ല. | ||
===ഖര ഇന്ധനങ്ങളുടെ ഉപയോഗം === | ===ഖര ഇന്ധനങ്ങളുടെ ഉപയോഗം === | ||
| - | ഖര ഇന്ധനങ്ങളുടെ ഘടനയിലും ഗുണവിശേഷങ്ങളിലും ഉള്ള വലിയ വ്യത്യാസംമൂലം കാര്യക്ഷമമായ ഉപയോഗത്തിന് അവയുടെ ഘടന, യന്ത്രസംവിധാനം എന്നിവയെക്കുറിച്ച് | + | ഖര ഇന്ധനങ്ങളുടെ ഘടനയിലും ഗുണവിശേഷങ്ങളിലും ഉള്ള വലിയ വ്യത്യാസംമൂലം കാര്യക്ഷമമായ ഉപയോഗത്തിന് അവയുടെ ഘടന, യന്ത്രസംവിധാനം എന്നിവയെക്കുറിച്ച് അനേകവര്ഷത്തെ നിരീക്ഷണങ്ങളും പരീക്ഷണങ്ങളും ആവശ്യമായി വന്നു. ഈ പരീക്ഷണങ്ങള്മൂലം ഇന്ധനങ്ങളെക്കുറിച്ചു മാത്രമല്ല, വിവിധതരത്തിലുള്ള യന്ത്രസംവിധാനങ്ങളെയും അവയുടെ പ്രവര്ത്തനങ്ങളെയുംകുറിച്ച് കൂടുതല് അറിവ് നേടാന് ഇടയായി; കൂടാതെ, വ്യാവസായികമായി ഇന്ധനങ്ങളെ വിവിധ ഗുണങ്ങളനുസരിച്ച് തെരഞ്ഞെടുക്കുന്നതിനും ഈ പരീക്ഷണങ്ങള് സഹായിച്ചു. |
| - | ഒരു ഇന്ധനത്തിന്റെ താപമൂല്യത്തിനാണ് ഏറ്റവും പ്രാധാന്യം. താപം | + | ഒരു ഇന്ധനത്തിന്റെ താപമൂല്യത്തിനാണ് ഏറ്റവും പ്രാധാന്യം. താപം എത്രവേഗത്തില് ഉത്പാദിപ്പിക്കാമെന്നും എത്രകണ്ട് ഉപയോഗപ്പെടുത്താമെന്നും ഉള്ളത് ഒട്ടും അപ്രധാനമല്ല. |
==== ദഹനം==== | ==== ദഹനം==== | ||
| - | ഒരു വസ്തുവും വായുവിലെ ഓക്സിജനും തമ്മിലുള്ള അഭിക്രിയയെയാണ് ദഹനം എന്നു പറയുന്നത്. ഇന്ധനത്തിലെ | + | ഒരു വസ്തുവും വായുവിലെ ഓക്സിജനും തമ്മിലുള്ള അഭിക്രിയയെയാണ് ദഹനം എന്നു പറയുന്നത്. ഇന്ധനത്തിലെ കാര്ബണും ഹൈഡ്രജനും ചുരുങ്ങിയ തോതില് സള്ഫറും ഓക്സിജനുമായി പ്രതിപ്രവര്ത്തിക്കുമ്പോഴാണ് താപവും പ്രകാശവും ഉണ്ടാകുന്നത്. ശരിയായ ദഹനത്തിന് പദാര്ഥത്തെ അതിന്റെ ജ്വലനാങ്കം (ignition temperature) വരെ ചൂടാക്കണം (ഇന്ധനം ജ്വലിക്കാനാരംഭിക്കുകയും ബാഹ്യസ്രോതസ്സുകളില് നിന്നുള്ള താപം കൂടാതെതന്നെ തുടര്ന്നു കത്തുകയും ചെയ്യുന്ന ഊഷ്മാവിനെയാണ് ജ്വലനാങ്കം എന്നു പറയുന്നത്). |
| - | + | കാര്ബണികപദാര്ഥങ്ങളുടെ ദഹനം സങ്കീര്ണമായ പ്രക്രിയയാണ്. ഏതാനും ഘട്ടങ്ങളായിട്ടാണ് ഇത് നടക്കുന്നത്. ഇന്ധനം പരിപൂര്ണമായി കാര്ബണ്ഡൈഓക്സൈഡും ജലബാഷ്പവുമാകുന്നതിന് വേണ്ട ഓക്സിജന്റെ സൈദ്ധാന്തിക അളവ് (theoretical quantity) ഇന്ധനത്തിന്റെ മൂലകവിശ്ലേഷണത്തില്നിന്ന് കണ്ടുപിടിക്കാം. | |
| - | ഇന്ധനത്തിലെ മൊത്തം ഹൈഡ്രജന്റെയും ഓക്സിജന്റെയും ഒരുഭാഗം | + | ഇന്ധനത്തിലെ മൊത്തം ഹൈഡ്രജന്റെയും ഓക്സിജന്റെയും ഒരുഭാഗം കാര്ബണിന്റെ സംയോഗമായും മറ്റൊരു ഭാഗം ജലാംശമായും ആണ് കാണുന്നത്. ഹൈഡ്രജന്റെ വലിയൊരു ശതമാനം കാര്ബണ്സംയുക്തമായിരിക്കും. വ്യാവസായിക ഇന്ധനങ്ങളില് മൊത്തം ഹൈഡ്രജന് ഓക്സിജനുമായി ചേരുവാന് വേണ്ട ഹൈഡ്രജനെക്കാള് കൂടുതലായിരിക്കും. ഓക്സിജനുമായിച്ചേര്ന്ന ഹൈഡ്രജന്റെ അളവ് മൊത്തം ഹൈഡ്രജനില്നിന്ന് കുറച്ചാണ് ദഹനപ്രക്രിയയില് പങ്കെടുക്കുന്ന ഹൈഡ്രജന്റെ അളവ് കണക്കാക്കുന്നത്. അതിനാല് അസ്സല് ഹൈഡ്രജനാണ് (net hydrogen) ദഹനപ്രക്രിയയ്ക്ക് വിധേയമാകുന്നത്. |
| - | ദഹനത്തിന് ആവശ്യമായ ഓക്സിജനെക്കാള് | + | ദഹനത്തിന് ആവശ്യമായ ഓക്സിജനെക്കാള് കൂടുതല് അളവ് ഓക്സിജന് ചൂളയിലേക്ക് കടത്തിവിടുന്നു. ഓക്സിജന് കുറഞ്ഞുപോയാല് ചിമ്മിനിവാതകത്തില് കാര്ബണ് മോണോക്സൈഡിന്റെ അളവ് കൂടുതലായിരിക്കും. കാര്ബണ് മോണോക്സൈഡിന്റെ അളവ് വളരെ കൂടുകയാണെങ്കില് സ്വതന്ത്രാവസ്ഥയിലുള്ള ഹൈഡ്രജന് ചിമ്മിനിവാതകത്തില് ഏറിയിരിക്കും. |
| - | താഴെപ്പറയുന്ന അഭിക്രിയകളാണ് | + | താഴെപ്പറയുന്ന അഭിക്രിയകളാണ് ദഹനത്തില് സംഭവിക്കുന്നത്: |
<nowiki> | <nowiki> | ||
| - | (a) C + | + | (a) C + O<sub>2</sub> = CO<sub>2</sub> |
| - | 12 | + | 12 32 44 |
</nowiki> | </nowiki> | ||
| - | 12 ഗ്രാം | + | 12 ഗ്രാം കാര്ബണ് 32 ഗ്രാം ഓക്സിജനുമായി ചേരുമ്പോള് 44 ഗ്രാം കാര്ബണ്ഡൈഓക്സൈഡ് ഉണ്ടാകുന്നു; ഈ അഭിക്രിയയിലുണ്ടാകുന്ന താപം ഏകദേശം 14,590 BTU/റാത്തല് ആണ്. |
<nowiki> | <nowiki> | ||
| - | (b) 2C + | + | (b) 2C + O<sub>2</sub> = 2CO |
| - | 2x28 | + | 2x12 32 2x28 |
</nowiki> | </nowiki> | ||
| - | 24 ഗ്രാം | + | 24 ഗ്രാം കാര്ബണ് 32 ഗ്രാം ഓക്സിജനുമായി ചേരുമ്പോള് 56 ഗ്രാം കാര്ബണ് മോണോക്സൈഡ് ലഭിക്കുന്നു; നിര്ഗമിക്കുന്ന താപം ഏകദേശം 4,350 BTU/റാത്തല് ആണ്. |
<nowiki> | <nowiki> | ||
| - | (c) 2CO + | + | (c) 2CO + O<sub>2</sub> = 2CO<sub>2</sub> |
| - | 2x28 32 | + | 2x28 32 2x44 |
</nowiki> | </nowiki> | ||
| - | 56 ഗ്രാം | + | 56 ഗ്രാം കാര്ബണ് മോണോക്സൈഡ് 32 ഗ്രാം ഓക്സിജനുമായി ചേരുമ്പോള് 88 ഗ്രാം കാര്ബണ് ഡൈ ഓക്സൈഡ് കിട്ടുന്നു. ഒരു റാത്തല് കാര്ബണ് മോണോക്സൈഡില് നിന്ന് നിര്ഗമിക്കുന്ന താപം ഏകദേശം 4,390 BTU/റാത്തല് ആണ്. |
<nowiki> | <nowiki> | ||
| - | (d) | + | (d) 2H<sub>2</sub> + O<sub>2</sub> = 2H<sub>2</sub>O |
| - | 2x2 | + | 2x2 32 2x18 |
</nowiki> | </nowiki> | ||
| - | 4 ഗ്രാം ഹൈഡ്രജന് 32 ഗ്രാം ഓക്സിജനുമായി | + | 4 ഗ്രാം ഹൈഡ്രജന് 32 ഗ്രാം ഓക്സിജനുമായി ചേര്ന്ന് 36 ഗ്രാം ജലം ഉണ്ടാകുന്നു. ഇതില്നിന്നു ലഭിക്കുന്ന താപം ഏകദേശം 61,340 BTU/റാത്തല് ആണ്. |
<nowiki> | <nowiki> | ||
| - | (e) S + | + | (e) S + O<sub>2</sub> = SO<sub>2</sub> |
| - | 32 | + | 32 32 64 |
</nowiki> | </nowiki> | ||
| - | 32 ഗ്രാം | + | 32 ഗ്രാം സള്ഫര് 32 ഗ്രാം ഓക്സിജനുമായി യോജിക്കുമ്പോള് 64 ഗ്രാം സള്ഫര്ഡൈഓക്സൈഡ് ഉണ്ടാകുന്നു. മോചിപ്പിക്കപ്പെടുന്ന താപമാകട്ടെ, ഒരു റാത്തല് സള്ഫറിന് ഏകദേശം 3,930 BTU ആണ്. |
| - | + | ||
| + | കാര്ബണ്, ഹൈഡ്രജന്, ഓക്സിജന് എന്നിവ നിര്ദിഷ്ട അളവില് അടങ്ങിയ ഒരു റാത്തല് കല്ക്കരി പരിപൂര്ണമായി ദഹിപ്പിക്കുന്നതിന് ആവശ്യമായ വായുവിന്റെ അളവ് താഴെപ്പറയുംവിധം കണക്കാക്കാം: | ||
<nowiki> | <nowiki> | ||
| - | + | കാര്ബണ് - 78% | |
| - | ഹൈഡ്രജന് | + | ഹൈഡ്രജന് - 3.6% |
| - | ഓക്സിജന് | + | ഓക്സിജന് - 4.9% |
| - | + | അസ്സല് ഹൈഡ്രജന് = 3.6 - 4.9 X (4/32) | |
| - | + | = 3.01% | |
ആയതുകൊണ്ട് ദഹനത്തിനു വേണ്ടതായ ഓക്സിജന് | ആയതുകൊണ്ട് ദഹനത്തിനു വേണ്ടതായ ഓക്സിജന് | ||
| - | = 0.78( | + | = 0.78(32frac12;) + 0.0301(32frac4;) |
| - | = 2.32 | + | = 2.32 റാത്തല് |
| - | 100 ഗ്രാം | + | 100 ഗ്രാം വായുവില് 23.2 ഗ്രാം ഓക്സിജന് ഉണ്ട്. |
| - | വായുവിന്റെ ഭാരം = 2.32 x 100/23.2 | + | ∴ വായുവിന്റെ ഭാരം = 2.32 x 100/23.2 |
| - | + | = 10 റാത്തല് | |
</nowiki> | </nowiki> | ||
| - | ഇതുപോലെതന്നെ വായുവിന്റെ അളവുകൊണ്ട് | + | ഇതുപോലെതന്നെ വായുവിന്റെ അളവുകൊണ്ട് കാര്ബണ് ഡൈ ഓക്സൈഡിന്റെ അളവ് കണക്കാക്കാം. മേല്പറഞ്ഞ സമവാക്യങ്ങളില്നിന്ന് വാതകങ്ങള് ഏതുവിധത്തില് നിര്ഗമിക്കുന്നുവെന്നോ, വാതകങ്ങള് തമ്മിലോ, ഓക്സിജനും ജലബാഷ്പവും തമ്മിലോ ഏതു വിധത്തില് പ്രതിപ്രവര്ത്തിക്കുന്നുവെന്നോ മനസ്സിലാക്കാന് കഴിയുകയില്ല. ദഹനത്തിന്റെ ക്രിയാവിധി(mechanism)കളെക്കുറിച്ചുള്ള ഗവേഷണം ഇപ്പോഴും തുടര്ന്നുകൊണ്ടിരിക്കുന്നു. |
| - | ==== | + | ==== ഗാര്ഹികാവശ്യങ്ങള്==== |
| - | + | ശീതരാജ്യങ്ങളില് ചൂട് കിട്ടാന് തീക്കുണ്ഡങ്ങളിലും സ്റ്റൗവുകളിലും ഖര ഇന്ധനങ്ങളാണ് ഉപയോഗിക്കുന്നത്. ആദ്യകാലങ്ങളില് മനുഷ്യയത്നം ഉപയോഗിച്ച് ഇന്ധനം കൈകാര്യം ചെയ്തിരുന്നു. പില്ക്കാലത്ത് അത് യന്ത്രവത്കരിക്കപ്പെട്ടു. ഇതുമൂലം വേണ്ടവിധത്തില് ഇന്ധനം നിറയ്ക്കുന്നതിനും ആവശ്യാനുസരണം ചൂട് ലഭിക്കുന്നതിനും ചാരം നീക്കം ചെയ്യുന്നതിനും എളുപ്പമായി. | |
==== വ്യാവസായികാവശ്യങ്ങള്==== | ==== വ്യാവസായികാവശ്യങ്ങള്==== | ||
| - | ഏറെക്കുറെ എല്ലാത്തരം ഖര ഇന്ധനങ്ങളും വ്യവസായാവശ്യങ്ങള്ക്ക് ഉപയോഗിക്കാം. നൂതനയന്ത്രങ്ങളുടെ | + | ഏറെക്കുറെ എല്ലാത്തരം ഖര ഇന്ധനങ്ങളും വ്യവസായാവശ്യങ്ങള്ക്ക് ഉപയോഗിക്കാം. നൂതനയന്ത്രങ്ങളുടെ ആവിര്ഭാവത്തോടെ മനുഷ്യയത്നം ലഘൂകരിക്കാനും ഇന്ധനം ലാഭിക്കുവാനും കഴിഞ്ഞു. ഓരോ ഇന്ധനവും കാര്യക്ഷമമായി കത്തിക്കുന്നതിന് യന്ത്രസംവിധാനത്തില് പ്രത്യേക പരിഗണനകള് ആവശ്യമാണ്. |
| - | ഖര ഇന്ധനങ്ങള് ഇന്ധനവിതാനത്തിലോ(fuel bed) നിലംബിതമായോ (suspended) | + | |
| - | ഇന്ധനവിതാനങ്ങളിലുള്ള ജ്വലനം | + | ഖര ഇന്ധനങ്ങള് ഇന്ധനവിതാനത്തിലോ(fuel bed) നിലംബിതമായോ (suspended)അല്ലെങ്കില് രണ്ടും ചേര്ന്നവിധത്തിലോ കത്തിക്കാം. ജ്വലനോപാധികള് തെരഞ്ഞെടുക്കുന്നത് ഇന്ധനത്തിന്റെ തരവും ആവശ്യമായ താപത്തിന്റെ അളവും സാമഗ്രിയുടെ താരതമ്യവിലയും അനുസരിച്ചായിരിക്കും. |
| - | + | ||
| - | ബിറ്റ്യൂമിനീയ | + | ഇന്ധനവിതാനങ്ങളിലുള്ള ജ്വലനം ഓവര്ഫീഡ് (over feed) എന്നും അണ്ടര്ഫീഡ് (under feed) എന്നും രണ്ടുതരമായി വിഭജിക്കാം. |
| - | ==== ബ്ലാസ്റ്റ് | + | |
| - | ആധുനിക വാതകച്ചൂളയുടെ വ്യാസം ഏകദേശം 9 മീറ്ററും ഉയരം 27-34 മീറ്ററും വരും. പ്രതിദിന ഉത്പാദനം ഏകദേശം 1,000 ടണ് കാരിരുമ്പും ആയിരിക്കും. ഇതിലുപയോഗിക്കുന്ന കോക്ക് | + | ഓവര്ഫീഡ് ജ്വലനത്തില് ഇന്ധനം വായുവിന്റെ പ്രവേശനത്തിന് മുകളിലായി ഗ്രേറ്റി(grate)ലേക്ക് നിറയ്ക്കുന്നു. കോരിക ഉപയോഗിച്ച് ഗ്രേറ്റിലേക്ക് ഇന്ധനം നിറയ്ക്കുന്നതും അടിയില്നിന്ന് വായു ഗ്രേറ്റിലേക്ക് വരുന്നതും ഓവര്ഫീഡ് ജ്വലനത്തിന് ഉദാഹരണമാണ്. വ്യാപന അംഗാരിത്രവും (spreader stoker) സഞ്ചാരിതഗ്രേറ്റ് അംഗാരിത്രവും (travelling grate stoker) ഈ വിഭാഗത്തില്പ്പെടുന്നു. അണ്ടര്ഫീഡിലാകട്ടെ, വിതാനത്തിലേക്കുള്ള വായുവിന്റെയും ജ്വലനതലത്തിലേക്കുള്ള ഇന്ധനത്തിന്റെയും ദിശകള് ഒരേവിധമായിരിക്കും. ഈ വിഭാഗത്തില്, ദാഹ്യവാതകങ്ങള് ധവളോജ്ജ്വലമായ മേല്വിതാനത്തിലൂടെ കടന്നുപോകുന്നതുകൊണ്ട് പരിപൂര്ണദഹനം സാധ്യമാകുന്നു. സിംഗിള്-റിട്ടോര്ട്ട് അംഗാരിത്രവും (single retort stoker)സ്ക്രൂഫീഡ് അംഗാരിത്രവും (screw-feed stoker) മറ്റും ഇതില് ഉള്പ്പെടുന്നു. |
| + | |||
| + | ബിറ്റ്യൂമിനീയ കല്ക്കരി ഉപയോഗിക്കുന്ന, താരതമ്യേന വലിയ അംഗാരിത്രത്തില് കുഴിച്ചെടുക്കുന്ന കല്ക്കരിയിലെ വലിയ കഷണങ്ങള് നീക്കം ചെയ്തശേഷമാണ് ഉപയോഗിക്കുന്നത്; ചെറിയ അംഗാരിത്രത്തില് കല്ക്കരിയിലെ ചെറിയ തരികളാണു നീക്കം ചെയ്യുന്നത്. | ||
| + | ==== ബ്ലാസ്റ്റ് ഫര്ണസ്==== | ||
| + | ഉരുക്കുന്നതിനും ഭര്ജിക്കുന്നതിനും(roast), നീരോക്സീകരിക്കുന്നതിനും ഉപയോഗിക്കുന്നതും ലംബരൂപമുള്ളതും, തുടര്ച്ചയായി പ്രവര്ത്തിക്കുന്നതുമായ ഉരുക്കുചൂളയെയാണ് ബ്ലാസ്റ്റ് ഫര്ണസ് എന്നു പറയുന്നത്; ഇതിനെ വാതകച്ചൂളയെന്നും പറയാം. ഇരുമ്പയിരിനെ ഉരുക്കി കാരിരുമ്പ് (pig iron) ആക്കുന്നതിനാണ് ഇത് പ്രധാനമായി ഉപയോഗിക്കുന്നത്. ഒരു ആധുനിക വാതകച്ചൂളയുടെ വ്യാസം ഏകദേശം 9 മീറ്ററും ഉയരം 27-34 മീറ്ററും വരും. പ്രതിദിന ഉത്പാദനം ഏകദേശം 1,000 ടണ് കാരിരുമ്പും ആയിരിക്കും. ഇതിലുപയോഗിക്കുന്ന കോക്ക് നിര്ദിഷ്ട മേന്മയും ആകൃതിയും ബലവും ഉള്ളതായിരിക്കണം; ഇത് ഒരേ സമയം ഇന്ധനമായും നിരോക്സീകാരിയായും വര്ത്തിക്കുന്നു. | ||
| - | ഉന്നത ഊഷ്മാവിലുണ്ടാകുന്ന കോക്കിന്റെ സുഷിരത, സാന്ദ്രത മുതലായവയാണ് അതിനെ വാതകച്ചൂളയ്ക്കു പറ്റിയതാക്കുന്നത്. ഈ | + | ഉന്നത ഊഷ്മാവിലുണ്ടാകുന്ന കോക്കിന്റെ സുഷിരത, സാന്ദ്രത മുതലായവയാണ് അതിനെ വാതകച്ചൂളയ്ക്കു പറ്റിയതാക്കുന്നത്. ഈ ചൂളയില് ഉപയോഗിക്കുമ്പോള് കോക്കിന്റെ തരിയും പൊടിയും ഒഴിവാക്കേണ്ടതാണ്. 10 സെ.മീ. വലുപ്പമുള്ള കോക്കുപയോഗിക്കുന്നതാണ് അഭികാമ്യം. ഇത്തരം കോക്കില് ബാഷ്പശീലമുള്ള പദാര്ഥം 2 ശതമാനവും സ്ഥിരകാര്ബണ് 85 ശതമാനം മുതല് 90 ശതമാനം വരെയും, സള്ഫര് 0.6 ശതമാനം മുതല് 1.5 ശതമാനം വരെയും ആയിരിക്കും. ചാരത്തിന്റെ ശതമാനം 8 മുതല് 16 വരെ ആകാമെങ്കിലും, 12 ശതമാനത്തില് കൂടാതിരിക്കുന്നതാണ് അഭികാമ്യം. ചാരം കുറയ്ക്കുന്നതിനനുസരിച്ച് വാതകച്ചൂളയില്നിന്നുള്ള ഇരുമ്പിന്റെ ഉത്പാദനം കൂടുന്നു. കോക്കിലുള്ള ജലാംശം 5 ശതമാനത്തില് താഴെയാകണം. വാതകച്ചൂളയിലേക്ക് കടത്തിവിടുന്ന വായു ഒരു മിനിട്ടില് 70,000 പ്രമാണ ഘന അടി (standard cubic foot)ആയിരിക്കും. ഈ വായു 900°F-നും 1,200°Fഎനും മധ്യേ മുന്കൂട്ടി ചൂടാക്കി, 15 psi മര്ദത്തില് കടത്തിവിടുന്നു. ഇങ്ങനെ മുന്കൂട്ടി ചൂടാക്കുന്നതിന് നാല് സ്റ്റൗവുകള് അടങ്ങുന്ന ഒരു സെറ്റാണ് ഉപയോഗിക്കുന്നത്. ഇതിനുപയോഗിക്കുന്ന സ്റ്റൗവിന്റെ ഉയരം 30 മീറ്ററും വ്യാസം 6.6 മീറ്ററും ആയിരിക്കും. |
| - | മേല്പറഞ്ഞ തരത്തിലുള്ള ഒരു | + | മേല്പറഞ്ഞ തരത്തിലുള്ള ഒരു ചൂളയില് 2,000 ടണ് ഇരുമ്പയിരും 100 ടണ് കോക്കും 500 ടണ് ചുണ്ണാമ്പുകല്ലുമാണ് ഉപയോഗിക്കുന്നത്. ഈ പദാര്ഥങ്ങള് യഥാനുപാതം ഇടവിട്ട് ചൂളയുടെ മുകള്ഭാഗത്തുകൂടി നിറയ്ക്കുന്നു. ചൂളയില്നിന്ന് ഇരുമ്പും കിട്ടവും (slag)പുറത്തെടുക്കുന്നതിനനുസരിച്ച് അസംസ്കൃതപദാര്ഥങ്ങള് ചൂളയില് നിറച്ചുകൊണ്ടിരിക്കണം. |
==ദ്രവ ഇന്ധനങ്ങള് == | ==ദ്രവ ഇന്ധനങ്ങള് == | ||
08:59, 5 സെപ്റ്റംബര് 2014-നു നിലവിലുണ്ടായിരുന്ന രൂപം
ഇന്ധനങ്ങള്
Fuels
വായുവില് കത്തിദഹിക്കുമ്പോള് ഉപഭോഗപ്രദമായ രൂപത്തില് ഊര്ജം ഉത്പാദിപ്പിക്കുവാന് കഴിവുള്ള പദാര്ഥങ്ങള്. ഇന്ധനത്തിന്റെ ഓക്സിഡേഷന് (oxidation) ദഹനം (combustion) എന്നു പറയുന്നു.
പ്രാചീനശിലായുഗത്തിനു മുമ്പുമുതല്ക്കേ മനുഷ്യവര്ഗം ഇന്ധനം ഉപയോഗിച്ചിരുന്നതായി കരുതപ്പെടുന്നു. ഭക്ഷണം പാകംചെയ്യുന്നതിനും പ്രകൃതിപ്രാതികൂല്യങ്ങളില് ജീവന് നിലനിര്ത്തുന്നതിനും ഇന്ധനത്തിന്റെ കണ്ടുപിടിത്തം മനുഷ്യനെ സഹായിച്ചു. ഇന്ധനത്തിന്റെയും തീയുടെയും ഉപയോഗം മനുഷ്യന്റെ സാങ്കേതിക മുന്നേറ്റത്തിന്റെ ആരംഭം കുറിച്ചു. ഇന്ധനം ലഭിക്കാതായാല് മനുഷ്യവര്ഗത്തിന്റെ നിലനില്പുതന്നെ അപകടത്തിലാകും. പ്രധാന കമ്പോള ഇന്ധനങ്ങള് കാര്ബണ്, ഹൈഡ്രജന് എന്നിവയുടെ സംയുക്തങ്ങളാണ്.
ഇന്ധന ഘടകങ്ങള്
വിറക്, പീറ്റ്, കല്ക്കരി, പെട്രാളിയം, പ്രകൃതിവാതകം മുതലായ നൈസര്ഗിക ഇന്ധനങ്ങളിലെ പ്രധാനഘടകങ്ങള് കാര്ബണ്, ഹൈഡ്രജന്, ഓക്സിജന് തുടങ്ങിയ മൂലകങ്ങളും, ചെറിയ അളവില് ഗന്ധകവും (Sulphur) നൈട്രജനും ആണ്. ഇതുകൂടാതെ ജലാംശവും ഖനിജചാരവും (mineral ash) കാണപ്പെടുന്നു.
ഇന്ധനത്തിലെ ഘടകങ്ങള് ഓക്സിജനുമായി സംയോജിക്കുമ്പോള് താപം ഉത്പാദിപ്പിക്കപ്പെടുന്നു. ഇന്ധനത്തിന്റെ രാസയോഗത്തില്നിന്നുണ്ടാകുന്ന താപം എത്രയെന്ന് ഏകദേശം കണക്കാക്കാം. താപത്തിന്റെ ബ്രിട്ടീഷ് ഏകകമാണ് BTU (British Thermal Unit).ഒരു റാത്തല് (pound) വെള്ളത്തിന്റെ ചൂട് 60oF-ല് നിന്ന് ഒരു ഡിഗ്രി ഉയര്ത്തുന്നതിനുവേണ്ട താപത്തിന്റെ അളവാണിത്.
താപത്തിന്റെ അന്താരാഷ്ട്രമാത്ര "കലോറി' (Calorie) ആണ്. ഒരു ഗ്രാം വെള്ളത്തിന്റെ താപനില 0oCല് നിന്നും 100oC വരെ ഉയര്ത്താന് വേണ്ട താപത്തിന്റെ നൂറിലൊരംശമാണ് ഒരു കലോറി. ഒരു BTU = 252 കലോറി = 0.252 കിലോ കലോറി. ഒരു കിലോ കലോറി 4200 ജൂള് ഊര്ജത്തിനു തുല്യമാണ്.
ഒരു റാത്തല് (0.453 കി.ഗ്രാം) കാര്ബണ് പരിപൂര്ണമായി കാര്ബണ്ഡൈഓക്സൈഡ് ആയി മാറുമ്പോള് ഏകദേശം 14,590 BTUവും, കാര്ബണ് മോണോക്സൈഡ് ആയി മാറുമ്പോള് ഏകദേശം 4350 BTUവും ഉണ്ടാകുന്നു. [ഈ ലേഖനത്തില് സൗകര്യത്തിനുവേണ്ടി ഭാരത്തിന്റെ അളവുകളായി "റാത്തല്' അഥവാ "പൗണ്ട്', "ഗ്രാം' എന്നീ മാത്രകളും; താപനിലത്തോതുകളായി സെല്ഷ്യസ്, ഫാരന്ഹീറ്റ് എന്നീ മാത്രകളും ഉപയോഗിച്ചിട്ടുണ്ട്. 1 റാത്തല് = 435.4 ഗ്രാം; 1 കിലോഗ്രാം = 1000 ഗ്രാം = 2.2 പൗണ്ട്. സെല്ഷ്യസും (C) ഫാരന്ഹീറ്റും (F) തമ്മിലുള്ള ബന്ധം, C/100 = (F-32)/180 ആണ് ]. ഈ കാര്ബണ്മോണോക്സൈഡ്, കാര്ബണ്ഡൈഓക്സൈഡ് ആകുമ്പോള് ശേഷിച്ച 10,240 BTU-ഉം ഉണ്ടാകുന്നു.
ഏകകപിണ്ഡമുള്ള (unit mass)ഒരു പദാര്ഥം പൂര്ണമായി ദഹിക്കുമ്പോള് ലഭിക്കുന്ന താപമൂല്യത്തെ അതിന്റെ കലോറികമൂല്യം (calorific value) എന്നു പറയുന്നു. ഇന്ധനത്തിന്റെ മൂല്യം അതിന്റെ കലോറികമൂല്യത്തോട് ബന്ധപ്പെട്ടിരിക്കും. ഇന്ധനത്തിലെ മാലിന്യങ്ങള് കലോറികമൂല്യത്തെ ബാധിക്കുകയും ചെയ്യും.
ഖര ഇന്ധനങ്ങള്
ഖര ഇന്ധനങ്ങളെ പ്രകൃതിദത്തമെന്നും നിര്മിതമെന്നും രണ്ടായി തിരിക്കാം. ആദ്യത്തേതില് ജൈവപദാര്ഥങ്ങള്, വിറക്, പീറ്റ്, കല്ക്കരി മുതലായവയും രണ്ടാമത്തേതില് ഭഞ്ജകസ്വേദനം (destructive distillation) വഴി ലഭിക്കുന്ന കോക്ക്, മരക്കരി എന്നിവയും ഉള്പ്പെടുന്നു. വായുരഹിതമായ അടച്ച പാത്രത്തില് പദാര്ഥങ്ങളെ താപശക്തികൊണ്ട് സ്വേദനംചെയ്യുന്ന പ്രക്രിയയെയാണ് ഭഞ്ജകസ്വേദനം എന്നു പറയുന്നത്. ലോഹകര്മീയകോക്കും (metallurgical coke)വാതകകോക്കും (gas coke) ഉണ്ടാക്കുവാന് ഈ പ്രക്രിയയാണ് പ്രയോജനപ്പെടുത്തുന്നത്.
കല്ക്കരിയും ബന്ധപ്പെട്ട ഇന്ധനങ്ങളും
യുഗങ്ങള്ക്കുമുമ്പ് അടിഞ്ഞുകൂടിയ സസ്യപദാര്ഥങ്ങളിലും മറ്റ് സെല്ലുലോസ് പദാര്ഥങ്ങളിലും ചൂടിന്റെയും മര്ദത്തിന്റെയും ജീവാണുക്കളുടെയും സഹായത്താല് ഉരുത്തിരിയുന്ന കാര്ബണിക പദാര്ഥങ്ങളുടെ അട്ടികളാണ് കല്ക്കരി. ഘടനയും ഗുണവും അനുസരിച്ച് അവ പലതരത്തില് കാണപ്പെടുന്നു. ഏകദേശം 1,000-ത്തിലധികം വര്ഷത്തേക്കുള്ള കല്ക്കരിശേഖരം ഭൂമുഖത്ത് അവശേഷിച്ചിട്ടുള്ളതായി കണക്കാക്കപ്പെട്ടിരിക്കുന്നു.
വര്ഗീകരണം
രാസയോഗം, വ്യാവസായികോപയോഗം, കോക്കല് സ്വഭാവം (coking properties), ജിയോളജീയ വയസ് (geological age) എന്നിവയെ അടിസ്ഥാനമാക്കി കല്ക്കരിയെ വര്ഗീകരിക്കാവുന്നതാണ്. ഇനങ്ങള്ക്ക് സ്പഷ്ടമായ വ്യത്യാസങ്ങള് ഇല്ലെങ്കിലും വിഭിന്ന സ്വഭാവവിശേഷങ്ങളുള്ള ഘടകങ്ങളടങ്ങിയ ഒരു കുടുംബമായി കല്ക്കരിയെ കണക്കാക്കാം. ഏതിനം കല്ക്കരിയുടെയും നിലവാരം നിര്ണയിക്കുന്നത് അതിന്റെ രൂപാന്തരീകരണ പ്രക്രിയയെ അടിസ്ഥാനമാക്കിയാണ്. കല്ക്കരി രൂപാന്തരീകരണപ്രക്രിയ പീറ്റ് →ലിഗ്നൈറ്റ് → ബിറ്റ്യൂമിനീയ കല്ക്കരി → ആന്ഥ്റസൈറ്റ് → ഗ്രാഫൈറ്റ് എന്ന ക്രമത്തിലാണ്. മേല്പറഞ്ഞ ഓരോ ഇനത്തിനും വ്യക്തമായ ഭൗതികവും രാസപരവുമായ സവിശേഷതകള് ഉണ്ടെങ്കിലും അവയുടെ അതിര്ത്തിരേഖകള് തുലോം ലോലമാണ്.
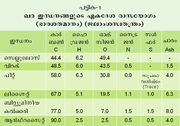
അമേരിക്കന് സ്റ്റാന്ഡേര്ഡ് അസോസിയേഷന് (American Standard Association)കല്ക്കരിയെ നാല് ഇനങ്ങളായി തിരിച്ചിരിക്കുന്നു: ആന്ഥ്റസൈറ്റ്, ബിറ്റ്യൂമിനീയ കല്ക്കരി, സബ്-ബിറ്റ്യൂമിനീയ കല്ക്കരി, ലിഗ്നൈറ്റും തവിട്ടു കല്ക്കരിയും. മുകളില് കൊടുത്തിരിക്കുന്ന പട്ടിക, കാര്ബണിന്റെ വര്ധനവും ഓക്സിജന്റെ ലോപവും അനുസരിച്ച് സെല്ലുലോസില്നിന്ന് ആന്ഥ്റസൈറ്റിലേക്കുള്ള അവസ്ഥാന്തരം കാണിക്കുന്നു.
കല്ക്കരിയുടെ നിലവാരം നിര്ണയിക്കുന്നതില് ജലാംശത്തിന്റെ അളവിനോ അന്യഖനിജങ്ങളുടെ സാന്നിധ്യത്തിനോ ഒരു പ്രാധാന്യവുമില്ല. ഈ വസ്തുത കണ്ടെത്തിയ എസ്.ഡബ്ല്യു. പാര് ഖനിജപദാര്ഥരഹിതവും ജലാംശമുക്തവുമായ അവസ്ഥയിലുള്ള താപമൂല്യമനുസരിച്ച് കല്ക്കരിയെ വര്ഗീകരിച്ചു. ഇതനുസരിച്ച് ബാഷ്പശീലമുള്ള പദാര്ഥങ്ങളും (volatile matter) സ്ഥിര കാര്ബണും (fixed carbon) ആണ് കല്ക്കരിയുടെ പ്രധാന ഘടകങ്ങള്. ബാഷ്പശീലമുള്ള പദാര്ഥങ്ങളുടെ ശതമാനം, "യഥാര്ഥ' കല്ക്കരിയുടെ താപമൂല്യം എന്നിവയുടെ താരതമ്യപഠനം പാര് വര്ഗീകരണത്തിലൂടെ മനസ്സിലാക്കാം.
ഈ വര്ഗീകരണമനുസരിച്ച് കല്ക്കരിയെ താഴെപ്പറയുന്ന വിഭാഗങ്ങളായി തിരിച്ചിരിക്കുന്നു: ആന്ഥ്റസൈറ്റ്, സെമി-ആന്ഥ്റസൈറ്റ്, ബിറ്റ്യൂമിനീയം-A, ബിറ്റ്യൂമിനീയം-B, ബിറ്റ്യൂമിനീയം-C, ബിറ്റ്യൂമിനീയം-D, ലിഗ്നൈറ്റ്, പീറ്റ്.
സി.എ. സേയ്ലറുടെയാണ് മറ്റൊരു വര്ഗീകരണം: ഇതില് ഹൈഡ്രജന്റെ അളവനുസരിച്ച് അഞ്ചു ഗ്രൂപ്പുകളായി തരംതിരിക്കുകയും വീണ്ടും അവയെ കാര്ബണിന്റെ അളവനുസരിച്ച് ഉപഗ്രൂപ്പുകളായി വിഭജിക്കുകയും ചെയ്തിരിക്കുന്നു.
കാര്ബണിക പദാര്ഥങ്ങള്ക്കുള്ള പരീക്ഷണങ്ങള്
കല്ക്കരി, കോക്ക് മുതലായ കാര്ബണിക പദാര്ഥങ്ങളുടെ വാണിജ്യമൂല്യത്തെയും ദഹനഗുണങ്ങളെയും പ്രത്യേകാവശ്യങ്ങള്ക്കുള്ള അവയുടെ അനുയോജ്യതയെയും ബന്ധപ്പെടുത്തിയുള്ള അപഗ്രഥനപരീക്ഷണങ്ങള് ആവിഷ്കരിക്കപ്പെട്ടിട്ടുണ്ട്. ഇവയില് പല പരീക്ഷണങ്ങളും രാസവിശ്ലേഷണങ്ങള് അല്ല; അവ അടിസ്ഥാന ഭൗതിക സ്ഥിരാങ്കങ്ങളും (physical constants)തരുന്നില്ല. പദാര്ഥങ്ങളുടെ സ്വഭാവഗുണങ്ങള് പരിശോധിക്കുന്നതിനുള്ള അമേരിക്കന് സൊസൈറ്റി (American Society for Testing Materials-ASTM) കല്ക്കരിയും കോക്കും പ്രതിചയിക്കുന്നതിനും (sampling) പരീക്ഷിക്കുന്നതിനും നിഷ്കൃഷ്ടവും വിശദവുമായ ഉപകരണങ്ങളും നടപടിക്രമങ്ങളും ആവിഷ്കരിച്ചിട്ടുണ്ട്.
പദാര്ഥത്തിലെ സ്വതന്ത്രജലാംശം (free moisture)വായു ഉപയോഗിച്ച് ഉണക്കി കണ്ടുപിടിക്കാം; അതിനുശേഷം പദാര്ഥത്തെ പൊടിച്ച് 60-മെഷ് (Mesh) അരിപ്പയിലൂടെ അരിച്ച് വായുനിബദ്ധമായ അറകളില് സൂക്ഷിച്ച് പരീക്ഷണങ്ങള്ക്കുപയോഗിക്കുന്നു. വ്യത്യസ്ത രീതിയിലുള്ള പരീക്ഷണങ്ങള് വിഭിന്നങ്ങളായ ഫലങ്ങള് തരുന്നതിനാല് ഒരേ രീതിതന്നെ എല്ലാവരും ഉപയോഗിക്കേണ്ടതുണ്ട്. പരക്കെ ഉപയോഗിക്കുന്ന പരീക്ഷണ രീതികള് നാലാണ്: ഏകദേശവിശ്ലേഷണം (Approximate analysis), മൂലക വിശ്ലേഷണം(ultimate analysis), കേക്കിങ് സൂചകം (caking index), കലോറികമൂല്യം (caking index). ചൂടാക്കുന്നതിനും നീരാവിയുത്പാദിപ്പിക്കുന്നതിനും മറ്റും ഉപയോഗിക്കുന്ന ഇന്ധനങ്ങള് ചൂടാക്കുമ്പോഴോ ജ്വലിക്കുമ്പോഴോ ഉള്ള അവയുടെ പ്രവര്ത്തനരീതിയുമായി ബന്ധപ്പെട്ട മൂല്യം കണക്കാക്കുന്ന ലളിതവും സത്വരവും ആയ പരീക്ഷണം ആവിഷ്കരിക്കപ്പെട്ടിട്ടുണ്ട്. ഏകദേശവിശ്ലേഷണത്തില് ജലാംശം, ചാരം, ബാഷ്പശീലമുള്ള പദാര്ഥം (volatile matter), സ്ഥിരകാര്ബണ് (fixed carbon) എന്നിവയുടെ അളവ് നിര്ണയിക്കപ്പെടുന്നു. 60-മെഷ് അരിപ്പയിലൂടെ കടക്കുന്ന കല്ക്കരിപ്പൊടിയാണിതിന് ഉപയോഗിക്കുന്നത്.
a. ജലാംശം. ഒന്നോരണ്ടോ ഗ്രാം കല്ക്കരി ഒരു മണിക്കൂര് നേരത്തേക്ക് 105-110°C ഊഷ്മാവില് ചൂടാക്കുമ്പോള് നഷ്ടപ്പെടുന്ന ഭാരമായിരിക്കും അതിലുണ്ടായിരുന്ന ജലാംശം. ഓക്സീകരണപ്രക്രിയയ്ക്ക് വിധേയമാകാന് സാധ്യതയുള്ളതുകൊണ്ട് നിഷ്ക്രിയവാതകമായ നൈട്രജന്റെ സാന്നിധ്യത്തിലാണ് ചൂടാക്കേണ്ടത്.
b. ചാരം. ഒന്നോരണ്ടോ ഗ്രാം കല്ക്കരി പ്ലാറ്റിനമോ സിലിക്കയോ കൊണ്ടുള്ള പാത്രത്തില് ക്രമമായി 800°C വരെ ചൂടാക്കുക. ദഹനം പരിപൂര്ണമാവുമ്പോഴുള്ള അവശിഷ്ടം തണുപ്പിച്ച് കിട്ടുന്ന ഭാരം ചാരത്തിന്റെ ഭാരമായിരിക്കും.
c. ബാഷ്പശീലമുള്ള പദാര്ഥങ്ങള്. ഒരുഗ്രാം കല്ക്കരി പ്രത്യേക വിധത്തില് അടച്ച പാത്രത്തില് 7 മിനിട്ട് നേരം 925°C-ല് ചൂടാക്കുമ്പോള് നഷ്ടപ്പെടുന്ന ഭാരം ബാഷ്പശീലമുള്ള പദാര്ഥത്തിന്റെ ഭാരമായിരിക്കും.
d. സ്ഥിരകാര്ബണ്. ആകെ ഭാര(100%)ത്തില് നിന്ന് ചാരം, ബാഷ്പശീലമുള്ള പദാര്ഥം, ജലാംശം എന്നിവയുടെ ഭാരശതമാനം കുറച്ചാല് സ്ഥിരകാര്ബണിന്റെ ഭാരശതമാനം ലഭിക്കും.
e. മൂലകവിശ്ലേഷണം. ഉയര്ന്നതോതില് കല്ക്കരി ഉപയോഗിക്കുന്നവര്ക്ക് വിവിധയിനം കല്ക്കരികളെക്കുറിച്ചുള്ള കൂടുതല് വിവരം ആവശ്യമായതുകൊണ്ട് മുന്വിവരിച്ചവയില്നിന്ന് വ്യത്യസ്തമായ പരീക്ഷണം ആവശ്യമായി വന്നു. അതുകൊണ്ട് കാര്ബണ്, ഹൈഡ്രജന്, ഓക്സിജന്, നൈട്രജന്, ഗന്ധകം എന്നീ മൂലകങ്ങളും ചാരവും അടിസ്ഥാനമാക്കിയുള്ള രാസവിശ്ലേഷണം നിലവില്വന്നു.
കാര്ബണിന്റെയും ഹൈഡ്രജന്റെയും അളവ് നിശ്ചയിക്കുന്നതിന് 0.2 ഗ്രാം കല്ക്കരി ഓക്സിജന്റെ സാന്നിധ്യത്തില് കത്തിക്കുന്നു. ദഹനോത്പന്നങ്ങള് 800°C ഉള്ള കോപ്പര്ഓക്സൈഡില്ക്കൂടിയും പിന്നീട് 600°C ഉള്ള ലെഡ്ക്രോമേറ്റില്ക്കൂടിയും കടത്തിവിട്ട് സള്ഫര്സംയുക്തങ്ങളെ ആഗിരണം ചെയ്യുന്നു. ഈ പ്രക്രിയയില് ഉത്പാദിപ്പിക്കപ്പെടുന്ന കാര്ബണ്ഡൈഓക്സൈഡിന്റെയും, ജലത്തിന്റെയും ഭാരം വെവ്വേറെ കാണാവുന്നതാണ്. ഇതില്നിന്നും കല്ക്കരിയിലുള്ള കാര്ബണിന്റെയും ഹൈഡ്രജന്റെയും ഭാരശതമാനം കണ്ടുപിടിക്കാം.
ഒരുഗ്രാം കല്ക്കരി സള്ഫ്യൂറിക് അമ്ലവുമായി പ്രതിപ്രവര്ത്തിപ്പിച്ച് നൈട്രജന്റെ ഭാരം കണക്കാക്കാം. ഇതിനെ ക്യെല്ഡാല് (kjeldahl)പദ്ധതിയെന്നു പറയുന്നു. ഈ പദ്ധതിയില് കല്ക്കരിയിലുള്ള നൈട്രജന് അമോണിയയായി രൂപാന്തരപ്പെടുന്നു. ഇതിനെ സ്വേദന(distillation)ത്തിനും ഒരു പ്രമാണ (standard) ലായനിയുമായി അനുമാപനത്തിനും വിധേയമാക്കി നൈട്രജന്റെ ഭാരം കണ്ടുപിടിക്കാം.
കല്ക്കരിയെ ചുണ്ണാമ്പും മഗ്നീഷ്യംഓക്സൈഡും ചേര്ന്ന ഉരുകല്മിശ്രവുമായി ചേര്ത്ത് ചൂടാക്കുമ്പോള് സള്ഫറിനെ സള്ഫേറ്റാക്കി രൂപാന്തരപ്പെടുത്തുന്നതിലൂടെ സള്ഫറിന്റെ ഭാരം കണ്ടുപിടിക്കാം. ഇതിനെ ഏഷാക്കാ (eschakas) പദ്ധതിയെന്നു പറയാം.
f. കേക്കിങ് സൂചകം (Caking Index). ചിലതരം കല്ക്കരി ചൂടാക്കുമ്പോള് ഉരുകി കട്ടകളാകുന്നു; ഇത് സ്റ്റോക്കറിന്റെ (stoker) പ്രവര്ത്തനത്തെ തടയും. (ഇന്ധനം ക്രമമായി കൊടുത്ത് ദഹനം നടത്താനുള്ള സംവിധാനത്തെയാണ് സ്റ്റോക്കര് എന്നു പറയുന്നത്.) കല്ക്കരിയുടെ കട്ടപിടിക്കാനുള്ള പ്രവണത താഴെ പറയുന്ന പരീക്ഷണം വഴി നിര്ണയിക്കാം.
ചൂര്ണിതകല്ക്കരി സിലിക്കാക്രൂസിബിളില് വച്ച് പ്രത്യേകാവസ്ഥയില് ചൂടാക്കുമ്പോള് കോക്ക്ബട്ടണ് ഉണ്ടാകുന്നു. ഇതിന്റെ വലുപ്പം 1 മുതല് 9 വരെ അക്കങ്ങളില് അറിയപ്പെടുന്ന പ്രമാണ രൂപങ്ങളുമായി തിട്ടപ്പെടുത്തി ഏതു നമ്പര് ആണെന്നു തീരുമാനിക്കാം. കേക്കിങ്സൂചകം എന്നു പറയുന്നത് കോക്ക്ബട്ടന്റെ ഏറ്റവും കൂടിയ പരിച്ഛേദകവിസ്തീര്ണത്തോട് ബന്ധപ്പെട്ടിരിക്കുന്ന പ്രമാണപരിച്ഛേദകത്തിന്റെ അക്കമാണ്.
g. കലോറികമൂല്യം. ഇന്ധനം പ്രധാനമായി ഉപയോഗിക്കുന്നത് താപ-ഉത്പാദനത്തിന് ആയതിനാല് കലോറികമൂല്യനിര്ണയം വളരെ പ്രാധാന്യമര്ഹിക്കുന്നു. ഒരു ഏകകപിണ്ഡമുള്ള ഖര-ദ്രവ ഇന്ധനമോ, ഏകകവ്യാപ്തമുള്ള വാതകഇന്ധനമോ പരിപൂര്ണമായി ദഹിപ്പിച്ചതിനു ശേഷം അന്തരീക്ഷ ഊഷ്മാവിലേക്ക് തണുപ്പിച്ചാല് ലഭിക്കുന്ന താപത്തെയാണ് മൊത്തം കലോറികമൂല്യമെന്നു പറയുന്നത് (gross calorific value).
ഇപ്രകാരം കണക്കാക്കപ്പെടുന്ന കലോറികമൂല്യത്തില് ബാഷ്പം ദ്രവീകരിക്കപ്പെടുന്നതുകൊണ്ട് ജലത്തിന്റെ ബാഷ്പീകരണലീനതാപം (latent heat of vaporization) കൂടി അടങ്ങിയിരിക്കും. മൊത്തം കലോറികമൂല്യത്തില് നിന്ന് ബാഷ്പീകരണലീനതാപം കുറച്ചാല് അസല് കലോറികമൂല്യം (gross calorific value) ലഭിക്കുന്നു.
കലോറികമൂല്യം കൃത്യമായി നിര്ണയിക്കുന്നതിനുള്ള ഉപകരണമാണ് ബോംബ്കലോറിമീറ്റര്. ഒരു ഗ്രാം നേരിയ കല്ക്കരിപ്പൊടി ചെറിയ ഗുളികരൂപത്തിലാക്കി വായുനിബദ്ധമായ ഒരു ലോഹബോംബില് അടക്കം ചെയ്യുന്നു; 25 അന്തരീക്ഷമര്ദമുള്ള ഓക്സിജന് ബോംബില് നിറച്ചശേഷം, വെള്ളം നിറച്ച ഊഷ്മമാപി(calorimeter)യില് താഴ്ത്തുന്നു; വൈദ്യുതസ്ഫുലിംഗം ഉപയോഗിച്ച് ഇന്ധനം കത്തിക്കുന്നു. ദഹനപ്രക്രിയയില് ഉത്പാദിപ്പിക്കപ്പെടുന്ന താപം ഊഷ്മമാപിയിലെ ജലത്തിന്റെ താപവര്ധനവില്നിന്നു കണ്ടുപിടിക്കാം. വിവിധ ഇന്ധനങ്ങളുടെ കലോറികമൂല്യം അതിന്റെ തരമനുസരിച്ചും ജലാംശത്തിന്റെ തോതനുസരിച്ചും വ്യത്യാസപ്പെട്ടിരിക്കും. ഖര ഇന്ധനങ്ങളുടെ കലോറികമൂല്യം ഏകദേശം 3,000 മുതല് 15,000 വരെ BTU/റാത്തല് ആണ്.
കല്ക്കരിയുടെ ഘടന
കല്ക്കരിയുടെ ഘടന (Constitution of Coal). ഏകദേശവിശ്ലേഷണവും മൂലകവിശ്ലേഷണവും കല്ക്കരിയുടെ രാസഘടനയെക്കുറിച്ച് വിവരങ്ങളൊന്നും തരുന്നില്ല; അതുകൊണ്ട് കല്ക്കരിയുടെ തന്മാത്രിക ഘടന (Molecular Structure) കണ്ടുപിടിക്കുന്നതിന് രാസഭൗതികക്രിയകള് ഉപയോഗപ്പെടുത്തിവരുന്നു. താഴെ പറയുന്ന പരീക്ഷണങ്ങളാണ് പ്രധാനമായി ഉപയോഗിക്കുന്നത്:
a. ലായകനിഷ്കര്ഷണം (Solvent Extraction). ഉന്നതമര്ദത്തില് ബെന്സീന് (Benzene) ഉപയോഗിച്ച് നിഷ്കര്ഷണം ചെയ്യുമ്പോള് കല്ക്കരിയെ കേക്കിങ് സ്വഭാവമുള്ളതാക്കുന്ന ഘടകങ്ങളെ വേര്തിരിച്ചെടുക്കാന് സാധിക്കുന്നു.
b. അഭികര്മക (Reagent) പ്രതിക്രിയ. നിയന്ത്രിത ഓക്സീകരണം, ഹൈഡ്രൊജനീകരണം (Hydrogenation), ക്ലോറിനീകരണം(chlorination), മെഥിലീകരണം (methylation) തുടങ്ങിയവ ഇവയില്പ്പെടുന്നു.
c. സൂക്ഷ്മദര്ശിനി ഉപയോഗിച്ചുള്ള പരിശോധന
d. എക്സ്-റേ പരിശോധന
e. സൂക്ഷ്മമായി നിയന്ത്രിക്കപ്പെട്ട ഭഞ്ജകസ്വേദനം
ബെന്സീന് നിഷ്കര്ഷണത്തിനുശേഷമുള്ള അവശേഷങ്ങളെ ഓക്സീകരിച്ചപ്പോള് ബോണിന് (W.A. Bone)ഗണ്യമായ അളവില് ബെന്സീന് കാര്ബോക്സിലിക് അമ്ലവും മറ്റ് സദൃശങ്ങളായ സംയുക്തങ്ങളും ലഭിക്കുകയുണ്ടായി. ഇതില്നിന്നും കല്ക്കരിയുടെ ഒരു പ്രധാന അംശം 6-കാര്ബണ്വലയഘടനയോടുകൂടിയതാണെന്ന് അനുമാനിക്കപ്പെട്ടു.
പൈറോള് (pyrrole), ഫ്യൂറാന് (furan) തുടങ്ങിയവയുടെയോ അവയുടെ വ്യുത്പന്നങ്ങളുടെയോ ഘടനകളാല് ബന്ധിക്കപ്പെട്ട ബെല്സിനോയ്ഡ് ഗ്രൂപ്പും ഉള്ളതായി കണ്ടു.
പീറ്റ്
സെല്ലുലോസില്നിന്നുള്ള കല്ക്കരിയുടെ രൂപാന്തരണത്തിലെ ആദ്യത്തെ അവസ്ഥയാണ് പീറ്റ്. കുഴിച്ചെടുത്ത അവസ്ഥയില് 80 മുതല് 90 വരെ ശതമാനം ജലാംശം ഉണ്ടായിരിക്കും; ഉണക്കിയ പീറ്റില് 6 ശതമാനം മുതല് 15 ശതമാനം വരെയും. ജലാംശം കോശ(cell)ഘടനകളിലായി കാണപ്പെടുന്നതുകൊണ്ട് ഉണക്കുക പ്രയാസമാണെങ്കിലും, ഉണക്കിയ പീറ്റ് ഉപയോഗിക്കാന് എളുപ്പമാണ്. ഇതിന്റെ കലോറികമൂല്യം ഏകദേശം 5,000 മുതല് 10,000 വരെ BTU/റാത്തല് ആണ്; വിറകിനെക്കാള് കലോറികമൂല്യം അല്പം കൂടുമെന്നുമാത്രം. പീറ്റ് കുഴിച്ചെടുക്കലും ഉണക്കലും ചെലവേറിയതായതുകൊണ്ട് കല്ക്കരിപോലെ കുഴിച്ചെടുക്കപ്പെടുന്നില്ല; ചില രാജ്യങ്ങളില് ബ്രിക്കറ്റ് ആക്കി ഗാര്ഹികാവശ്യങ്ങള്ക്ക് ഉപയോഗിക്കുന്നുണ്ട്.
ലിഗ്നൈറ്റ്
പീറ്റിനും ബിറ്റ്യൂമിനീയ കല്ക്കരിക്കും മധ്യേയാണ് ലിഗ്നൈറ്റിന്റെ സ്ഥാനം. കുഴിച്ചെടുത്ത അവസ്ഥയില് 20 ശതമാനം മുതല് 45 ശതമാനംവരെ ജലാംശം കാണപ്പെടുന്നു. അസംസ്കൃത ലിഗ്നൈറ്റ് രണ്ടു തരത്തില് കാണപ്പെടുന്നു; തവിട്ടു കല്ക്കരി (brown coal), കറുത്ത കല്ക്കരി (black coal). ലിഗ്നൈറ്റിന് അപക്ഷയം (weathering) സംഭവിക്കുമ്പോള് ജലാംശത്തിന്റെ നല്ലൊരു പങ്ക് നഷ്ടപ്പെടുന്നു; അപ്പോള് പൊടിഞ്ഞുപോകുകയും ചെയ്യുന്നു. ദഹനസമയത്തും പൊടിഞ്ഞുപോകാന് സാധ്യതയുള്ളതുകൊണ്ട് ഗ്രേറ്റില് (grate)കൂടിയുള്ള നഷ്ടം താരതമ്യേന അധികമാണ്. ലിഗ്നൈറ്റ് സ്വതഃദഹനത്തിനു (spontaneous combustion) വിധേയമാകുന്നതുകൊണ്ട് തുറന്ന സ്ഥലത്ത് സൂക്ഷിച്ചുവയ്ക്കാറില്ല. ലിഗ്നൈറ്റിന്റെ കലോറികമൂല്യം ഏകദേശം 6,000 മുതല് 12,000 വരെ BTU/റാത്തല് ആണ്. ബ്രിക്കറ്റ് ആക്കിയും ഇത് ഉപയോഗിക്കുന്നുണ്ട്. ലോകത്തിലെ കല്ക്കരിസമ്പത്തില് പകുതിയോളം ലിഗ്നൈറ്റ് ആണെന്നു കണക്കാക്കപ്പെട്ടിരിക്കുന്നു.
സബ്-ബിറ്റ്യൂമിനീയ കല്ക്കരി
ലിഗ്നൈറ്റിനും ബിറ്റ്യൂമിനീയ കല്ക്കരിക്കും മധ്യേയുള്ള ഇനമാണിത്. ഇത് കോക്കിങ്ങിനു വിധേയമല്ലാത്തതും എളുപ്പം പൊടിഞ്ഞുപോകുന്നതും ആയ പദാര്ഥമാണ്. ലിഗ്നൈറ്റിനെക്കാള് കാഠിന്യവും സാന്ദ്രതയും ഏറിയിരിക്കും. ഏകദേശം 12 ശതമാനം മുതല് 25 ശതമാനം വരെ ജലാംശം കാണപ്പെടുന്നു.
ബിറ്റ്യൂമിനീയ കല്ക്കരി
ഏറ്റവുമധികം ഉപയോഗിക്കപ്പെടുന്ന ഇനമാണിത്; വായുവിന്റെ അസാന്നിധ്യത്തില് ചൂടാക്കുമ്പോള് "ബിറ്റ്യൂമന്'(bitumen)എന്ന പദാര്ഥത്തോട് സാദൃശ്യമുള്ള കറുത്ത ടാര് ഉണ്ടാവുന്നതുകൊണ്ടാണ് അതിന് "ബിറ്റ്യൂമിനീയ' കല്ക്കരി എന്ന പേരുണ്ടായത്. സാന്ദ്രവും കഠിനവുമായ ഈ കല്ക്കരിക്ക് വായുവില് അപക്ഷയം സംഭവിക്കുന്നില്ല. ജലാംശം ലിഗ്നൈറ്റിനെക്കാളും, സബ്-ബിറ്റ്യൂമിനീയ കല്ക്കരിയെക്കാളും കുറവാണ് (ഏകദേശം 3%). ബിറ്റ്യൂമിനീയ കല്ക്കരിയുടെ കലോറികമൂല്യം 8,000 മുതല് 15,000 വരെ BTU/റാത്തല് ആണ്.
ഇതില് കോക്കിങ്ങിനു യോജ്യമായതും അല്ലാത്തതുമായ(coking and non-coking) ഇനങ്ങളുണ്ട്. കോക്കിങ് കല്ക്കരി ലോഹകര്മീയകോക്ക് ഉണ്ടാക്കാന് ഉപയോഗിക്കുന്നു. നീരാവിയുത്പാദനത്തിനും മറ്റു വാതകങ്ങളുടെ നിര്മാണത്തിനും ബിറ്റ്യൂമിനീയ കല്ക്കരി ഉപയോഗിക്കാം.
ആന്ഥ്റസൈറ്റ്
കല്ക്കരിയുടെ രൂപവത്കരണപ്രക്രിയയില് അവസാനത്തെ അവസ്ഥയായിട്ടാണ് ഇത് അറിയപ്പെടുന്നത്. താഴ്ന്ന ജലാംശം, ബാഷ്പശീലമുള്ള ഘടകങ്ങള്, ഉയര്ന്ന കാര്ബണ് ശതമാനം എന്നിവയാണ് സവിശേഷതകള്. താരതമ്യേന പുക കുറവായതിനാലും സാവധാനം കത്തുന്നതിനാലും ഇത് ഗാര്ഹികാവശ്യങ്ങള്ക്കും നീരാവി ഉത്പാദനത്തിനും ഉപയോഗിക്കുന്നു. പുക കുറയ്ക്കുന്നതിനായി ബിറ്റ്യൂമിനീയ കല്ക്കരി ആന്ഥ്റസൈറ്റുമായി ചേര്ക്കുന്നു; കോക്ക് ഉണ്ടാക്കുന്നതിനായി കോക്കിങ്ങിന് യോജ്യമായ ബിറ്റ്യൂമിനീയ കല്ക്കരിയുമായി കൂട്ടിക്കലര്ത്തുന്നു.
കോക്ക്
വായുസമ്പര്ക്കമില്ലാതെ കല്ക്കരിയെ സ്വേദനം ചെയ്യുമ്പോഴോ കാര്ബണീകരിക്കുമ്പോഴോ ലഭിക്കുന്ന അവശിഷ്ടപദാര്ഥമാണ് കോക്ക്; ഇതുകൂടാതെ ബാഷ്പശീലമുള്ള വസ്തുക്കളും ഉണ്ടാകുന്നു. കോക്കിങ്ങിനു യോജ്യമായ ബിറ്റ്യൂമിനീയ കല്ക്കരിയോ അതിന്റെ കൂട്ടോ (blend) ആണ് ഇതിനുപയോഗിക്കുന്നത്. കോക്ക് ഉത്പാദിപ്പിക്കുന്നതിന് രണ്ടുതരം പ്രക്രിയകളുണ്ട്: ഉന്നതതാപകാര്ബണീകരണവും (high temperature carbonization) നിമ്നതാപകാര്ബണീകരണവും (low temperature carbonization).
കല്ക്കരിയെ 900°C-1100°C വരെയുള്ള താപനിലയില് ചൂടാക്കുന്ന പ്രക്രിയയെയാണ് ഉന്നതതാപ കാര്ബണീകരണം എന്നു പറയുന്നത്. ഈ പ്രക്രിയയില് ലഭിക്കുന്ന കോക്ക് ലോഹസംസ്കരണത്തിന് ഉപയോഗിക്കുന്നതുകൊണ്ട് ലോഹകര്മീയ കോക്ക് (meta-llurgical coke)എന്നു പറയുന്നു. വാതകച്ചൂളയില് ഉപയോഗിക്കുന്ന ഏതു ഭാരവും താങ്ങാനുള്ള കഴിവാണ് അതിന്റെ പ്രധാന ഗുണം.
വാതകനിര്മാണത്തിനുവേണ്ടി ഉന്നതതാപത്തില് കല്ക്കരിയെ വാലുക(retort))യിലിട്ട് കാര്ബണീകരിക്കുമ്പോള് ലഭിക്കുന്ന ഉപോത്പന്നമാണ് വാതകക്കോക്ക് (gas coke). ഗാര്ഹികാവശ്യങ്ങള്ക്കും നീരാവി ഉത്പാദിപ്പിക്കാനും ലോഹസംസ്കരണ ചൂളയിലെ ഇന്ധനമായിട്ടും വാതകക്കോക്ക് ഉപയോഗിക്കാം.
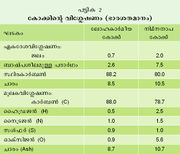
ഏകദേശം 600°C-ല് കല്ക്കരി കാര്ബണീകരിക്കുന്നതിനെയാണ് നിമ്നതാപകാര്ബണീകരണമെന്നു പറയുന്നത്. ഇപ്രകാരം ലഭിക്കുന്ന കോക്കില് 10 ശതമാനം മുതല് 15 ശതമാനം വരെ ബാഷ്പശീല പദാര്ഥം കാണപ്പെടുന്നു. ലോഹകര്മീയ കോക്കിലോ വാതകക്കോക്കിലോ കാണപ്പെടുന്ന 2-3 ശതമാനത്തെക്കാള് അധികമാണിത്. അതുകൊണ്ട് ഗാര്ഹികാവശ്യങ്ങള്ക്കും ചെറുകിടവ്യാവസായികാവശ്യങ്ങള്ക്കുംവേണ്ടി, വേഗത്തില് കത്തുന്നതും താരതമ്യേന പുക കുറഞ്ഞതുമായ, ഇന്ധനങ്ങള് നിര്മിക്കുന്നതിന് നിമ്നതാപകാര്ബണീകരണം ഉപയോഗിക്കുന്നു. ലോഹകര്മീയ കോക്കിന്റെയും നിമ്നതാപ കോക്കിന്റെയും ഏകദേശവിശ്ലേഷണവും മൂലകവിശ്ലേഷണവും പട്ടിക 2-ല് ചേര്ത്തിരിക്കുന്നു.
സുഷിരമയമായ കോക്കിന് ഓക്സിജനുമായി ചേര്ന്ന് എളുപ്പത്തില് കത്തുവാന് കഴിയും. കല്ക്കരിയിലെ ചില അംശങ്ങള് ബാഷ്പീകരിക്കുമ്പോഴുണ്ടാകുന്ന കുമിളകളില്നിന്നാണ് സരന്ധ്രഘടന (porosity) സംഭവിക്കുക. ഇത് കല്ക്കരി എത്ര നേര്മയായി പൊടിക്കുന്നു എന്നതിനെയും ചൂടാക്കുമ്പോഴുണ്ടാകുന്ന പരിതഃസ്ഥിതിയെയും ഉപയോഗിക്കുന്ന കല്ക്കരിയുടെ തരത്തെയും ആശ്രയിച്ചിരിക്കുന്നു.
കോക്കിന്റെ പ്രകടവും യഥാര്ഥവുമായ ആപേക്ഷിക സാന്ദ്രതകളും സരന്ധ്രതയും നിര്ണയിക്കാനുള്ള പരീക്ഷണങ്ങള് ഉണ്ട്. കോക്കിന്റെ ബലം അളക്കുന്നത് ഷാറ്റര്പരീക്ഷണമുപയോഗിച്ചാണ്. 50 റാത്തല് ഭാരവും, രണ്ടിഞ്ച് വലുപ്പവുമുള്ള കോക്ക് നാലുതവണ ആറടി ഉയരത്തില്നിന്നും താഴെയുള്ള ഇരുമ്പുഷീറ്റിലേക്കിടുമ്പോള് എത്ര പങ്ക് പൊടിഞ്ഞുപോയെന്ന് കണക്കാക്കുന്നു; ഇത് അടിസ്ഥാനമാക്കിയാണ് ഷാറ്റര്സൂചകം നിര്ണയിക്കുന്നത്.
രണ്ടു പ്രക്രിയകളിലും ഉത്പാദകവസ്തുക്കള് ഒന്നുതന്നെയാണെങ്കിലും അവയുടെ അളവ് വ്യത്യസ്തങ്ങളായിരിക്കും. നിമ്നതാപത്തിലുള്ള നിര്മാണരീതിയില് വാതകോത്പന്നങ്ങള് കുറവും ദ്രാവകോത്പന്നങ്ങള് കൂടുതലുമായിരിക്കും; എന്നാല് ഉന്നതോഷ്മാവില് നേരേതിരിച്ചാണ്. പുകയില്ലാതെ കത്തുന്നതും ചാരത്തിന്റെ അംശം വളരെ കുറവുള്ളതുമായ ഈ ഇന്ധനത്തിന്റെ താപമൂല്യം ഏകദേശം 13,400 BTU/റാത്തല് ആണ്.
ബ്രിക്കറ്റ്
വളരെ നേര്ത്ത കല്ക്കരിപ്പൊടി സംബന്ധകവസ്തു(binder)ക്കളുടെ സാന്നിധ്യത്തിലോ അല്ലാതെയോ, മര്ദത്തിന്റെ സഹായത്താല് കട്ടകളാക്കുന്നതിനെയാണ് ബ്രിക്കറ്റിങ് (briquetting) എന്നു പറയുന്നത്. ഇപ്രകാരം പീറ്റ്, ലിഗ്നൈറ്റ് എന്നീ ഇനങ്ങളെ ബ്രിക്കറ്റുകളാക്കുന്നു.
പഞ്ചസാര വ്യവസായത്തില്നിന്നു ലഭിക്കുന്ന മൊളാസസ് (molasses), സ്റ്റാര്ച്ച് ഫാക്ടറിയില്നിന്നും ലഭിക്കുന്ന ഡെക്സ്ട്രിന്പശ, കടലാസ് ഫാക്ടറിയില് നിന്നും ലഭിക്കുന്ന സള്ഫൈറ്റ് ലിക്വര് (sulphite liquor), ടാര്, അസംസ്കൃതഎണ്ണ മുതലായവ സംബന്ധകവസ്തുക്കളായി ഉപയോഗിക്കാം. ബ്രിക്കറ്റുകള് ചതുരാകൃതിയിലോ മുട്ടയുടെ ആകൃതിയിലോ ആകാം. ഏകദേശം 5 മുതല് 10 വരെ ശതമാനം സംബന്ധകവസ്തുക്കളും റോള്പ്രസ്സുകളും ഉപയോഗിച്ച് കട്ടകളാക്കുന്നു.
മുന്തിയയിനം ബ്രിക്കറ്റുകള് ബലമുള്ളതും, ജലരോധകശക്തിയുള്ളതും ആയിരിക്കും. സംബന്ധകവസ്തുവിന്റെ കലോറികമൂല്യം, ഉപയോഗിച്ച കല്ക്കരിയുടേതിനെക്കാള് കൂടുതലാണെങ്കില്, ബ്രിക്കറ്റിന്റെ കലോറികമൂല്യവും കൂടിയിരിക്കും. ഇവ വ്യാവസായികാവശ്യങ്ങള്ക്ക് ഉപയോഗിക്കുന്നുണ്ടെങ്കിലും പ്രധാനമായും പ്രയോജനപ്പെടുത്തുന്നത് ഗാര്ഹികാവശ്യങ്ങള്ക്കാണ്.
പൊടിയാക്കിയ കല്ക്കരി (Pulverized coal)
പൊടിച്ച കല്ക്കരി വായുവുമായി കൂട്ടിക്കലര്ത്തിയാല് വേഗത്തിലും പരിപൂര്ണമായും കത്തുന്നു. അതുകൊണ്ട് കാര്യക്ഷമമായ ദഹനത്തിന് കല്ക്കരി നന്നായി പൊടിച്ച് ഉപയോഗിക്കുന്നു. ദ്രവ ഇന്ധനങ്ങളെപ്പോലെ ഇവയെ കത്തിക്കാം.
പൊടിയാക്കിയ കല്ക്കരി ഇന്ധനമായി ഉപയോഗിക്കുമ്പോള് പല ഗുണങ്ങളുമുണ്ട്. ഏതുതരം ഖര ഇന്ധനവും ഉപയോഗിക്കാം; കല്ക്കരിപ്പൊടി ഉപയോഗിക്കുന്ന ചൂളയില് ചില ചെറിയ മാറ്റങ്ങള് വരുത്തി വാതക ഇന്ധനമോ ദ്രവ ഇന്ധനമോ ഉപയോഗിക്കാം. ജ്വലനം ആരംഭിക്കാനും നിര്ത്താനും വളരെക്കുറച്ചു സമയം മാത്രമേ ആവശ്യമുള്ളൂ.
കല്ക്കരിപ്പൊടി സാധാരണ വായുപ്രവാഹത്തിലൂടെ ചൂളയിലേക്ക് കയറ്റുന്നു. ജ്വാലകത്തില്(burner)വച്ച് രണ്ടാംഘട്ടത്തിലുള്ള വായു(secondary air)വുമായി ചേര്ന്ന് ചൂളയിലേക്ക് വീഴുകയും അവിടെ നിലംബിത (suspended) അവസ്ഥയില് ജ്വലിക്കുകയും ചെയ്യുന്നു.
പൊടിച്ച കല്ക്കരിയുടെ ദഹനത്തിന് സാധാരണ പരിപൂര്ണദഹനത്തിനു വേണ്ടുന്നതില് അല്പംകൂടുതല് വായുമാത്രമേ ആവശ്യമുള്ളൂ. ചൂളയിലേക്ക് നല്കുന്നതിനുമുമ്പ് ഈ വായുവിനെ ഉന്നത ഊഷ്മാവിലേക്ക് ഉയര്ത്തിയാല് ബോയിലറിന്റെ ക്ഷമത വര്ധിക്കും. പൊടിച്ച കല്ക്കരിയിലെ ചാരത്തിന്റെ അംശം അതിന്റെ സമ്പൂര്ണദഹനത്തിന് തടസ്സമാണ്. കല്ക്കരി നേരിയ പൊടിയായി ഉപയോഗിക്കുന്നതിനാല് ദഹനപ്രക്രിയയ്ക്കുശേഷം ഉണ്ടാകുന്ന ചാരം (fly ash) നിര്ഗമവാതകങ്ങളില്ക്കൂടി പുറത്തുപോകുകയും അന്തരീക്ഷത്തെ മലിനപ്പെടുത്തുകയും ചെയ്യുന്നു. അവക്ഷേപകങ്ങള് (precipitators) ഉപയോഗിച്ച് ചാരം പുറത്തുപോകുന്നത് തടയാം.
ചൂളയിലെ ഊഷ്മാവ് വളരെയധികമാകുകയാണെങ്കില് ചാരം ഉരുകി ബോയിലര്ട്യൂബിന്റെ പുറത്തു പറ്റിപ്പിടിക്കുകയും താപപ്രസരണത്തിന് അതു തടസ്സം സൃഷ്ടിക്കുകയും ചെയ്യുന്നു.
ചൂള തെരഞ്ഞെടുക്കുന്നതിലും അതിന്റെ വ്യാപ്തം തീരുമാനിക്കുന്നതിലും പ്രധാന ഘടകമാണ് ചാരം ഉരുകുന്ന ഊഷ്മാവ്. വളരെ താഴ്ന്ന ഊഷ്മാവില് ഉരുകുന്ന ചാരമാണെങ്കില് ജ്വാലയില്വച്ച് ഉരുകുകയും ചൂളയുടെ ഭിത്തികളില് പറ്റിപ്പിടിക്കുകയും ചെയ്യുന്നു. ഇങ്ങനെ ഉണ്ടാകുന്ന അട്ടികള് ഭാരം കൂടുമ്പോള് അസ്തരങ്ങളുടെ (lining) കഷണങ്ങളോടുകൂടെ താഴെ വീഴുന്നു. ഇത് പരിഹരിക്കാന് ചൂളയുടെ വ്യാപ്തം കൂട്ടുകയും ട്യൂബുകളില്ക്കൂടി ജലം പ്രവഹിപ്പിച്ച് ചുമരുകളെ തണുപ്പിക്കുകയും ചെയ്യുന്നു.
കല്ക്കരി നന്നായി പൊടിക്കുന്നതുപോലെ ഉണക്കുകയും ചെയ്തില്ലെങ്കില് സൈലോകളിലും മില്ലുകളിലും മറ്റും ബുദ്ധിമുട്ടുണ്ടാക്കും. ബിന്-ആന്ഡ്-ഫീഡര് (bin-and-feeder) സമ്പ്രദായമനുസരിച്ച് കല്ക്കരി ഉണക്കി പൊടിയാക്കി വലിയ ബങ്കറുകളില് സൂക്ഷിച്ചുവയ്ക്കുന്നു; പിന്നീട് അവ ആവശ്യാനുസരണം ചൂളയിലേക്കെത്തിക്കുന്നു.
യൂണിറ്റ് (unit) സമ്പ്രദായമനുസരിച്ച് മില്ലുകളില് വച്ചുതന്നെ ഉണക്കുകയും പൊടിക്കുകയും ചെയ്യുന്നു; പിന്നീട് മുന്കൂട്ടി ചൂടാക്കിയ വായുപ്രവാഹത്തില് നേരെ ചൂളയിലേക്ക് തള്ളപ്പെടുന്നു. ഇതില് വലിയ ബങ്കറുകളുടെ ആവശ്യമില്ല.
നീരാവി ഉത്പാദനത്തിനും, സിമന്റ് ഫാക്ടറികളിലും പൊടിച്ച കല്ക്കരി ധാരാളമായി ഉപയോഗിക്കുന്നു.
വിറക്
തടി ഇന്ധനമെന്ന നിലയില്
വിറകില് പ്രധാനമായും സെല്ലുലോസും (cellulose) ചെറിയ അളവില് ലിഗ്നിന്, റെസിനുകള് (resins), അജൈവപദാര്ഥങ്ങള്, ജലം എന്നിവയും അടങ്ങിയിരിക്കുന്നു. വിറകിലെ ജലാംശം ഏകദേശം 25-50 ശതമാനം വരും. വിറക് എത്രമാത്രം ഉണങ്ങിയതാണ് എന്നതിനെ ആശ്രയിച്ചിരിക്കും അതിലെ ജലാംശത്തിന്റെ തോത്. ജലാംശം കൂടുന്നതനുസരിച്ച് താപമൂല്യം കുറയുന്നതിനാല് വ്യാവസായികാവശ്യങ്ങള്ക്ക് ഇത് ഉപയോഗിക്കുന്നില്ല. അറക്കപ്പൊടിയും വിറകിന്റെ മറ്റ് അവശിഷ്ടങ്ങളും ബോയിലറുകളില് ചിലപ്പോള് ഉപയോഗിക്കാറുണ്ട്.
മരക്കരി
വിറക് വായുസമ്പര്ക്കമില്ലാതെ ഭഞ്ജകസ്വേദനം ചെയ്യുമ്പോള് ലഭിക്കുന്ന പദാര്ഥമാണ് മരക്കരി. വിറക് മണ്ണുകൊണ്ട് മൂടി ഭാഗികമായി ദഹിപ്പിച്ചാണ് ചെറിയ തോതില് മരക്കരി ഉണ്ടാക്കുന്നത്. അടയ്ക്കാവുന്ന റിട്ടോര്ട്ടിലിട്ടാണ് വ്യാവസായികാടിസ്ഥാനത്തില് മരക്കരി ഉണ്ടാക്കുന്നത്. കാഠിന്യമേറിയ (hard) മരമാണ് മരക്കരി ഉണ്ടാക്കാന് ഉത്തമം.
മരം ഭഞ്ജകസ്വേദനം ചെയ്യുമ്പോള് ബാഷ്പങ്ങളും ടാറും മറ്റും ബഹിര്ഗമിക്കുന്നു. ശേഷിക്കുന്ന ഖരപദാര്ഥമാണ് മരക്കരി. ഉണങ്ങിയ മരത്തില്നിന്ന് ഏകദേശം 30 ശതമാനം മരക്കരി ലഭിക്കുന്നു. മരക്കരിയില് ഏകദേശം 80 ശതമാനം കാര്ബണ്, 15 ശതമാനം ഓക്സിജനും നൈട്രജനും, 2 ശതമാനം ഹൈഡ്രജന്, 3 ശതമാനം ചാരം എന്നിവ അടങ്ങിയിരിക്കുന്നു.
മരക്കരി ജലത്തെ എളുപ്പത്തില് ആഗിരണം ചെയ്യുന്നു. ഇതില് ഏകദേശം 10-15 ശതമാനം ജലാംശം കാണും. ഇതിന്റെ കലോറികമൂല്യം 12,000 മുതല് 13,000 വരെ BTU/റാത്തല് ആണ്. താഴ്ന്ന ചാരശതമാനവും, ശുദ്ധി (purity)യുംമൂലം ലോഹകര്മീയ ഇന്ധനമായി പ്രയോജനപ്പെടുന്നു; പക്ഷേ, എളുപ്പം പൊടിഞ്ഞുപോകുന്നതുകൊണ്ട് കോക്കുപോലെ ഉപയോഗയോഗ്യമല്ല.
ഖര ഇന്ധനങ്ങളുടെ ഉപയോഗം
ഖര ഇന്ധനങ്ങളുടെ ഘടനയിലും ഗുണവിശേഷങ്ങളിലും ഉള്ള വലിയ വ്യത്യാസംമൂലം കാര്യക്ഷമമായ ഉപയോഗത്തിന് അവയുടെ ഘടന, യന്ത്രസംവിധാനം എന്നിവയെക്കുറിച്ച് അനേകവര്ഷത്തെ നിരീക്ഷണങ്ങളും പരീക്ഷണങ്ങളും ആവശ്യമായി വന്നു. ഈ പരീക്ഷണങ്ങള്മൂലം ഇന്ധനങ്ങളെക്കുറിച്ചു മാത്രമല്ല, വിവിധതരത്തിലുള്ള യന്ത്രസംവിധാനങ്ങളെയും അവയുടെ പ്രവര്ത്തനങ്ങളെയുംകുറിച്ച് കൂടുതല് അറിവ് നേടാന് ഇടയായി; കൂടാതെ, വ്യാവസായികമായി ഇന്ധനങ്ങളെ വിവിധ ഗുണങ്ങളനുസരിച്ച് തെരഞ്ഞെടുക്കുന്നതിനും ഈ പരീക്ഷണങ്ങള് സഹായിച്ചു.
ഒരു ഇന്ധനത്തിന്റെ താപമൂല്യത്തിനാണ് ഏറ്റവും പ്രാധാന്യം. താപം എത്രവേഗത്തില് ഉത്പാദിപ്പിക്കാമെന്നും എത്രകണ്ട് ഉപയോഗപ്പെടുത്താമെന്നും ഉള്ളത് ഒട്ടും അപ്രധാനമല്ല.
ദഹനം
ഒരു വസ്തുവും വായുവിലെ ഓക്സിജനും തമ്മിലുള്ള അഭിക്രിയയെയാണ് ദഹനം എന്നു പറയുന്നത്. ഇന്ധനത്തിലെ കാര്ബണും ഹൈഡ്രജനും ചുരുങ്ങിയ തോതില് സള്ഫറും ഓക്സിജനുമായി പ്രതിപ്രവര്ത്തിക്കുമ്പോഴാണ് താപവും പ്രകാശവും ഉണ്ടാകുന്നത്. ശരിയായ ദഹനത്തിന് പദാര്ഥത്തെ അതിന്റെ ജ്വലനാങ്കം (ignition temperature) വരെ ചൂടാക്കണം (ഇന്ധനം ജ്വലിക്കാനാരംഭിക്കുകയും ബാഹ്യസ്രോതസ്സുകളില് നിന്നുള്ള താപം കൂടാതെതന്നെ തുടര്ന്നു കത്തുകയും ചെയ്യുന്ന ഊഷ്മാവിനെയാണ് ജ്വലനാങ്കം എന്നു പറയുന്നത്).
കാര്ബണികപദാര്ഥങ്ങളുടെ ദഹനം സങ്കീര്ണമായ പ്രക്രിയയാണ്. ഏതാനും ഘട്ടങ്ങളായിട്ടാണ് ഇത് നടക്കുന്നത്. ഇന്ധനം പരിപൂര്ണമായി കാര്ബണ്ഡൈഓക്സൈഡും ജലബാഷ്പവുമാകുന്നതിന് വേണ്ട ഓക്സിജന്റെ സൈദ്ധാന്തിക അളവ് (theoretical quantity) ഇന്ധനത്തിന്റെ മൂലകവിശ്ലേഷണത്തില്നിന്ന് കണ്ടുപിടിക്കാം.
ഇന്ധനത്തിലെ മൊത്തം ഹൈഡ്രജന്റെയും ഓക്സിജന്റെയും ഒരുഭാഗം കാര്ബണിന്റെ സംയോഗമായും മറ്റൊരു ഭാഗം ജലാംശമായും ആണ് കാണുന്നത്. ഹൈഡ്രജന്റെ വലിയൊരു ശതമാനം കാര്ബണ്സംയുക്തമായിരിക്കും. വ്യാവസായിക ഇന്ധനങ്ങളില് മൊത്തം ഹൈഡ്രജന് ഓക്സിജനുമായി ചേരുവാന് വേണ്ട ഹൈഡ്രജനെക്കാള് കൂടുതലായിരിക്കും. ഓക്സിജനുമായിച്ചേര്ന്ന ഹൈഡ്രജന്റെ അളവ് മൊത്തം ഹൈഡ്രജനില്നിന്ന് കുറച്ചാണ് ദഹനപ്രക്രിയയില് പങ്കെടുക്കുന്ന ഹൈഡ്രജന്റെ അളവ് കണക്കാക്കുന്നത്. അതിനാല് അസ്സല് ഹൈഡ്രജനാണ് (net hydrogen) ദഹനപ്രക്രിയയ്ക്ക് വിധേയമാകുന്നത്.
ദഹനത്തിന് ആവശ്യമായ ഓക്സിജനെക്കാള് കൂടുതല് അളവ് ഓക്സിജന് ചൂളയിലേക്ക് കടത്തിവിടുന്നു. ഓക്സിജന് കുറഞ്ഞുപോയാല് ചിമ്മിനിവാതകത്തില് കാര്ബണ് മോണോക്സൈഡിന്റെ അളവ് കൂടുതലായിരിക്കും. കാര്ബണ് മോണോക്സൈഡിന്റെ അളവ് വളരെ കൂടുകയാണെങ്കില് സ്വതന്ത്രാവസ്ഥയിലുള്ള ഹൈഡ്രജന് ചിമ്മിനിവാതകത്തില് ഏറിയിരിക്കും. താഴെപ്പറയുന്ന അഭിക്രിയകളാണ് ദഹനത്തില് സംഭവിക്കുന്നത്:
(a) C + O<sub>2</sub> = CO<sub>2</sub> 12 32 44
12 ഗ്രാം കാര്ബണ് 32 ഗ്രാം ഓക്സിജനുമായി ചേരുമ്പോള് 44 ഗ്രാം കാര്ബണ്ഡൈഓക്സൈഡ് ഉണ്ടാകുന്നു; ഈ അഭിക്രിയയിലുണ്ടാകുന്ന താപം ഏകദേശം 14,590 BTU/റാത്തല് ആണ്.
(b) 2C + O<sub>2</sub> = 2CO 2x12 32 2x28
24 ഗ്രാം കാര്ബണ് 32 ഗ്രാം ഓക്സിജനുമായി ചേരുമ്പോള് 56 ഗ്രാം കാര്ബണ് മോണോക്സൈഡ് ലഭിക്കുന്നു; നിര്ഗമിക്കുന്ന താപം ഏകദേശം 4,350 BTU/റാത്തല് ആണ്.
(c) 2CO + O<sub>2</sub> = 2CO<sub>2</sub> 2x28 32 2x44
56 ഗ്രാം കാര്ബണ് മോണോക്സൈഡ് 32 ഗ്രാം ഓക്സിജനുമായി ചേരുമ്പോള് 88 ഗ്രാം കാര്ബണ് ഡൈ ഓക്സൈഡ് കിട്ടുന്നു. ഒരു റാത്തല് കാര്ബണ് മോണോക്സൈഡില് നിന്ന് നിര്ഗമിക്കുന്ന താപം ഏകദേശം 4,390 BTU/റാത്തല് ആണ്.
(d) 2H<sub>2</sub> + O<sub>2</sub> = 2H<sub>2</sub>O 2x2 32 2x18
4 ഗ്രാം ഹൈഡ്രജന് 32 ഗ്രാം ഓക്സിജനുമായി ചേര്ന്ന് 36 ഗ്രാം ജലം ഉണ്ടാകുന്നു. ഇതില്നിന്നു ലഭിക്കുന്ന താപം ഏകദേശം 61,340 BTU/റാത്തല് ആണ്.
(e) S + O<sub>2</sub> = SO<sub>2</sub> 32 32 64
32 ഗ്രാം സള്ഫര് 32 ഗ്രാം ഓക്സിജനുമായി യോജിക്കുമ്പോള് 64 ഗ്രാം സള്ഫര്ഡൈഓക്സൈഡ് ഉണ്ടാകുന്നു. മോചിപ്പിക്കപ്പെടുന്ന താപമാകട്ടെ, ഒരു റാത്തല് സള്ഫറിന് ഏകദേശം 3,930 BTU ആണ്.
കാര്ബണ്, ഹൈഡ്രജന്, ഓക്സിജന് എന്നിവ നിര്ദിഷ്ട അളവില് അടങ്ങിയ ഒരു റാത്തല് കല്ക്കരി പരിപൂര്ണമായി ദഹിപ്പിക്കുന്നതിന് ആവശ്യമായ വായുവിന്റെ അളവ് താഴെപ്പറയുംവിധം കണക്കാക്കാം:
കാര്ബണ് - 78% ഹൈഡ്രജന് - 3.6% ഓക്സിജന് - 4.9% അസ്സല് ഹൈഡ്രജന് = 3.6 - 4.9 X (4/32) = 3.01% ആയതുകൊണ്ട് ദഹനത്തിനു വേണ്ടതായ ഓക്സിജന് = 0.78(32frac12;) + 0.0301(32frac4;) = 2.32 റാത്തല് 100 ഗ്രാം വായുവില് 23.2 ഗ്രാം ഓക്സിജന് ഉണ്ട്. ∴ വായുവിന്റെ ഭാരം = 2.32 x 100/23.2 = 10 റാത്തല്
ഇതുപോലെതന്നെ വായുവിന്റെ അളവുകൊണ്ട് കാര്ബണ് ഡൈ ഓക്സൈഡിന്റെ അളവ് കണക്കാക്കാം. മേല്പറഞ്ഞ സമവാക്യങ്ങളില്നിന്ന് വാതകങ്ങള് ഏതുവിധത്തില് നിര്ഗമിക്കുന്നുവെന്നോ, വാതകങ്ങള് തമ്മിലോ, ഓക്സിജനും ജലബാഷ്പവും തമ്മിലോ ഏതു വിധത്തില് പ്രതിപ്രവര്ത്തിക്കുന്നുവെന്നോ മനസ്സിലാക്കാന് കഴിയുകയില്ല. ദഹനത്തിന്റെ ക്രിയാവിധി(mechanism)കളെക്കുറിച്ചുള്ള ഗവേഷണം ഇപ്പോഴും തുടര്ന്നുകൊണ്ടിരിക്കുന്നു.
ഗാര്ഹികാവശ്യങ്ങള്
ശീതരാജ്യങ്ങളില് ചൂട് കിട്ടാന് തീക്കുണ്ഡങ്ങളിലും സ്റ്റൗവുകളിലും ഖര ഇന്ധനങ്ങളാണ് ഉപയോഗിക്കുന്നത്. ആദ്യകാലങ്ങളില് മനുഷ്യയത്നം ഉപയോഗിച്ച് ഇന്ധനം കൈകാര്യം ചെയ്തിരുന്നു. പില്ക്കാലത്ത് അത് യന്ത്രവത്കരിക്കപ്പെട്ടു. ഇതുമൂലം വേണ്ടവിധത്തില് ഇന്ധനം നിറയ്ക്കുന്നതിനും ആവശ്യാനുസരണം ചൂട് ലഭിക്കുന്നതിനും ചാരം നീക്കം ചെയ്യുന്നതിനും എളുപ്പമായി.
വ്യാവസായികാവശ്യങ്ങള്
ഏറെക്കുറെ എല്ലാത്തരം ഖര ഇന്ധനങ്ങളും വ്യവസായാവശ്യങ്ങള്ക്ക് ഉപയോഗിക്കാം. നൂതനയന്ത്രങ്ങളുടെ ആവിര്ഭാവത്തോടെ മനുഷ്യയത്നം ലഘൂകരിക്കാനും ഇന്ധനം ലാഭിക്കുവാനും കഴിഞ്ഞു. ഓരോ ഇന്ധനവും കാര്യക്ഷമമായി കത്തിക്കുന്നതിന് യന്ത്രസംവിധാനത്തില് പ്രത്യേക പരിഗണനകള് ആവശ്യമാണ്.
ഖര ഇന്ധനങ്ങള് ഇന്ധനവിതാനത്തിലോ(fuel bed) നിലംബിതമായോ (suspended)അല്ലെങ്കില് രണ്ടും ചേര്ന്നവിധത്തിലോ കത്തിക്കാം. ജ്വലനോപാധികള് തെരഞ്ഞെടുക്കുന്നത് ഇന്ധനത്തിന്റെ തരവും ആവശ്യമായ താപത്തിന്റെ അളവും സാമഗ്രിയുടെ താരതമ്യവിലയും അനുസരിച്ചായിരിക്കും.
ഇന്ധനവിതാനങ്ങളിലുള്ള ജ്വലനം ഓവര്ഫീഡ് (over feed) എന്നും അണ്ടര്ഫീഡ് (under feed) എന്നും രണ്ടുതരമായി വിഭജിക്കാം.
ഓവര്ഫീഡ് ജ്വലനത്തില് ഇന്ധനം വായുവിന്റെ പ്രവേശനത്തിന് മുകളിലായി ഗ്രേറ്റി(grate)ലേക്ക് നിറയ്ക്കുന്നു. കോരിക ഉപയോഗിച്ച് ഗ്രേറ്റിലേക്ക് ഇന്ധനം നിറയ്ക്കുന്നതും അടിയില്നിന്ന് വായു ഗ്രേറ്റിലേക്ക് വരുന്നതും ഓവര്ഫീഡ് ജ്വലനത്തിന് ഉദാഹരണമാണ്. വ്യാപന അംഗാരിത്രവും (spreader stoker) സഞ്ചാരിതഗ്രേറ്റ് അംഗാരിത്രവും (travelling grate stoker) ഈ വിഭാഗത്തില്പ്പെടുന്നു. അണ്ടര്ഫീഡിലാകട്ടെ, വിതാനത്തിലേക്കുള്ള വായുവിന്റെയും ജ്വലനതലത്തിലേക്കുള്ള ഇന്ധനത്തിന്റെയും ദിശകള് ഒരേവിധമായിരിക്കും. ഈ വിഭാഗത്തില്, ദാഹ്യവാതകങ്ങള് ധവളോജ്ജ്വലമായ മേല്വിതാനത്തിലൂടെ കടന്നുപോകുന്നതുകൊണ്ട് പരിപൂര്ണദഹനം സാധ്യമാകുന്നു. സിംഗിള്-റിട്ടോര്ട്ട് അംഗാരിത്രവും (single retort stoker)സ്ക്രൂഫീഡ് അംഗാരിത്രവും (screw-feed stoker) മറ്റും ഇതില് ഉള്പ്പെടുന്നു.
ബിറ്റ്യൂമിനീയ കല്ക്കരി ഉപയോഗിക്കുന്ന, താരതമ്യേന വലിയ അംഗാരിത്രത്തില് കുഴിച്ചെടുക്കുന്ന കല്ക്കരിയിലെ വലിയ കഷണങ്ങള് നീക്കം ചെയ്തശേഷമാണ് ഉപയോഗിക്കുന്നത്; ചെറിയ അംഗാരിത്രത്തില് കല്ക്കരിയിലെ ചെറിയ തരികളാണു നീക്കം ചെയ്യുന്നത്.
ബ്ലാസ്റ്റ് ഫര്ണസ്
ഉരുക്കുന്നതിനും ഭര്ജിക്കുന്നതിനും(roast), നീരോക്സീകരിക്കുന്നതിനും ഉപയോഗിക്കുന്നതും ലംബരൂപമുള്ളതും, തുടര്ച്ചയായി പ്രവര്ത്തിക്കുന്നതുമായ ഉരുക്കുചൂളയെയാണ് ബ്ലാസ്റ്റ് ഫര്ണസ് എന്നു പറയുന്നത്; ഇതിനെ വാതകച്ചൂളയെന്നും പറയാം. ഇരുമ്പയിരിനെ ഉരുക്കി കാരിരുമ്പ് (pig iron) ആക്കുന്നതിനാണ് ഇത് പ്രധാനമായി ഉപയോഗിക്കുന്നത്. ഒരു ആധുനിക വാതകച്ചൂളയുടെ വ്യാസം ഏകദേശം 9 മീറ്ററും ഉയരം 27-34 മീറ്ററും വരും. പ്രതിദിന ഉത്പാദനം ഏകദേശം 1,000 ടണ് കാരിരുമ്പും ആയിരിക്കും. ഇതിലുപയോഗിക്കുന്ന കോക്ക് നിര്ദിഷ്ട മേന്മയും ആകൃതിയും ബലവും ഉള്ളതായിരിക്കണം; ഇത് ഒരേ സമയം ഇന്ധനമായും നിരോക്സീകാരിയായും വര്ത്തിക്കുന്നു.
ഉന്നത ഊഷ്മാവിലുണ്ടാകുന്ന കോക്കിന്റെ സുഷിരത, സാന്ദ്രത മുതലായവയാണ് അതിനെ വാതകച്ചൂളയ്ക്കു പറ്റിയതാക്കുന്നത്. ഈ ചൂളയില് ഉപയോഗിക്കുമ്പോള് കോക്കിന്റെ തരിയും പൊടിയും ഒഴിവാക്കേണ്ടതാണ്. 10 സെ.മീ. വലുപ്പമുള്ള കോക്കുപയോഗിക്കുന്നതാണ് അഭികാമ്യം. ഇത്തരം കോക്കില് ബാഷ്പശീലമുള്ള പദാര്ഥം 2 ശതമാനവും സ്ഥിരകാര്ബണ് 85 ശതമാനം മുതല് 90 ശതമാനം വരെയും, സള്ഫര് 0.6 ശതമാനം മുതല് 1.5 ശതമാനം വരെയും ആയിരിക്കും. ചാരത്തിന്റെ ശതമാനം 8 മുതല് 16 വരെ ആകാമെങ്കിലും, 12 ശതമാനത്തില് കൂടാതിരിക്കുന്നതാണ് അഭികാമ്യം. ചാരം കുറയ്ക്കുന്നതിനനുസരിച്ച് വാതകച്ചൂളയില്നിന്നുള്ള ഇരുമ്പിന്റെ ഉത്പാദനം കൂടുന്നു. കോക്കിലുള്ള ജലാംശം 5 ശതമാനത്തില് താഴെയാകണം. വാതകച്ചൂളയിലേക്ക് കടത്തിവിടുന്ന വായു ഒരു മിനിട്ടില് 70,000 പ്രമാണ ഘന അടി (standard cubic foot)ആയിരിക്കും. ഈ വായു 900°F-നും 1,200°Fഎനും മധ്യേ മുന്കൂട്ടി ചൂടാക്കി, 15 psi മര്ദത്തില് കടത്തിവിടുന്നു. ഇങ്ങനെ മുന്കൂട്ടി ചൂടാക്കുന്നതിന് നാല് സ്റ്റൗവുകള് അടങ്ങുന്ന ഒരു സെറ്റാണ് ഉപയോഗിക്കുന്നത്. ഇതിനുപയോഗിക്കുന്ന സ്റ്റൗവിന്റെ ഉയരം 30 മീറ്ററും വ്യാസം 6.6 മീറ്ററും ആയിരിക്കും.
മേല്പറഞ്ഞ തരത്തിലുള്ള ഒരു ചൂളയില് 2,000 ടണ് ഇരുമ്പയിരും 100 ടണ് കോക്കും 500 ടണ് ചുണ്ണാമ്പുകല്ലുമാണ് ഉപയോഗിക്കുന്നത്. ഈ പദാര്ഥങ്ങള് യഥാനുപാതം ഇടവിട്ട് ചൂളയുടെ മുകള്ഭാഗത്തുകൂടി നിറയ്ക്കുന്നു. ചൂളയില്നിന്ന് ഇരുമ്പും കിട്ടവും (slag)പുറത്തെടുക്കുന്നതിനനുസരിച്ച് അസംസ്കൃതപദാര്ഥങ്ങള് ചൂളയില് നിറച്ചുകൊണ്ടിരിക്കണം.
ദ്രവ ഇന്ധനങ്ങള്
പ്രാഥമിക ഹൈഡ്രാകാർബണുകളുടെയും (Hydrocarbons)കൊർബണിക സംയുക്തങ്ങളുടെയും മിശ്രിതത്തെയാണ് പെട്രാളിയം (petroleum) അഥവാ അസംസ്കൃതഎച്ച (crude oil) എന്നു പറയുന്നത്. സൂക്ഷ്മസമുദ്രജീവികളിൽ നിന്നും സസ്യങ്ങളിൽനിന്നുമാണ് പെട്രാളിയം ഉണ്ടായതെന്ന് വ്യക്തമാണ്. ഈ ജീവജാലങ്ങള് നശിച്ചപ്പോള് ജലത്തിൽവച്ച് ഓക്സിജന്റെ (oxygen)അഭാവംമൂലം അഴുകാന് ഇടയായില്ല; പകരം അടിത്തട്ടിൽ അടിഞ്ഞുകൂടി. ആധുനിക സിദ്ധാന്തപ്രകാരം ജീവാണുക്കള് (Bacteria)ഈ പദാർഥത്തിലുള്ള കൊഴുപ്പിനെ സ്നേഹാമ്ലം (fatty acid) ആക്കി മാറ്റുകയും പിന്നീട്, അറിയപ്പെടാത്ത ഒരു പ്രക്രിയയാൽ കെറോജന് (kerogen)എന്ന ദ്രവ്യം ഉണ്ടാകുകയും ചെയ്യുന്നു. തുടർന്ന് കോടിക്കണക്കിന് വർഷങ്ങളിലെ താപ-മർദ ആഘാതംമൂലം പെട്രാളിയം ഉണ്ടായി.
ചരിത്രാതീതകാലം മുതൽ ദ്രാവക ഇന്ധനങ്ങള് ഉപയോഗത്തിലുണ്ടായിരുന്നു. സസ്യഎച്ചകളും കൊഴുപ്പുകളും വിളക്കു കത്തിക്കാന് പ്രയോജനപ്പെടുത്തി വന്നു. 19-ാം ശതകത്തിന്റെ ആദ്യഘട്ടത്തിൽപ്പോലും തിമിംഗലഎച്ച പ്രചാരത്തിലുണ്ടായിരുന്നു. പക്ഷേ, അവയ്ക്കൊന്നും വർധിച്ചുവരുന്ന ആവശ്യങ്ങള് നിറവേറ്റാന് കഴിഞ്ഞില്ല. 19-ാം ശതകത്തിന്റെ അന്ത്യത്തോടെ മച്ചെച്ച തിമിംഗല എച്ചയുടെ സ്ഥാനം പിടിച്ചുപറ്റി. 1847-ൽ ജെയിംസ് എച്ച്. യങ് സ്കോട്ട്ലന്ഡിൽ എച്ചപ്പാളികളിൽ(shale) നിന്ന് എച്ച ഉത്പാദിപ്പിച്ചു. 1859-ൽ പെന്സിൽവേനിയയിൽ യന്ത്രശക്തി ഉപയോഗിച്ചുള്ള ആദ്യത്തെ എച്ചക്കിണർ നിലവിൽ വന്നു. പെട്രാളിയം ഉത്പന്നങ്ങളുടെ മുന്നേറ്റം 20-ാം ശതകത്തിന്റെ മധ്യത്തോടുകൂടി മറ്റു ദ്രവ ഇന്ധനങ്ങളുടെ പ്രാധാന്യം കുറച്ചു.
പെട്രാളിയം
പെട്രാളിയം നേരിട്ട് ഒരു ഇന്ധനമായി ഉപയോഗിക്കപ്പെടുന്നില്ല. പക്ഷേ, അത് വ്യാവസായിക ദ്രവ ഇന്ധനങ്ങളുടെ ഉത്പാദനത്തിന് അടിസ്ഥാനം കുറിക്കുന്നു. ആന്തരദഹനയന്ത്രങ്ങളുടെയും(internal combustion engines) മോട്ടോർകാറുകളുടെയും ആവിർഭാവത്തോടുകൂടി പെട്രാളി(petrol)നുള്ള (പെട്രാളിയത്തിൽനിന്നും ലഭിക്കുന്ന, താരതമ്യേന സാന്ദ്രത കുറഞ്ഞ അംശം) ആവശ്യം ക്രമാതീതമായി ഉയർന്നു. പെട്രാളിയത്തിന്റെ സാന്ദ്രതയേറിയ ഘടകങ്ങള് താപനിർമിതിക്കുവേണ്ടി വ്യവസായശാലകളിൽ ഉപയോഗിക്കാന് തുടങ്ങി. യന്ത്രാപകരണങ്ങളുടെ സുഗമമായ പ്രവർത്തനത്തിന് ആവശ്യമായ സ്നേഹകഎച്ച(lubricating oil)യും പെട്രാളിയത്തിൽനിന്നു ലഭിക്കുന്നു.
വ്യത്യസ്തജ്വലനസ്വഭാവമുള്ള ഹൈഡ്രാകാർബണുകളുടെ ഒരു സങ്കീർണമിശ്രിതമാണ് പെട്രാളിയം; കൂടാതെ അതിൽ ചെറിയ അളവിൽ ഓക്സിജന്, സള്ഫർ, നൈട്രജന് എന്നിവയും അടങ്ങിയിരിക്കുന്നു. പെട്രാളിയത്തിൽ കാർബണ് 84-88 ശതമാനവും ഹൈഡ്രജന് 11.5-14.5 ശതമാനവും മറ്റുഘടകങ്ങള് 0.5-4.5 ശതമാനവും ആയിരിക്കും.
പെട്രാളിയം സാധാരണയായി വെള്ളവും പ്രകൃതിവാതകവും കലർന്ന രൂപത്തിലാണു കണ്ടുവരുന്നത്. അപ്രവേശ്യമായ പാറക്കെട്ടുകള്ക്കടിയിലാണ് ഇത് കാണപ്പെടുന്നത്. ഇതിനും പുറമേ അവസാദശിലകള് (sedimentary rocks), ചുണ്ണാമ്പുകല്ല് മുതലായവയ്ക്കിടയിലും എണ്ണനിക്ഷേപം കണ്ടുവരുന്നു. പെട്രാളിയത്തിനു മുകളിൽ പ്രകൃതിവാതകവും താഴെ വെള്ളവുമാണ്. ഭൂഗർഭത്തിൽനിന്ന് പെട്രാളിയം എടുക്കുന്നതിനുള്ള സംവിധാനം ലളിതമാണ്. ആദ്യം ആവശ്യമായ ആഴത്തിൽ കിണർ കുഴിക്കുന്നു. എണ്ണയുടെ ലഭ്യത പരമാവധി വർധിപ്പിക്കാന് ഉയർന്ന മർദത്തിലുള്ള ജലമോ വാതകമോ ഉപയോഗിക്കുന്നു.
പെട്രാളിയ സമ്പത്ത്
മധ്യപൂർവദേശങ്ങളിലെ രാജ്യങ്ങളിലാണ് മൊത്തം പെട്രാളിയം ഉത്പാദനത്തിന്റെ വലിയ പങ്കും നടക്കുന്നത്. സൗദിഅറേബ്യ, ഇറാന്, കുവൈത്ത്, ഇറാഖ് എന്നീ രാജ്യങ്ങളാണ് ഇതിൽ മുമ്പന്തിയിൽ നിൽക്കുന്നത്. യു.എസ്., റഷ്യ എന്നീ രാജ്യങ്ങളിലും ഇന്ന് വന്തോതിൽ പെട്രാളിയം ഖനനം നടക്കുന്നുണ്ട്. ഇന്ത്യ, ചൈന തുടങ്ങിയ രാജ്യങ്ങളിൽ പുതിയ എണ്ണ ഉറവിടങ്ങള് കണ്ടുപിടിക്കപ്പെടുന്നുണ്ട്.
ഉത്പാദനം
പ്രധാന പെട്രാളിയം ഉത്പന്നങ്ങള് ഗ്യാസോലിന് (gasoline) അഥവാ പെട്രാള്, മണ്ണെണ്ണ(kerosene), സ്വേദക എണ്ണകള് (distillate oils), അവശേഷക ഇന്ധനഎണ്ണകള് (residual fuel oils), സ്നേഹകഎണ്ണകള് (lubricating oils), ആസ്ഫാള്ട്ട് (asphalt)എന്നിവയാണ്.
ജലാംശം, ഉപ്പ്, ഗന്ധകം മുതലായവ നീക്കം ചെയ്തതിനുശേഷം പെട്രാളിയത്തെ അംശികസ്വേദനം (fractional distillation)ചെയ്ത് അതിന്റെ ഘടകങ്ങളാക്കി മാറ്റുന്നു. ഒരു ദ്രവപദാർഥത്തെ അതിന്റെ ഘടകങ്ങളുടെ വ്യത്യസ്ത തിളനിലയനുസരിച്ച് (boiling point) വേർതിരിക്കുന്ന പ്രക്രിയയെയാണ് അംശികസ്വേദനമെന്നു പറയുന്നത്. ഇങ്ങനെ ലഭിക്കുന്നവയിൽ ചില ഘടകങ്ങളെ നേരിട്ടും മറ്റുള്ളവയെ വിവിധ പ്രക്രിയകള്ക്കു ശേഷവും ഉപയോഗിക്കുന്നു.
താഴ്ന്ന തിളനിലയുള്ള വസ്തുവിന് പെട്ടെന്ന് കത്തുന്നതിനുള്ള കഴിവുണ്ട്. യാദൃച്ഛികമായ ജ്വലനത്തിനും സ്ഫോടനത്തിനും വിധേയമാകുന്നതുകൊണ്ടും ബാഷ്പീകരണംമൂലം നഷ്ടപ്പെടുന്നതുകൊണ്ടും ഇവയെ ശേഖരിച്ചു വയ്ക്കുന്നതിൽ ശ്രദ്ധ ചെലുത്തേണ്ടതുണ്ട്. താരതമ്യേന സാന്ദ്രതയേറിയതോ ഉന്നത തിളനിലയുള്ളതോ ആയ സ്വേദങ്ങളെ (distillate)ഉയർന്ന താപനിലയിലോ, രാസത്വരകം പ്രയോഗിച്ചോ, അതുമല്ലെങ്കിൽ മേല്പറഞ്ഞ രണ്ടിന്റെയും സാന്നിധ്യത്തിലോ, ഭഞ്ജനം ചെയ്ത് (cracking) ഗ്യാസൊലീന് ഉണ്ടാക്കാം. ഗുരുത്വമേറിയ ഹൈഡ്രാകാർബണ് തന്മാത്രകളെ ലഘുവും ബാഷ്പശീലമുള്ളതുമായ ഹൈഡ്രാകാർബണ് തന്മാത്രകളാക്കുന്നതിനെയാണ് ഭഞ്ജനം എന്നു പറയുന്നത്.
പെട്രാളിയത്തിന്റെ സ്വേദകപ്രക്രിയയിൽ കിട്ടുന്ന അവശിഷ്ടങ്ങളെ (residue) ഭഞ്ജകം ചെയ്ത് ഉപയോഗയോഗ്യമായ ഗ്യാസൊലീന്, കോക്ക് മുതലായവയോ അതല്ലെങ്കിൽ വ്യാവസായിക ഇന്ധനങ്ങളോ ആസ്ഫാള്ട്ടോ (പ്രധാനമായും റോഡ് ടാറിടുന്നതിന്) ഉണ്ടാക്കാം. എച്ചശുദ്ധീകരണശാലകളുടെ പ്രഥമമായ ലക്ഷ്യം പദാർഥങ്ങളെ ആവശ്യമനുസരിച്ച് വേണ്ട അളവിൽ ഉത്പാദിപ്പിക്കുകയാണ്. ഓരോ രാജ്യത്തിനും പെട്രാളിയം ഉത്പന്നങ്ങള്ക്ക് സ്വന്തമായ നിലവാര പ്രമാണങ്ങള് (standard specifi-cations) ഉണ്ട്. ഈ പ്രമാണങ്ങള് തീരുമാനിക്കുന്നതിന് അന്താരാഷ്ട്ര സഹകരണമുള്ളതുകൊണ്ട് വാഹനങ്ങള്ക്ക് ഏതു രാജ്യത്തുനിന്നും ഇന്ധനം നിറയ്ക്കാന് കഴിയും.
ഒരു ഇന്ധന എച്ചയുടെ മൊത്തം കലോറികമൂല്യം 18,500-20,000 ആഠഡ/റാത്തൽ ആയിരിക്കും. ഹൈഡ്രാ കാർബണിന്റെ വിവിധ തരത്തിലുള്ള സംയോജനമനുസരിച്ച് ഇന്ധനത്തിന്റെ കലോറികമൂല്യത്തിന് മാറ്റം സംഭവിക്കുന്നതാണ്. സാന്ദ്രതയും (density) ശ്യാനതയും(viscosity) ഏറിയ ഇന്ധനഎച്ചയ്ക്ക് സാന്ദ്രത കുറഞ്ഞവയെ അപേക്ഷിച്ച് കലോറികമൂല്യം കുറവായിരിക്കും; പക്ഷേ, വ്യാപ്തത്തിന്റെ അനുപാതത്തിൽ കലോറികമൂല്യം സാന്ദ്രതയേറിയ എച്ചയിൽ കൂടുതലായിരിക്കും.
വിമാനം മുതലായവയിൽ ഇന്ധനം സൂക്ഷിക്കാനുള്ള സ്ഥലപരിമിതിമൂലം ഉയർന്ന ആപേക്ഷികസാന്ദ്രതയുള്ള ഇന്ധന എച്ച ഉപയോഗിക്കുന്നതായിരിക്കും കൂടുതൽ അഭികാമ്യം. കലോറികമൂല്യം വസ്തുവിന്റെ സാന്ദ്രതയോട് കൂടുതൽ ബന്ധപ്പെട്ടിരിക്കുന്നു.
പ്രത്യേക പരിതഃസ്ഥിതിയിൽ പദാർഥം തീ കാട്ടിയാലുടനെ കത്തുന്ന താപാങ്കത്തെ അതിന്റെ പ്രജ്വലനതാപാങ്കം(flash point)എന്നു പറയുന്നു. ഗ്യാസൊലീന്റെ പ്രജ്വലനതാപാങ്കം അന്തരീക്ഷ താപനിലയെക്കാള് കുറവായിരിക്കും. സ്വേദക എച്ചയുടെയും ജ്വാലക(burner) എച്ചയുടെയും ചുരുങ്ങിയ പ്രജ്വലന താപാങ്കം 125oF (61.67oC) ആണ്. മണ്ണെണ്ണ, സാന്ദ്രതകുറഞ്ഞ ഡീസൽ മുതലായവയുടെ പ്രജ്വലന താപാങ്കം 125o-130oF ന് (51.6754.44oC) ഇടയ്ക്കായിരിക്കും.
മധ്യമസാന്ദ്രതയുള്ള ജ്വാലകഎച്ചയ്ക്കും തീവണ്ടിപോലുള്ള ഭാരിച്ച വാഹനങ്ങളിലും മറ്റും ഉപയോഗിക്കുന്ന ഡീസലിനും പ്രജ്വലന താപാങ്കം 145oF (62.78oC)നു അടുത്തുവരും. സാന്ദ്രതയേറിയ എച്ചകളുടെ പ്രജ്വലന താപാങ്കം 170oF (76.17oC)-ൽ കൂടുതലായിരിക്കും.
ഒരു ദ്രവ ഇന്ധനം സ്വയം കത്തുന്നതിന് ആവശ്യമായ താപനിലയാണ് ജ്വലനതാപാങ്കം (fire point) എന്നു പറയപ്പെടുന്നത്. ജ്വലന താപാങ്കം പ്രജ്വലന താപാങ്കത്തെക്കാള് സാധാരണയായി 20oF കൂടുതലായിരിക്കും. എണ്ണയുടെ ശ്യാനത (viscosity) ഒഴുക്കിനെതിരെയുള്ള അതിന്റെ പ്രതിരോധത്തെ അടിസ്ഥാനമാക്കി കണക്കാക്കുന്നു. നിർദിഷ്ടസമയത്ത് ഒരു പ്രാമാണിക ദ്വാരത്തിൽ(standard orifice) കൂടി കടന്നുപോകുന്ന എച്ചയുടെ പരിമാണത്താൽ അത് അളക്കപ്പെടുന്നു. ശ്യാനത താപനിലയെ ആശ്രയിച്ചിരിക്കും. ജ്വാലകത്തിലെ സുകരമായ കണീകരണത്തിന് (atomization) ഇന്ധനത്തെ ചൂടാക്കി ശ്യാനത കുറച്ച് ഉപയോഗിക്കണം.
മറ്റ് ദ്രവ ഇന്ധനങ്ങള്
ഇന്ധന എച്ചയ്ക്ക് പുറമേ, നേരിട്ട് ഇന്ധനമായി ഉപയോഗിക്കാവുന്ന മറ്റു ദ്രവ ഇന്ധനങ്ങളുമുണ്ട്. ഗ്യാസൊലീനും മണ്ണെണ്ണയും സ്റ്റൗ കത്തിക്കുന്നതിനും മറ്റു ചില പ്രത്യേകാവശ്യങ്ങള്ക്കും ഉപയോഗിക്കുന്നു. ആൽക്കഹോളും ബെന്സോളും (benzol)ഉപയോഗിക്കുന്നത് പ്രത്യേകം സംവിധാനം ചെയ്ത ഉപകരണങ്ങളിലാണ്. ഷെയ്ൽ എണ്ണ, കോള്ട്ടാർ, ടാർ എണ്ണ, നിമ്ന താപകാർബണീകരണത്തിൽനിന്നും ലഭിക്കുന്ന സ്വേദകങ്ങളോ അവശിഷ്ടങ്ങളോ ആയ എണ്ണഎന്നിവയെല്ലാം വ്യാവസായികമായി ഉപയോഗിക്കപ്പെടുന്നുണ്ട്.
ഗ്യാസൊലീന്
ഗ്യാസൊലീന്റെ രാസയോഗം ഏകദേശം താഴെപ്പറയുന്ന വിധമാണ്. കാർബണ് 83.5 മുതൽ 85 ശതമാനം വരെ; ഹൈഡ്രജന് 15 മുതൽ 15.8 ശതമാനം വരെ; നൈട്രജനും സള്ഫറും ഓക്സിജനും പൂജ്യം മുതൽ 1 ശതമാനം വരെ. താപമൂല്യം ഏകദേശം 20,000 BTU/റാത്തൽ ആണ്. ടെട്രാ എഥിൽ ലെഡ് കലർത്തിയ ഗ്യാസൊലീന് ചൂടാക്കുന്നതിനുള്ള ഉപകരണങ്ങളിൽ ഉപയോഗിക്കാന് പാടില്ല.
മണ്ണെണ്ണ
മണ്ണെണ്ണയുടെ ശരാശരി രാസയോഗം കാർബണ് 85 ശതമാനം, ഹൈഡ്രജന് 16 ശതമാനം എന്ന തോതിലാണ്. സള്ഫറിന്റെ ശതമാനം 0.125-ൽ കൂടരുത്; മണ്ണെണ്ണയുടെ താപമൂല്യം 20,000 മുതൽ 21,000 വരെ BTU/റാത്തൽ. ഇതിന്റെ പ്രാഥമിക തിളനില 128oC മുതൽ 180oC വരെയും, അന്തിമ തിളനില 235oC മുതൽ 336oC വരെയുമാണ്. മച്ചെച്ചയുടെ ആപേക്ഷിക സാന്ദ്രത 0.775 മുതൽ 0.850 വരെ വ്യതിചലിച്ചുകാണുന്നു; പ്രജ്വലന താപാങ്കം 24oC മുതൽ 66oC വരെയായിരിക്കും.
ആൽക്കഹോള്
എഥിൽ ആൽക്കഹോള്, പവർ ആൽക്കഹോള് (power alcohol) എന്നീ പേരിലും അറിയപ്പെടുന്നു. ഇത് പെട്രാള് എന്ജിനുകളിൽ പ്രതിസ്ഥാപിത (substitute) ഇന്ധനമായും ഉപയോഗിക്കം. പ്രത്യേകം സംവിധാനം ചെയ്ത കാർബുറേറ്ററുകളുപയോഗിച്ചോ അല്ലെങ്കിൽ ഗ്യാസൊലീനുമായി കലർത്തി സാധാരണ കാർബുറേറ്ററുപയോഗിച്ചോ ആന്തരദഹനയന്ത്രങ്ങളിൽ ഉപയോഗിക്കാം. എഥിൽ ആൽക്കഹോളിന്റെ താപമൂല്യം ഏകദേശം 12,780 BTU/റാത്തൽ ആണ്.
ഫാക്ടറിയിൽനിന്നു ലഭിക്കുന്ന ഉപോത്പന്നമായ ശർക്കരപ്പാവ് (molasses) പുളിപ്പിച്ച് സ്വേദനം ചെയ്യുമ്പോഴാണ് എഥിൽ ആൽക്കഹോള് ലഭിക്കുന്നത്; ഇപ്പോള് ചോളം, ഗോതമ്പ് തുടങ്ങിയ ധാന്യങ്ങള് പുളിപ്പിച്ചും വലിയ അളവിൽ ആൽക്കഹോള് ഉത്പാദിപ്പിച്ച് ഇന്ധനമായി ഉപയോഗിക്കുന്നുണ്ട്. സംശ്ലേഷണം (synthesis) വെഴിയായും ആൽക്കഹോള് ലഭിക്കുന്നു. മെഥിൽ ആൽക്കഹോളും (methyl alcohol) മേല്പറഞ്ഞ വിധം ഉപയോഗിക്കാം. അതിന്റെ കലോറികമൂല്യം ഏകദേശം 9,550 BTU/റാത്തൽ ആണ്.
ബെന്സോള്
കൽക്കരി കാർബണീകരിക്കുമ്പോള് ലഭിക്കുന്ന ബാഷ്പശീലമുള്ള പദാർഥങ്ങളിൽനിന്നു വേർതിരിച്ചെടുക്കുന്നതാണ് ബെന്സോള്. ഇത് 70oC-നും 150oC-നും മധ്യേ തിളയ്ക്കുന്നു. അതിൽ ഏകദേശം 70 ശതമാനം ബെന്സീന്, 18 ശതമാനം ടൊളുവീന് (Toluene), 6 ശതമാനം സൈലിന് (sylene) എന്നിവ അടങ്ങിയിരിക്കുന്നു. കലോറികമൂല്യം ഏകദേശം 18,000 BTU/റാത്തൽ ആണ്. പെട്രാളുമായി കൂട്ടിച്ചേർത്ത് ആന്തരദഹനയന്ത്രങ്ങളിൽ ഉപയോഗിക്കാം.
കോള്ട്ടാർ
കൽക്കരി കാർബണീകരിക്കുമ്പോള് ലഭിക്കുന്ന മറ്റൊരു ഉപോത്പന്നമാണ് കോള്ട്ടാർ. ഇത് ആരോമാറ്റിക സംയുക്ത(aromatic compounds)ങ്ങളുള്ള, ശ്യാനതയേറിയ മിശ്രിതമാണ്. താപമൂല്യം 15,000 മുതൽ 16,500 വരെ BTU/റാത്തൽ ആയിരിക്കും. ഇന്ധന എച്ച ഉപയോഗിക്കുന്ന ജ്വാലകങ്ങളിൽ ഉപയോഗിക്കാനായി അരിച്ച് നല്ലവച്ചം ചൂടാക്കി ശ്യാനത കുറയ്ക്കുന്നു.
ടാർ എണ്ണ
കോള്ട്ടാർ സ്വേദനം ചെയ്താണ് ടാർ എണ്ണ കിട്ടുന്നത്. "ക്രിയോസോട്ട് എണ്ണ' (creosote oil), "ആന്ത്രാസീന് എണ്ണ' (anthracene oil) മുതലായവയാണ് ഇതിലെ പ്രധാന അംശങ്ങള്. ഇതിന്റെ താപമൂല്യം കോള്ട്ടാറിന്റെ അത്ര തന്നെ വരും.
പ്രതിസ്ഥാപിത ദ്രവ ഇന്ധനങ്ങള്
ഖര, വാതക ഇന്ധനങ്ങളെ ദ്രവ ഇന്ധനമായി രൂപാന്തരപ്പെടുത്തുന്ന വളരെയധികം പ്രക്രിയകളുണ്ട്. ഇപ്രകാരമുള്ള പല വ്യവസായശാലകളും സ്ഥാപിക്കപ്പെട്ടിട്ടുണ്ട്. പെട്രാളിയം സുലഭമായി ലഭിക്കുന്ന സ്ഥലത്ത് ഇവ ലാഭകരമായിരിക്കുകയില്ല. ഈ പ്രക്രിയകള് മുഖാന്തരം ദ്രവ ഇന്ധനങ്ങളോടൊപ്പം, രാസവസ്തുക്കള്കൂടി ലഭിക്കുന്നു.
കാർബണീകരണം
കൽക്കരിയെ കാർബണീകരിക്കുമ്പോള് ലഭിക്കുന്ന ദ്രവ ഇന്ധനങ്ങളാണ് കോള്ട്ടാറും ടാർ എച്ചയും. നിമ്നതാപ കാർബണീകരണത്തിൽ ദ്രാവകോത്പന്നങ്ങള് കൂടുതലും ഉന്നതതാപ കാർബണീകരണത്തിൽ കുറവുമായിരിക്കും.
വാതക സംശ്ലേഷണം
ഹൈഡ്രജന്റെയും കാർബണ്മോണോക്സൈഡിന്റെയും മിശ്രിതം ഉത്പ്രരക (catalyst)ത്തിന്റെ സാന്നിധ്യത്തിൽ പ്രവർത്തിപ്പിച്ചാൽ ദ്രവ ഇന്ധനങ്ങളും, ദാഹ്യവാതകങ്ങളും ഉണ്ടാകുന്നു. ഹൈഡ്രജന്കാർബണ് മോണോക്സൈഡ് മിശ്രിതത്തെ "സംശ്ലേഷകവാതക' (synthesis gas)മെന്നു പറയുന്നു. കൽക്കരിയെ വാതകീകരിച്ചാണ് സംശ്ലേഷക വാതകം ഉണ്ടാക്കുന്നത്. താഴെ പറയുന്ന പ്രതിക്രിയ ഇതിന് ഉപയോഗിക്കാം:
C + H2O = H2 + CO (കാർബണ്) (നീരാവി) (സംശ്ലേഷണ വാതകം)
ജലവാതകജനിത്ര(Water gas Generator)മാണ് ഇതിനുപയോഗിക്കുന്നത്. പ്രകൃതിവാതകവും ദ്രവീകൃത പെട്രാളിയം വാതകവും മറ്റും ഉപയോഗിച്ച് സംശ്ലേഷകവാതകം ഉണ്ടാക്കാം. ഒട്ടനവധി പദ്ധതികളുണ്ടെങ്കിലും, "ഫിഷർ-ട്രാ(Fisher-tropsch) സംശ്ലേഷണ'മാണ് ശ്രദ്ധേയമായത്. ഈ പദ്ധതിയിൽ സംശ്ലേഷകവാതകത്തെ 200oC-300oC താപനിലയിൽ ഉത്പ്രരകമായ ഇരുമ്പുമായോ കൊബാള്ട്ടുമായോ സമ്പർക്കപ്പെടുത്തുന്നു. ഉത്പ്രരകത്തിന്റെ സ്ഥിരമായ വിതാനമോ (fixed bed), നേർത്ത കുഴമ്പോ (slurry), നിലംബിതവിതാനമോ (fluidized bed) ഉപയോഗിക്കാം. താപനില, മർദം, ഉത്പ്രരകങ്ങള് എന്നിവയിലുള്ള വ്യത്യാസമനുസരിച്ച് വിവിധ തരത്തിലുള്ള ഉത്പന്നങ്ങള് ലഭിക്കുന്നു. സാധാരണ മർദത്തിലും, 250oC-350oC താപനിലയിലും നിക്കലോ, കൊബാള്ട്ടോ ഉത്പ്രരകമായി ഉപയോഗിച്ചാൽ മീഥേന് ആയിരിക്കും പ്രധാന ഉത്പന്നം. ഇരുമ്പോ കൊബാള്ട്ടോ നിക്കലോ കീസിൽഗർ (kieselguhr) എന്ന പദാർഥത്തിൽ നിക്ഷേപിച്ച് ഉത്പ്രരകമായി ഉപയോഗിക്കുകയും താപനില 150oC നും 250oC നും മധ്യേ നിലനിർത്തുകയും ചെയ്താൽ സാന്ദ്രതയേറിയ ഹൈഡ്രാകാർബണുകള് ലഭിക്കുന്നു.
"ഐസോ' (Iso)സംശ്ലേഷണത്തിൽ സംശ്ലേഷകവാതകം 400ºC-450oC ലും 300-600 അന്തരീക്ഷമർദത്തിലും ലോഹഓക്സൈഡിന്റെ മീതെ കടത്തിവിടുന്നു. ഇവിടെ ഐസോ ബൂട്ടേനും ഐസോബ്യൂട്ടീനും ആണ് ഉത്പന്നങ്ങള്. ഇവ പ്രധാനമായി വ്യോമയാന ഇന്ധനമായി ഉപയോഗിക്കാം.
കൽക്കരി ഹൈഡ്രജനീകരണം
കൽക്കരി ഹൈഡ്രജനീകരിക്കുമ്പോള് ഹൈഡ്രജന്-കാർബണ് അനുപാതം പെട്രാളിയത്തിലേതുപോലെ ആയിത്തീരുന്നു. കൽക്കരിയും കോള്ട്ടാറും ഹൈഡ്രജനീകരിച്ച് ഗ്യാസൊലീന് ഉണ്ടാക്കാം. ഉന്നതതാപനിലയിലും മർദത്തിലും കൽക്കരിയിൽ ഹൈഡ്രജന് കൂട്ടുന്നതിനെക്കുറിച്ച് പഠനങ്ങള് നടത്തിയത് ബെർഗീയുസ് ആണ്.
കൽക്കരി നന്നായി ഉണക്കിപ്പൊടിച്ച് എച്ചയുമായി ചേർത്ത് കുഴമ്പുരൂപത്തിലാക്കി ഉത്പ്രരകം ചേർക്കുന്നു. ഇതിനുശേഷം 300ീഇ450ീഇലോ, 200-700 അന്തരീക്ഷമർദത്തിലോ, ഹൈഡ്രജനീകരിക്കുന്നു. ഈ പ്രക്രിയയിൽ ഉണ്ടാകുന്ന ഹൈഡ്രാകാർബണ് വാതകം രൂപാന്തരപ്പെടുത്തി ഹൈഡ്രജനീകരണത്തിനുള്ള ഹൈഡ്രജന് ഉണ്ടാക്കാം.
ഈ പ്രക്രിയയിൽ ഗ്യാസൊലീന്റെ ക്വഥനപരിധിയുള്ള എണ്ണമിശ്രിതം ലഭിക്കുന്നു. ഇതു സ്വേദനം ചെയ്ത് ഗ്യാസൊലീന് ഉണ്ടാക്കാം. ഉന്നത തിളനിലയുള്ള പദാർഥങ്ങളാകട്ടെ, ഭഞ്ജനം ചെയ്ത് താഴ്ന്ന തിളനിലയുള്ള ഗ്യാസൊലീന് ഉണ്ടാക്കാം. ഒരു ടണ് കൽക്കരിയിൽനിന്ന് 40 ഗ്യാലന് മോട്ടോർ ഇന്ധനവും 50 ഗ്യാലന് ഡീസൽഎണ്ണയും 35 ഗ്യാലന് ഇന്ധന എണ്ണയും 10,000 ക്യുബിക്ക് അടി ഇന്ധനവാതകവും ലഭിക്കുന്നു.
ദ്രവ ഇന്ധനങ്ങളുടെ ഉപയോഗം
പെട്രാളിയത്തിൽനിന്നു ലഭിക്കുന്ന ദ്രവ ഇന്ധനങ്ങള് ചൂളകളിലെ ദഹനത്തിനോ ആന്തരദഹനയന്ത്രങ്ങളുടെ സിലിണ്ടറുകളിൽ ഊർജം ഉത്പാദിപ്പിക്കുന്നതിനോ ഉപയോഗിക്കാം. സാന്ദ്രത കൂടിയതും കുറഞ്ഞതുമായ എച്ചകള് ആന്തരദഹനയന്ത്രങ്ങളിൽ ഉപയോഗിക്കുന്നു.
സാന്ദ്രത കുറഞ്ഞ എണ്ണ അഗ്നിജ്വാലയുടെയോ സ്ഫുലിംഗത്തിന്റെയോ സഹായത്താൽ ജ്വലിപ്പിക്കാം; സാന്ദ്രത കൂടിയ എണ്ണയാകട്ടെ, ബാഷ്പീകരിക്കുന്നതും ജ്വലിപ്പിക്കുന്നതും സമ്മർദാഘാതം (compression stroke) ഉണ്ടാക്കുന്ന ഉന്നത താപനിലകൊണ്ടാണ്.
ചൂളകളിൽ ഉപയോഗിക്കുകയാണെങ്കിൽ ധൂമരഹിതദഹനത്തിനായി ആവശ്യത്തിലധികം വായു പ്രവേശിപ്പിക്കേണ്ടിയിരിക്കുന്നു. ഓരോ റാത്തൽ ഇന്ധന എണ്ണയ്ക്കും ഏകദേശം 18-20 റാത്തൽ വായു ആവശ്യമുണ്ട്; ഉന്നതക്ഷമതയോടുകൂടിയ ദഹനത്തിന് ഏകദേശം 15 ശതമാനം മുതൽ 25 ശതമാനം വരെ വായു അധികം ഉപയോഗിക്കണം.
എണ്ണജ്വാലകം
ദ്രവ ഇന്ധനം ഉപയോഗിക്കുന്ന ജ്വാലകങ്ങള് രണ്ടുതരമുണ്ട്: ദ്രാവകത്തെ ജ്വാലകത്തിൽവച്ചുതന്നെ ബാഷ്പീകരിക്കുന്നത്; ദ്രാവകത്തെ കണീകരിക്കുന്നത്.
ബാഷ്പീകരണ ജ്വാലകങ്ങളിൽ ബാഷ്പശീലമുള്ള ദ്രാവകങ്ങളെ ഉപയോഗിക്കാം. കണീകരണജ്വാലക(atomizing burner)ങ്ങളിൽ യാന്ത്രികശക്തി ഉപയോഗിച്ച് ദ്രവ ഇന്ധനത്തെ ചെറിയ കണികകളാക്കുന്നു. ഇതിനുപയോഗിക്കുന്ന മാർഗം അനുസരിച്ച് കണീകരണജ്വാലകങ്ങളെ റോട്ടറി (rotary), സഹായകദ്രാവകം (auxiliary fluid), യാന്ത്രികകണീകാരകം (mechanical atomizer) എന്നിങ്ങനെ തരംതിരിച്ചിരിക്കുന്നു. കണീകരണം ഇന്ധനത്തെ ചെറിയ കണങ്ങളാക്കി മാറ്റുകയും ദഹനവായുവുമായി ചേർത്ത് നല്ല ജ്വലനവും സ്വച്ഛമായ ജ്വാലയും ഉളവാക്കുകയും ചെയ്യുന്നു. ഇത് വ്യാവസായികാവശ്യങ്ങള്ക്ക് ധാരാളമായി ഉപയോഗപ്പെടുത്തുന്നു. ചില ജ്വാലകങ്ങളിൽ നീരാവി ഉപയോഗിക്കുന്നു; ഇത് കണീകരണപ്രക്രിയയെ സഹായിക്കുന്നതോടൊപ്പം ജ്വാലകപ്രവർത്തനത്തിന്റെ അനുനേയത(flexibility) യ്ക്കും ജ്വാലകത്തിന്റെ ലളിതമായ രൂപകല്പനയ്ക്കും ഉപകരിക്കുന്നു.
ലഘു ആന്തരദഹനയന്ത്രങ്ങള്
മോട്ടോർഇന്ധനം അഥവാ ഗ്യാസൊലീന് പെട്രാളിയ ഉത്പന്നങ്ങളിൽ വളരെ പ്രധാനപ്പെട്ടതാണ്. അതിൽ നേരെ ലഭിക്കുന്ന (straight run) ഗ്യാസൊലീനും ഭഞ്ജനം (cracking)ചെയ്തു ലഭിക്കുന്ന ഗ്യാസൊലീനും അടങ്ങിയിരിക്കുന്നു; ഏകദേശം 20 ശതമാനത്തോളം പ്രാകൃതികഗ്യാസൊലീനും അടങ്ങിയെന്നു വരാം.
മോട്ടോർ ഗ്യാസൊലീന് 37.78oCമുതൽ 204.44oC വരെ തിളയ്ക്കുന്നു; വ്യോമയാന ഗ്യാസൊലീനാകട്ടെ 37.78oCമുതൽ 162.78oCവരെ തിളയ്ക്കുന്നു. ഉന്നത ഒക്ടേന്സംഖ്യ (octane number)കളുള്ള ഘടകങ്ങള് കർക്കശ നിബന്ധനകള് പാലിച്ച് മിശ്രണം ചെയ്താണ് വ്യോമയാന ഗ്യാസൊലീന് ഉണ്ടാക്കുന്നത്. ഒരു ഇന്ധനത്തിന്റെ അപസ്ഫോടനസവിശേഷതയെ (knocking characteristic)ആണ് ഒക്ടേന് സംഖ്യ സൂചിപ്പിക്കുന്നത്. n ഹെപ്ടേന് (n-heptane) വളരെ തീവ്രമായി അപസ്ഫോടനം ചെയ്യുന്നതുകൊണ്ട് അതിന്റെ അപസ്ഫോടകരോധിമൂല്യം (antiknock value) പൂജ്യമായി തീരുമാനിക്കപ്പെട്ടിരിക്കുന്നു. ഐസോ-ഒക്ടേന് (iso-octane എന്ന രാസപദാർഥം വളരെ കുറച്ചുമാത്രം അപസ്ഫോടനവിധേയമാക്കുന്നതുകൊണ്ട് അതിന്റെ അപസ്ഫോടകരോധിമൂല്യം 100 ആയി കണക്കാക്കപ്പെടുന്നു.
ഇന്ധനത്തിന്റെ അപസ്ഫോടനസവിശേഷതകള്ക്കു സമാനമായ സവിശേഷതകളുള്ള ഐസോ-ഒക്ടേയിനിന്റെയും n ഹെപ്ടേനിന്റെയും മിശ്രിതത്തിലെ ഐസോ-ഒക്ടേയിനിന്റെ വ്യാപ്തശതമാനത്തെയാണ് "ഒക്ടേന്സംഖ്യ' എന്നു പറയുന്നത്. ഉദാഹരണമായി ഒരു പെട്രാളിന്റെ സാമ്പിള് 80 ഭാഗം ഐസോ-ഒക്ടേനും 20 ഭാഗം n ഹെപ്ടേനും ഉള്ള ഒരു മിശ്രിതത്തിനു സമാനമായ അപസ്ഫോടനം ഉണ്ടാക്കുകയാണെങ്കിൽ ആ പെട്രാളിന്റെ ഒക്ടേന്സംഖ്യ 80 ആയിരിക്കും.
വിമാനങ്ങളിൽ ഉപയോഗിച്ചുവരുന്ന ചില ഇന്ധനങ്ങളുടെ ഒക്ടേന്സംഖ്യ 100-ൽ അധികമായിരിക്കും. ഇതു കണക്കാക്കുന്നത് താഴെപ്പറയുന്ന സമവാക്യം ഉപയോഗിച്ചാണ്.
ഒക്ടേന്സംഖ്യ = (ശക്തിസംഖ്യ-100)/3 + 100
സ്വേച്ഛാപരമായ ശക്തിസംഖ്യ (arbitrary power number) ആകട്ടെ, യന്ത്രത്തിൽനിന്നു ലഭിക്കുന്ന ശക്തിക്ക് ആനുപാതികമാണ്. യു.എസ്സിൽ മോട്ടോർ ഇന്ധനങ്ങള്ക്ക് 90-110 വരെ ഒക്ടേന് സംഖ്യയാണ് നിർദേശിക്കപ്പെട്ടിട്ടുള്ളത്; ഇന്ത്യയിൽ, 75-85 വരെയുമാണ്. വ്യോമയാന ഇന്ധനങ്ങള്ക്ക് 150 ഒക്ടേന് സംഖ്യവരെയും കാണപ്പെടുന്നു.
സ്ഫുലിംഗജ്വലന(spark ignition)യന്ത്രങ്ങളിൽ, ഇന്ധനം വായുവിലേക്ക് സ്പ്ര ചെയ്ത് ദഹന അറകളിലേക്ക് വിടുന്നു. ദഹനത്തിനുമുമ്പ് ഇന്ധനം പരിപൂർണമായി ബാഷ്പീകരിക്കപ്പെടേണ്ടത് ആവശ്യമാണ്. ഒരു ആന്തരദഹനയന്ത്രത്തിന്റെ ക്ഷമത സമ്മർദാനുപാതം (compression ratio), യന്ത്രഡിസൈന്, ഇന്ധനങ്ങളുടെ സവിശേഷസ്വഭാവങ്ങള് മുതലായവയെ ആശ്രയിച്ചിരിക്കുന്നു. യന്ത്രത്തിലെ "അപസ്ഫോടനം' (knocking, pinking or detonation) മേല്പറഞ്ഞ മൂന്നുഘടകങ്ങളുടെ അസന്തുലിതാവസ്ഥയെ സൂചിപ്പിക്കുന്നു.
അപസ്ഫോടനം ഉന്നതവേഗതയിലുള്ള മർദതരംഗങ്ങളുടെ പ്രവർത്തനഫലമാണ്. ദഹനയറകളിലെ ഈ തരംഗങ്ങള് സെക്കന്ഡിൽ 3,000 മുതൽ 6,000 വരെ ആവൃത്തി ഉള്ളവയാണ്. ഇത് ഉഗ്രശബ്ദത്തോടുകൂടിയ വിസ്ഫോടനംപോലെയാണ്; സമ്മർദമർദ(compression pressure)ത്തിന്റെ വർധനവനുസരിച്ച് തീക്ഷ്ണതയോടെ സംഭവിക്കുന്നു. സാധാരണയായി അപസ്ഫോടനം സംഭവിക്കുന്നത് താഴ്ന്ന ഒക്ടേന് സംഖ്യയുള്ളപ്പോഴാണ്. ടെട്രാ എഥിൽ ലെഡ് ഉപയോഗിച്ചും (1 മുതൽ 2 മില്ലി ലിറ്റർ ഓരോ ഗ്യാലനും), ചെറിയ അളവിൽ പരിഷ്കരിച്ച ശുദ്ധീകരണ പ്രക്രിയമൂലവും ഒക്ടേന്സംഖ്യ വർധിപ്പിക്കാം.
ഭാരിച്ച എന്ജിനുകള്ക്കുള്ള ദ്രവ ഇന്ധനങ്ങള്
സാധാരണ ഡീസൽഎന്ജിനുകളിലെ പിസ്റ്റണ് വായുവിനെ മാത്രമേ മർദിക്കുന്നുള്ളൂ. പിസ്റ്റണ് മുകളിലായിരിക്കുമ്പോള് സിലിണ്ടറിലുള്ള ഉന്നതമർദത്തിലേക്ക് ഇന്ധനം യാന്ത്രികമായി സ്പ്ര ചെയ്യുന്നു. ഇതുമൂലം ഇന്ധനം വായുവുമായി കൂടിച്ചേരാന് ഇടയാകുകയും സമ്മർദന സ്റ്റ്രാക്കി(compression stroke)ൽ ഉത്പാദിപ്പിക്കപ്പെടുന്ന താപത്താൽ ജ്വലിക്കുകയും ചെയ്യുന്നു. ഡീസൽഎന്ജിന് ഉത്തമക്ഷമതയുള്ള ദ്രവ ഇന്ധന എന്ജിനാകുന്നു. ബസ്സുകളിലും ട്രക്കുകളിലും പൂർവചാലകങ്ങളിലും (prime movers) വെർധിച്ച തോതിൽ ഇത് ഉപയോഗിക്കപ്പെടുന്നു. തീവണ്ടികളിൽ ഡീസൽഎന്ജിന് ഉപയോഗിക്കാന് തുടങ്ങിയതോടെ അവയുടെ പ്രവർത്തനച്ചെലവ് ഗണ്യമായി കുറഞ്ഞു. കടലിലെ പ്രതിഷ്ഠാപന(marine installation)ങ്ങള്ക്കും നിശ്ചലഘനയന്ത്രങ്ങള്ക്കും ഡീസൽഎന്ജിന് ഉത്തമമാണ്.
ഇന്ധനത്തിന്റെ ഘടന, തിളയ്ക്കലിന്റെ പരിധി, സീറ്റേന് സംഖ്യ (cetane number) എന്നിവ ഡീസൽഎച്ചയുടെ പ്രധാന സവിശേഷതകളാണ്. ഇന്ധന അന്തഃക്ഷേപണത്തിനു(fuel injection)ശേഷം ഇന്ധനം ജ്വലിക്കുന്നതിനുവേണ്ട സമയത്തിന്റെ ഒരളവാണ് സീറ്റേന്സംഖ്യ. സീറ്റേന് എന്ന രാസവസ്തുവിന്റെ ജ്വലനപശ്ചത (ignition lag) വളരെ കുറവായതിനാൽ അതിന്റെ സീറ്റേന്സംഖ്യ 100 ആയും, -മെഥിൽ നാഫ്തലി(-methyl naphthalene)ന്റെ ജ്വലനപശ്ചത വളരെക്കൂടുതൽ ആയതിനാൽ അതിന്റെ സീറ്റേന്സംഖ്യ പൂജ്യമായും എടുത്തിരിക്കുന്നു.
ഒരു ഇന്ധനത്തിന്റെ ദഹനഗുണങ്ങളോടു സദൃശമായ ഗുണങ്ങളുള്ള സീറ്റേനിന്റെയും, -മെഥിൽ നാഫ്തലിന്റെയും മിശ്രിതത്തിലെ സീറ്റേനിന്റെ വ്യാപ്തശതമാനത്തെയാണ് സീറ്റേന്സംഖ്യ എന്നു പറയുന്നത്. അധികം എന്ജിനുകളും 40 മുതൽ 50 വരെ സീറ്റേന്സംഖ്യയുള്ള ഇന്ധനങ്ങളെക്കൊണ്ട് നന്നായി പ്രവർത്തിക്കുന്നു. എഥിൽ നൈട്രറ്റ്, അസറ്റോണ് പെറോക്സൈഡ്, ഐസോ അമൈൽനൈട്രറ്റ് എന്നിവ ചേർത്ത് ഡീസലെച്ചയുടെ സീറ്റേന്സംഖ്യ വർധിപ്പിക്കാം. ലഘുസ്വേദകഎച്ചകള് (light distillate oils) 176.67o-237.78oC വരെയും, മധ്യമ ഡീസൽഎച്ചകള് 187.78o-343.33o വരെയും ഘനഎച്ചകള് 204.44o-371.11oC വരെയും തിളയ്ക്കുന്നു.
ദ്രവ ഇന്ധനങ്ങളുടെ മേന്മ
ദ്രവ ഇന്ധനങ്ങള് കൈമാറ്റം ചെയ്യാനും സൂക്ഷിച്ചുവയ്ക്കാനും കൈകാര്യം ചെയ്യാനും താരതമ്യേന എളുപ്പമാണ്. പൈപ്പ് ഉപയോഗിച്ച് ദ്രവ ഇന്ധനങ്ങളെ വിദൂരസ്ഥലങ്ങളിലേക്കുപോലും കൊണ്ടുപോകാം. കുറച്ച് ഇടം മാത്രം ഉപയോഗിച്ച് ചൂളകളിൽ ഉയർന്ന താപം ഉണ്ടാക്കാനും എളുപ്പം ജ്വലിക്കാനും ഈ ഇന്ധനത്തിന് കഴിയുന്നു. ദഹിക്കുമ്പോള് ഖര ഇന്ധനങ്ങളെപ്പോലെ ചാരം ഉണ്ടാകുന്നുമില്ല.
ദ്രവ ഇന്ധനത്തിന് ഖര ഇന്ധനത്തെക്കാള് ഏകദേശം 1.5 മുതൽ 2 വരെ മടങ്ങ് താപമൂല്യം കാണും. ദ്രവ ഇന്ധനങ്ങള് സൂക്ഷിക്കാന് വാതക ഇന്ധനങ്ങളെക്കാള് സ്ഥലം കുറച്ചുമതി. ശുദ്ധിയും സ്വതഃദഹനത്തിന്റെ (spontaneous combustion) അഭാവവും നിറച്ചു സൂക്ഷിക്കാനുള്ള എളുപ്പവുമാണ് ദ്രവ ഇന്ധനത്തിന്റെ മറ്റു ഗുണങ്ങള്.
വാതക ഇന്ധനങ്ങള്
വിവിധാനുപാതങ്ങളിൽ ലഘുവാതകങ്ങളും ചിലപ്പോള് നിഷ്ക്രിയവാതകങ്ങളും ഓക്സിജനും അടങ്ങിയിരിക്കുന്ന ഒരു മിശ്രിതമാണ് വാതക ഇന്ധനം. ഹൈഡ്രജന്, കാർബണ് മോണോക്സൈഡ്, മീഥേന്, ഈഥേന്, എഥിലിന്, പ്രാപ്പേന്, പ്രാപിലിന്, ബ്യൂട്ടേന്, ബ്യൂട്ടിലിന്, ബെന്സീന്, അസെറ്റിലിന് എന്നിവയാണ് ദാഹ്യവാതകങ്ങള്; നിഷ്ക്രിയവാതകങ്ങള് സാധാരണയായി കാർബണ്ഡൈഓക്സൈഡും നൈട്രജനുമാകുന്നു.
വിവിധതരങ്ങള്
വാതക ഇന്ധനങ്ങള് പ്രധാനമായും താപം ഉത്പാദിപ്പിക്കാനായി ഉപയോഗിക്കുന്നതുകൊണ്ട് കലോറികമൂല്യത്തിന്റെ അടിസ്ഥാനത്തിലാണ് അവയെ വകയിരുത്തുന്നത്. പ്രധാനപ്പെട്ട വ്യാവസായിക വാതകങ്ങള് താഴെപ്പറയുന്നവയാണ്:
ബ്ലാസ്റ്റ് ഫർണസ് വാതകം
ഇരുമ്പയിര്, കോക്കിന്റെയും ചൂടാക്കിയ വായുവിന്റെയും സാന്നിധ്യത്തിൽ ഉരുക്കുമ്പോള് ലഭിക്കുന്ന ഒരു ഉപോത്പന്നമാണ് ബ്ലാസ്റ്റ് ഫർണസ് വാതകം. 1000 ടണ് ഇരുമ്പും 1800 റാത്തൽ കോക്കും ഉപയോഗിക്കുന്ന ഒരു ആധുനിക ബ്ലാസ്റ്റ് ഫർണസിൽ 12,70,00,000 ഘന അടി (35,96,640 ഘ.മീ.) വാതകം ഒരു ദിവസം ഉണ്ടാക്കാന് കഴിയും; അതിന്റെ കലോറികമൂല്യം ഏകദേശം 100 BTU/ഘന അടി ആണ്. കലോറികമൂല്യം കുറവായതുകൊണ്ട് ഏറെ ആവശ്യങ്ങള്ക്കുപയോഗിക്കാനോ, വിദൂരസ്ഥലങ്ങളിലേക്ക് വിതരണം ചെയ്യാനോ സാധ്യമല്ല.
ബ്ലാസ്റ്റ് ഫർണസിൽനിന്നു ലഭിക്കുന്ന വാതകത്തിന്റെ മൂന്നിലൊരു ഭാഗം സ്റ്റൗ ചൂടാക്കുന്നതിനും, ശേഷിച്ചത് നീരാവി ഉത്പാദിപ്പിക്കുന്നതിനും കോക്കടുപ്പുകള് ചൂടാക്കുന്നതിനും മറ്റുമായി ഉപയോഗിക്കുന്നു. ബ്ലാസ്റ്റ് ഫർണസ് വാതകത്തിന്റെ ചേരുവ ശതമാനം: കാർബണ്ഡൈഓക്സൈഡ്-11.5; ഹൈഡ്രജന്-1.0; കാർബണ്മോണോക്സൈഡ്-27.5; നൈട്രജന്-60.0 എന്നിങ്ങനെയാണ്.
പ്രാഡ്യൂസർ വാതകം
മുഖ്യഘടകങ്ങളായി കാർബണ്മോണോക്സൈഡ്, നൈട്രജന് എന്നിവയും ചുരുങ്ങിയ തോതിൽ കാർബണ്ഡൈഓക്സൈഡും അടങ്ങിയിരിക്കുന്നു. തപിച്ച് ധവളോജ്ജ്വലമായ ഇന്ധനവിതാനത്തിലൂടെ വായുവും നീരാവിയും കടത്തിവിട്ടാണ് ഇത് നിർമിക്കുന്നത്. ഇന്ധനവിതാനത്തിൽ കോക്ക്, കൽക്കരി, ലിഗ്നൈറ്റ്, പീറ്റ് മുതലായവ ഉപയോഗിക്കാം. താപദീപ്തമായ കാർബണിലൂടെ വായുമാത്രം കടത്തിവിടുമ്പോള് ഉണ്ടാകുന്ന പ്രധാന അഭിക്രിയ ഇനി പറയുംപ്രകാരമാണ്.
വായുവിലെ ഓരോ വ്യാപ്തം ഓക്സിജന്റെയും കൂടെ 3.76 വ്യാപ്തം നൈട്രജന് ഉണ്ട്. മുഴുവന് കാർബണ്ഡൈഓക്സൈഡും കാർബണ്മോണോക്സൈഡായി മാറ്റിയാൽ ഉണ്ടാകുന്ന വാതകത്തിൽ 34.5 ശതമാനം കാർബണ് മോണോക്സൈഡും 65.5 ശതമാനം നൈട്രജനും ഏകദേശം 110 BTU/ഘന അടി കലോറികമൂല്യവും ഉണ്ടായിരിക്കും. പ്രയോഗത്തിൽ കാർബണ്ഡൈഓക്സൈഡ് പരിപൂർണമായി കാർബണ്മോണോക്സൈഡ് ആയി മാറുകയില്ല. ഈ വാതകത്തെ സീമന്വാതകം (siemen gas)എന്നു പറയുന്നു. ഇതിന് സാധാരണയായി താഴ്ന്ന കലോറികമൂല്യമേയുള്ളൂ. മേൽവിവരിച്ചപ്രകാരം പ്രാഡ്യൂസർ ഉപകരണം പ്രവർത്തിക്കുകയാണെങ്കിൽ കാർബണ് വായുവിൽ ജ്വലിച്ച ഭാഗത്തു താപം വർധിക്കുകയും ചാരം ഉരുകി ഉണ്ടാകുന്ന ക്ലിങ്കറുകള് (clinkers) നീക്കംചെയ്യാന് ബുദ്ധിമുട്ടു നേരിടുകയും ചെയ്യുന്നു. ഈ പ്രതിബന്ധം ഒഴിവാക്കാനായി വായുവിന്റെകൂടെ നീരാവിയും ഉപയോഗിക്കുന്നു. കാർബണും നീരാവിയും തമ്മിലുള്ള അഭിക്രിയ താഴെ പറയുംവിധമാണ്.
ഈ അഭിക്രിയകള് ഊഷ്മശോഷക(endothermic)ങ്ങളായതുകൊണ്ട് താപം ആഗിരണം ചെയ്യപ്പെടുകയും, ഇന്ധനവിതാനത്തിന്റെ താപനില ഉയർന്നുപോകാതെ ക്രമപ്പെടുകയും ചെയ്യുന്നു. പ്രാഡ്യൂസറിൽ നിറയ്ക്കുന്ന ഇന്ധനത്തിന്റെ തരമനുസരിച്ച് വാതകത്തിന്റെ സ്വഭാവം വ്യത്യാസപ്പെട്ടിരിക്കും. ഉന്നത ബാഷ്പശീലമുള്ള കൽക്കരി ഉപയോഗിച്ചാൽ ഏകദേശം 130 BTU/ഘനഅടിവരെയും താഴ്ന്ന ബാഷ്പശീലമുള്ള കോക്ക് ഉപയോഗിച്ചാൽ ഏകദേശം 110 BTU/ഘനഅടി വരെയും കലോറികമൂല്യം ലഭിക്കുന്നു. ബിറ്റ്യൂമീനിയകൽക്കരി ഉപയോഗിച്ചുള്ള പ്രാഡ്യൂസർ വാതകത്തിന്റെ ചേരുവശതമാനം കാർബണ്ഡൈഓക്സൈഡ്-4.5; ഓക്സിജന്-0.6; കാർബണ്മോണോക്സൈഡ്-27.0; ഹൈഡ്രജന്-14.0; മീഥേന്-3.0; നൈട്രജന്-50.9 എന്നിങ്ങനെയാണ്. ഈ വാതകത്തിന്റെ മൊത്തം കലോറികമൂല്യം 163 BTU/ഘനഅടി ആണ്. ഇത് കോക്കടുപ്പുകളിലും ഓപ്പണ് ഹാർത്(open hearth)ചൂളകളിലും ചുച്ചാമ്പുചൂളകളിലും ഇഷ്ടികച്ചൂളകളിലും കളിമണ്ചൂളകളിലും ഉപയോഗിക്കുന്നു.
ജലവാതകം
40 ശെതമാനത്തോളം കാർബണ്മോണോക്സൈഡും 50 ശതമാനത്തോളം ഹൈഡ്രജനും അടങ്ങിയ വാതക മിശ്രിതമാണ് ഇത്. താപദീപ്തമായ ഇന്ധനവിതാനത്തിലുടെ വായുവും നീരാവിയും ഒന്നിടവിട്ടു കടത്തിയാണ് ജലവാതകം ഉണ്ടാക്കുന്നത്. കാർബണും വായുവും തമ്മിലും കാർബണും നീരാവിയും തമ്മിലും ഉള്ള അഭിക്രിയകള് പ്രാഡ്യൂസർവാതകത്തിൽ വിവരിച്ചപോലെയാണ്; പക്ഷേ, ഒന്നിച്ചാവുന്നതിനുപകരം തവണകളായിട്ടാണ് ഇത് നടക്കുന്നതെന്നു മാത്രം.
വായു ഉപയോഗിക്കുമ്പോള് മോചിപ്പിക്കപ്പെടുന്നതും ഇന്ധനവിതാനത്തിൽ സംഭരിക്കപ്പെടുന്നതുമായ താപം, നീരാവി കടത്തിവിടുമ്പോഴത്തെ അഭിക്രിയയ്ക്കാവശ്യമായ ചൂടു നല്കുന്നു. വായു ഉപയോഗിക്കുമ്പോള് ഉണ്ടാകുന്ന വാതകത്തിൽ വലിയൊരംശം നൈട്രജന് ഉള്ളതുകൊണ്ട് അത് ഒരു ഇന്ധനമായി ഉപയോഗപ്പെടുന്നില്ലെങ്കിലും വായുവും നീരാവിയും മുന്കൂട്ടി ചൂടാകാന് ഉപകരിക്കുന്നു. നീരാവിവാതത്തിൽ (steam blow)ഉണ്ടാകുന്ന വാതകം ഇന്ധനമായി ഉപയോഗിക്കുന്നു.
ഉപയോഗിക്കുന്ന ഖര ഇന്ധനത്തിന്റെ സ്വഭാവമനുസരിച്ച് കലോറികമൂല്യം 285 മുതൽ 385 വരെ ആഠഡ/ഘനഅടി ഏറിയിരിക്കും. കാർബണ്മോണോക്സൈഡും ഹൈഡ്രജനും നീലജ്വാലയോടുകൂടി ജ്വലിക്കുന്നതുകൊണ്ടാണ് ഇതിന് ബ്ലൂഗ്യാസ് (blue gas)എന്ന പേര് വന്നത്.
കോക്ക് ഉപയോഗിച്ച് ഉണ്ടാക്കുന്ന ജലവാതകത്തിന്റെ മാതൃകാ ചേരുവശതമാനം ഇനി പറയുംപ്രകാരമാണ്; കാർബണ്ഡൈഓക്സൈഡ്-5.4; ഓക്സിജന്-0.7; കാർബണ്മോണോക്സൈഡ്-37.0; ഹൈഡ്രജന്-47.5; മീഥേന്-1.3; നൈട്രജന്-8.3. ഇത്തരം ജലവാതകത്തിന്റെ മൊത്തം കലോറികമൂല്യം 287 ആഠഡ/ ഘനഅടിയും സൈദ്ധാന്തിക ജ്വാലാതാപാങ്കം (theoretical flame temperature) 2021.1oCഉം ആണ്. ഇത് ഫോർജ്-വെൽഡിങ്ങിനും സംശ്ലേഷകവാതകമായി അമോണിയ, മെഥനോള് മുതലായവ ഉണ്ടാക്കാനും ഉപയോഗിക്കുന്നു.
കാർബുരിത ജലവാതകം
ജലവാതകവും വാതകഹൈഡ്രാ കാർബണുകളും ചേർന്ന മിശ്രിതത്തെയാണ് കാർബുരിത ജലവാതകം എന്നു പറയുന്നത്. ഹൈഡ്രാ കാർബണുകളിൽ മീഥേന്, വാതക ഒലിഫിനുകള്, ബെന്സീന് മുതലായവയും ചെറിയ തോതിൽ ഈഥേന്, ഉയർന്ന പാരഫിനുകള്, ആരോമാറ്റിക്കുകള് (aromatics)എന്നിവയും അടങ്ങിയിരിക്കുന്നു. കാർബുറേഷന് വാതകത്തിന്റെ താപമൂല്യം വർധിപ്പിക്കുന്നു. 1100 ആഠഡ/ഘനഅടിവരെ താപമൂല്യമുള്ള ജലവാതകം നിർമിക്കാം. നഗരങ്ങളിൽ വിതരണം ചെയ്യാനുള്ള വാതകത്തിന്റെ താപമൂല്യം 500 മുതൽ 600 വരെ ആഠഡ/ഘനഅടിയായി ക്രമീകരിച്ചിരിക്കുന്നു.
കാർബുരിത ജലവാതകയന്ത്രത്തിന്റെ പ്രധാനഭാഗങ്ങള് ജനറേറ്റർ, കാർബുറേറ്റർ, സൂപ്പർഹീറ്റർ സീൽ എന്നിവയാണ്. വായു പ്രവേശിപ്പിക്കുമ്പോഴുണ്ടാകുന്ന വാതകം കാർബുറേറ്ററിൽ കത്തിക്കുകയും പിന്നീട് സൂപ്പർഹീറ്ററിലൂടെ കടത്തിവിടുകയും ചെയ്യുന്നു. അത് കാർബുറേറ്ററിലെ ഭിത്തികളെയും ചെക്കർ-ഇഷ്ടിക(checker-bricks)കെളെയും ചൂടു പിടിപ്പിക്കുന്നു. ഈ വാതകം സൂപ്പർഹീറ്ററിലൂടെ അന്തരീക്ഷത്തിലേക്ക് വിടുന്നു.
നീരാവി കടത്തിവിടുമ്പോള്, കാർബുറേറ്ററിൽവച്ച് എച്ച ഭഞ്ജിക്കപ്പെടുകയും ജലവാതകവുമായി ചേരുകയും ചെയ്യുന്നു. ഒരു കാർബുരിത ജലവാതകത്തിന്റെ ഘടകശതമാനം താഴെ പറയുന്നവിധം ആണ്: കാർബണ്ഡൈഓക്സൈഡ്-4.3; എഥിലിന്;-4.7; ബെന്സീന്-2.3; ഓക്സിജന്-2.7; കാർബണ്മോണോക്സൈഡ്-32.0; ഹൈഡ്രജന്-34.0; മീഥേന്-15.5; നൈട്രജന്-6.5. ഇതിന്റെ മൊത്തം കലോറികമൂല്യം 534 BTU/ഘനഅടി ആണ്. സൈദ്ധാന്തിക ജ്വാലാതാപാങ്കം 2037.7ºC ആണ്. കാർബുരിത ജലവാതകം നഗരങ്ങളിലെ വാതക പൈപ്പുകളിൽ വിതരണത്തിന് ഉപയോഗിക്കുന്നു.
കൽക്കരിവാതകം
വൊയുസമ്പർക്കമില്ലാതെ ഭഞ്ജകസ്വേദനം ചെയ്യുമ്പോള് കൽക്കരിയിൽ നിന്നു ലഭിക്കുന്ന വാതക ഇന്ധനമാണിത്. ബാഷ്പശീലമുള്ള പദാർഥങ്ങള് താരതമ്യേന കൂടുതലുള്ളയിനം കൽക്കരിയാണ് ഇതിനുപയോഗിക്കുന്നത്. ലംബമോ തിരശ്ചീനമോ ആയ വാലുകകളിൽ ആണ് ഇതുണ്ടാക്കുന്നത്.
കൽക്കരിയുടെ ഇനം, കാർബണീകരണത്തിന്റെ സമയം, ഊഷ്മാവ് എന്നിവയനുസരിച്ച് വാതകത്തിന്റെ തരവും അളവും വ്യത്യാസപ്പെട്ടിരിക്കും. തിരശ്ചീന വാലുകയിൽനിന്നു ലഭിക്കുന്ന മാതൃകാവാതകത്തിന്റെ ഘടകശതമാനം താഴെ കൊടുക്കുന്നു: കാർബണ്ഡൈഓക്സൈഡ്-2.4; എഥിലിന്-1.32; ബെന്സീന്-1.73; ഓക്സിജന്-0.75; കാർബണ് മോണോക്സൈഡ്-7.35; ഹൈഡ്രജന്-47.95; മീഥേന്-27.15; നൈട്രജന്-11.35. ഇതിന്റെ കലോറികമൂല്യം 542 BTU/ഘനഅടിയും. സൈദ്ധാന്തിക ജ്വാലാതാപാങ്കം 1982.22oCഉം ആണ്.
ലംബ വാലുകയിലേക്ക് സാധാരണയായി നീരാവികൂടി കടത്തിവിടുന്നു; ഇത് കോക്കുമായി പ്രതിപ്രവർത്തിച്ച് ജലവാതകം ഉണ്ടാക്കുന്നു; തന്മൂലം കൂടുതൽ വാതകം ലഭിക്കുകയും പുറത്തേക്കു തള്ളപ്പെടുന്ന കോക്ക് തണുക്കുകയും ചെയ്യുന്നു. ഇപ്രകാരം ലഭിക്കുന്ന വാതകത്തിന്റെ കലോറികമൂല്യം 532 BTU/ഘനഅടി ആണ്.
കോക്ക് - അടുപ്പുവാതകം
കോക്കിങ്ങിനു വിധേയമായ ബിറ്റ്യൂമിനീയ കൽക്കരി വായുസമ്പർക്കമില്ലാതെ നാശകസ്വേദനം ചെയ്യുമ്പോള് കിട്ടുന്ന ഉപോത്പന്നമാണിത്. കൽക്കരിവാതകവാലുകകളെക്കാള് വളരെ വലുതാണ് കാർബണീകരണത്തിനുള്ള അറകള്.
സ്വേദനംമൂലം ലഭിക്കുന്ന ബാഷ്പശീലമുള്ള പദാർഥങ്ങളെ ഭാഗികമായി തണുപ്പിക്കുമ്പോള് കുറച്ച് ടാറും ജലവും രൂപീകരിക്കപ്പെടുകയും പിന്നീട് ദ്രവണിത്ര(condenser)ത്തിൽക്കൂടി കടത്തുമ്പോള് കൂടുതൽ ദ്രവീകരണം നടക്കുകയും ടാറും അമോണിയാദ്രാവകവും രണ്ടുധാര(layer)കളായി ലഭിക്കുകയും ചെയ്യുന്നു. ഈ വാതകം ജലമോ സള്ഫ്യൂറിക് അമ്ലമോ ഉപയോഗിച്ച് കഴുകി അമോണിയ മുഴുവന് നീക്കം ചെയ്യാം. ലഘുഎണ്ണകള് ഉപയോഗിച്ച് ബെന്സോള് വീണ്ടെടുക്കുന്നു. പ്രത്യേക ശുദ്ധീകാരികള് ഉപയോഗിച്ച് സള്ഫറിന്റെ സംയുക്തങ്ങളെ നീക്കം ചെയ്യുന്നു. വിഭിന്ന ഘടകങ്ങളെ വേർതിരിച്ചെടുക്കാനുള്ള പദ്ധതികള് വിവിധ വ്യവസായശാലകളിൽ പല തരത്തിലാണ്.
ഒരു മാതൃകാ കോക്ക്-അടുപ്പു വാതകത്തിന്റെ രാസഘടന (ശതമാനത്തിൽ) താഴെ ചേർക്കുന്നു: കാർബണ്ഡൈഓക്സൈഡ്-2.2; എഥിലിന്-3.5; ബെന്സീന്-0.5; ഓക്സിജന്-0.8; കാർബണ്മോണോക്സൈഡ്-6.3; ഹൈഡ്രജന്-46.5; മീഥേന്-32.1; നൈട്രജന്-8.1. മൊത്തം കലോറികമൂല്യം 574 BTU/ഘനഅടി ആണ്.
എണ്ണവാതകം
ഹൈഡ്രാ കാർബണ് സംയുക്തങ്ങള് അടങ്ങിയ എണ്ണയിൽനിന്നു ലഭിക്കുന്ന വാതകമാണിത്. എണ്ണയെ നീരാവി ഉപയോഗിച്ച് വാതകമാക്കി ചൂടുള്ള ചെക്കർ-ഇഷ്ടികകളിൽക്കൂടി കടത്തിവിടുന്നു. അപ്പോള് എണ്ണ ഭഞ്ജിക്കപ്പെടുകയും, ഇഷ്ടികകളിൽ നിക്ഷേപിച്ചിട്ടുള്ള കാർബണുമായി പ്രതിപ്രവർത്തിക്കുകയും ജലവാതകം ഉണ്ടാകുകയും ചെയ്യുന്നു. ഈ പരിണതമിശ്രിതം കാർബുരിത ജലവാതകംപോലെയാണ്. ഉത്പ്രരകം (catalyst)ഉപയോഗിച്ചും എണ്ണവാതകം ഉണ്ടാക്കാം. അവിരതപ്രക്രിയയോ ചക്രീയപ്രക്രിയയോ ഇതിനുപയോഗിക്കാം. അവിരതപ്രക്രിയയിൽ എണ്ണബാഷ്പവും നീരാവിയും ബാഹ്യമായി ചൂടാക്കിയ കുഴലിലുള്ള ഉത്പ്രരകവിതാനത്തിലൂടെ കടത്തിവിടുന്നു. ചക്രീയപ്രചാലനത്തിൽ ഉത്പ്രരകം ഒന്നിടവിട്ട് എച്ചയുടെ ദഹനത്താൽ ചൂടാകുകയും ഭഞ്ജനംമൂലവും കാർബണും നീരാവിയും പ്രതിപ്രവർത്തിക്കുന്നതുമൂലവും തണുക്കുകയും ചെയ്യുന്നു. വായുവുമായോ ഓക്സിജനുമായോ ചേർന്നുള്ള ഭാഗികദഹനംമൂലവും എണ്ണവാതകം ഉണ്ടാക്കാം. എണ്ണവാതകത്തിന്റെ കലോറികമൂല്യം ഏകദേശം 525 മുതൽ 1100 വരെ BTU/ഘനഅടി ആണ്.
നവീകൃത പ്രകൃതിവാതകം
ഭൊഗികമായ ദഹനവും താപമോ ഉത്പ്രരകമോ ഉപയോഗിച്ചുള്ള ഭഞ്ജനവുംമൂലം പ്രകൃതിവാതകത്തിന്റെ താപമൂല്യം കുറയ്ക്കാം. ഇങ്ങനെ ചെയ്യുന്നതുവഴി കാർബുരിത ജലവാതകം, എണ്ണവാതകം, കൽക്കരിവാതകം, കോക്ക്-അടുപ്പു വാതകം എന്നിവയുമായി ചേർത്ത് ഉപയോഗിക്കുന്നു.
ജലവാതകജനിത്രം (generator) ഉപയോഗിച്ചോ, എച്ചവാതകജനിത്രം ഉപയോഗിച്ചോ താപഭഞ്ജനം ചെയ്യാം. ശുഷ്കപ്രകൃതിവാതകത്തിന് കാർബുരിത ജലവാതകത്തിന്റെ ഇരട്ടിയോളം താപമൂല്യമുണ്ട്. ഒരു നവീകൃത പ്രകൃതിവാതകത്തിന്റെ കലോറികമൂല്യം 599 BTU/ഘനഅടി ആണ്.
പ്രകൃതിവാതകം
ഭൂഗർഭത്തിൽനിന്നു നേരിട്ടു ലഭിക്കുന്ന വാതകം. പെട്രാളിയവുമായി ബന്ധപ്പെട്ടോ, പെട്രാളിയമുള്ള സ്ഥലങ്ങളിലോ ഇത് കാണപ്പെടുന്നു: പ്രാപ്പേന്, ബ്യൂട്ടേന്, പെന്ടേന് എന്നിവ ധാരാളമായി കാണുകയാണെങ്കിൽ ആ വാതകത്തെ ആർദ്രപ്രകൃതിവാതകം (wet natural gas)എന്നും വാതകത്തിൽ ഉയർന്ന തന്മാത്രാഭാരം ഉള്ള പദാർഥങ്ങള് കാണപ്പെടുന്നില്ലെങ്കിൽ ശുഷ്കപ്രകൃതിവാതകമെന്നും (dry natural gas) പെറയുന്നു. പ്രകൃതിവാതകത്തിൽ പ്രധാനമായും മീഥേന് ആണ് കാണപ്പെടുന്നത്. ചെറിയ അളവിൽ ഈഥേനും നിഷ്ക്രിയവാതകങ്ങളും ഉണ്ട്. ഇതിന്റെ കലോറികമൂല്യം ഏകദേശം 1,000 മുതൽ 1,100 വരെ BTU/ഘനഅടി ആയിരിക്കും. ഒരു മാതൃകാവാതകത്തിന്റെ ചേരുവശതമാനം താഴെക്കൊടുക്കുന്നു: മീഥേന്-80.50; ഈഥേന്-18.20; നൈട്രജന്-1.30.
അസെറ്റിലീന്
ലോഹങ്ങള് മുറിക്കുന്നതിനും വെൽഡിങ്ങിനും മറ്റും ഉയർന്ന ജ്വാലാതാപം (flame temperature) ആവശ്യമുള്ളപ്പോള് അസെറ്റിലീന് ഉപയോഗിക്കുന്നു. ചില ഒറ്റപ്പെട്ട സ്ഥലങ്ങളിൽ വെളിച്ചം വിതറുന്നതിനും ഇത് പ്രയോജനപ്പെടുത്താറുണ്ട്. കാത്സ്യം കാർബൈഡും വെള്ളവും പ്രതിപ്രവർത്തിച്ചാണ് ഇത് ഉണ്ടാകുന്നത്. പ്രകൃതിവാതകമോ എച്ച ശുദ്ധീകരണശാലയിലെ വാതകങ്ങളോ രൂപാന്തരപ്പെടുത്തി അസെറ്റിലീന് ഉത്പാദിപ്പിക്കാം.
അസെറ്റിലീന്റെ മൊത്തം കലോറികമൂല്യം 1,499 BTU/ഘനഅടി ആകുന്നു; വായുവിൽ ദഹിക്കുമ്പോള് ഉള്ള സൈദ്ധാന്തിക ജ്വാലാതാപാങ്കം 2320oC. ഒരു വ്യാപ്തം അസെറ്റിലീന്, 1.4 വ്യാപ്തം ഓക്സിജനുമായി ദഹിക്കുമ്പോള് ലഭിക്കുന്ന ജ്വാലാതാപാങ്കം 3371oC ആണ്. ചില വെൽഡിങ്ങിനും മറ്റും ഈ ഊഷ്മാവ് ആവശ്യമായിവരുന്നു. ചെറിയ ഉപഭോക്താക്കള്ക്ക് ഉന്നതമർദത്തിൽ സിലിണ്ടറുകളിലാക്കിയും പൈപ്പ് ഉപയോഗിച്ചും അസെറ്റിലീന് വിതരണം ചെയ്യുന്നു. വിവിധ രാസപദാർഥങ്ങള് ഉണ്ടാക്കാനും ഇത് ഉപയോഗിക്കുന്നുണ്ട്.
ദ്രവീകൃത പെട്രാളിയം വാതകം
പെട്രാളിയം ശുദ്ധീകരണശാലകളിലും പ്രകൃതിവാതകത്തിലുംനിന്ന് ഈ വാതകം നിർമിക്കാം. ഈ വാതകത്തിൽ പ്രാപ്പേനും ബ്യൂട്ടേനും വ്യത്യസ്താനുപാതങ്ങളിൽ കാണപ്പെടുന്നു. ഈ വാതകം ദ്രാവകാവസ്ഥയിൽ സിലിണ്ടറുകളിലും മറ്റും ലഭിക്കുന്നു. ബാഷ്പീകരിക്കപ്പെടുമ്പോള് വാതകജ്വാലകങ്ങളിൽ(gas burner)) ഉപയോഗിക്കാം. ഈ വാതകത്തിന്റെ കലോറികമൂല്യം ഏകദേശം 2,500 മുതൽ 3,500 വരെ BTU/ഘനഅടി ആണ്. ഇത് പ്രകൃതിവാതകത്തിന്റേതിനെക്കാള് കൂടുതലാണ്.
പാചകം ചെയ്യുന്നതിനും, മറ്റു ഗാർഹികാവശ്യങ്ങള്ക്കും ഇത് ഉപയോഗിക്കാം. മോട്ടോർവാഹനങ്ങള്ക്കും ഇത് ഉപയോഗപ്പെടുത്താം. പൈപ്പുമുഖേനയും വിതരണം ചെയ്യപ്പെടുന്നുണ്ട്.
മേന്മ
വാതക ഇന്ധനങ്ങളുടെ ദഹനം വേഗത്തിൽ നിയന്ത്രിക്കാം; ദഹനവേഗത ആവശ്യത്തിനനുസരിച്ച് വ്യത്യാസപ്പെടുത്തുകയും ചെയ്യാം. വായുവുമായി എളുപ്പത്തിൽ കലരുന്നതുമൂലം ഖര-ദ്രവ ഇന്ധനങ്ങളുടെ ദഹനത്തിന് ആവശ്യമുള്ളത്ര വായു (excess air) ഇതിനാവശ്യമില്ല. വിവിധ ഊഷ്മാവിൽ ഓക്സീകരണജ്വാലയോ നിരോക്സീകരണജ്വാലയോ ലഭിക്കുന്നതിനുള്ള സൗകര്യവും ഉണ്ട്. ഇതെല്ലാം ചൂളയുടെ ലാഭകരമായ പ്രവർത്തനത്തിനും, ക്ഷമതയ്ക്കും സഹായകമാണ്.
ഉപയോഗത്തിൽ ഉയർന്ന താപക്ഷമത നല്കുന്നു. പുകയുടെയും ചാരത്തിന്റെയും അഭാവമാണ് മറ്റൊരു പ്രത്യേകത. ദഹനത്തിന്റെ വേഗത, ജ്വാലയുടെ നീളം എന്നിവ വാതകത്തിന്റെയും പ്രഥമവും ദ്വിതീയവും (primary and secondary)ആയി ഉപയോഗിക്കുന്ന വായുവിന്റെയും അളവ് ക്രമപ്പെടുത്തി നിയന്ത്രിക്കാവുന്നതാണ്.
ഉപയോഗങ്ങള്
വാതകജ്വാലകങ്ങള്
വൊതകജ്വാലകങ്ങള് രണ്ടുതരത്തിലുണ്ട്. ദഹനത്തിനുമുമ്പ് വാതകവും വായുവും കൂട്ടിക്കലർത്തുകയോ, കലർത്താതിരിക്കുകയോ ചെയ്യുന്നതനുസരിച്ചാണ് ഈ തരംതിരിവ്. ചില ചൂളകളിൽ സാമാന്യം നീളമുള്ള ജ്വാല ലഭിക്കുന്നതിന് വാതകം പ്രാഥമിക വായുവിന്റെ സഹായമില്ലാതെതന്നെ കത്തിക്കുന്നു. പരമാവധി ജ്വാലാതാപാങ്കം ആവശ്യമായിവരുമ്പോഴോ, ദഹനാന്തരീക്ഷം കുറവായിരിക്കുമ്പോഴോ, ബുന്സന് (bunsen) മാതൃകയിലുള്ള ജ്വാലകങ്ങള് ഉപയോഗിക്കാം. ഈ ജ്വാലകത്തിൽ ചെറിയ ജ്വാലകൊണ്ടുതന്നെ വർധിച്ച തോതിലുള്ള ദഹനം സാധ്യമാണ്.
നിമഗ്നദഹനം
ജലം ചൂടാക്കുന്നതിനും നീരാവി ഉത്പാദിപ്പിക്കുന്നതിനും മറ്റും വാതകത്തെ ജലത്തിൽവച്ചുതന്നെ ദഹിപ്പിക്കാം. ഇപ്രകാരമുള്ള ദഹനത്തിന്, ആവശ്യമായ പ്രാഥമികവായു വാതകവുമായി കൂട്ടിക്കലർത്തിയിരിക്കണം. ചില ലായനികള് തിളപ്പിക്കുമ്പോള് താപപ്രസരണപ്രതലങ്ങളിൽ ലവണങ്ങളോ മറ്റോ അടിഞ്ഞുകൂടാന് ഇടയുണ്ട്. ഇത് താപപ്രസരണക്ഷമത കുറയ്ക്കുന്നു. ഇതൊഴിവാക്കാന് നിമഗ്നദഹനജ്വാലകങ്ങള് ഉപയോഗിക്കാം. ദഹനവാതകങ്ങള് ലായനിയിൽ നേരിട്ട് പ്രവേശിക്കുന്നു. കുമിളകളായി ലായനികളിലൂടെ പുറത്തുപോകുന്നു.
പ്രതലദഹനം
ചൂടാക്കിയ പ്ലാറ്റിനം കമ്പി വായുവും കൽക്കരിവാതകവും ചേർന്ന ഒരു മിശ്രിതത്തിൽ കാണിച്ചാൽ ധവളോജ്ജ്വലമാകുകയും ഓക്സിജന് തീരുന്നതുവരെ ജ്വാലയില്ലാതെ തുടർന്ന് എരിയുകയും ചെയ്യുന്നു. ഹംഫ്രി ഡേവിയാണ് ഇതു കണ്ടുപിടിച്ചത്. മറ്റു ചില പദാർഥങ്ങള്ക്കും ഈ കഴിവ് ഉള്ളതായി കണ്ടുപിടിക്കപ്പെട്ടിട്ടുണ്ട്. വാതകങ്ങളുടെ ദഹനം ത്വരിപ്പിക്കാനുള്ള കഴിവ് താപനില വർധിക്കുന്തോറും കൂടിവരും. ഇത് ചില വ്യവസായങ്ങളിൽ ഉപയോഗപ്പെടുത്തുന്നുണ്ട്.
ചൂടുള്ള ഉച്ചതാപസഹ (refractory) പ്രതലം ജ്വാലയിൽനിന്ന് താപം സ്വീകരിക്കുകയും താരതമ്യേന തണുത്ത ദഹനമിശ്രിതത്തിന് താപം നല്കുകയും ചെയ്യുന്നു. ഇത് ദഹനത്തിന്റെ വേഗത കൂട്ടുന്നു. ആവശ്യമുള്ളിടത്തുമാത്രം ദഹനം, കൂടുതൽ വായുവിന്റെ ആവശ്യമില്ലായ്മ, ഉയർന്ന താപനില, വികിരണം (radiation) മൂലമുള്ള ത്വരിതതാപപ്രസരണം എന്നിവ പ്രതലദഹനത്തിന്റെ മേന്മകളാണ്.
അണുക ഇന്ധനങ്ങള്
സാധാരണ ഇന്ധനങ്ങളെ അപേക്ഷിച്ച് കൂടുതൽ ഊർജം നല്കുന്നത് അണുക ഇന്ധനങ്ങളാണ്; ഓക്സിജന്റെ ആവശ്യവും ഇല്ല. അണുവിഖണ്ഡനം (nuclear fission) ആണ് ഇതിനുപയോഗിക്കുന്നത്. ഉയർന്ന അണുസംഖ്യയുള്ള ചില ഐസോടോപ്പുകളുടെ അണുകേന്ദ്രത്തിലേക്ക് ന്യൂട്രാണ് വേധം നടത്തിയാൽ അവ വിഖണ്ഡനത്തിനു വിധേയമാകുകയും വന്തോതിൽ ഊർജം വിസർജിക്കുകയും ചെയ്യുന്നു; ഇതു വഴി കൂടുതൽ ന്യൂട്രാണുകളും ഉത്പാദിപ്പിക്കപ്പെടുന്നു. ഈ ന്യൂട്രാണുകള് വീണ്ടും അണുവിഖണ്ഡനം നടത്തിയാൽ തുടർച്ചയായി ഊർജം ഉത്പാദിപ്പിക്കാന് കഴിയും. ഇപ്രകാരമുള്ള ഇന്ധനങ്ങളാണ് യുറേനിയം-235 ((U235), യുറേനിയം-233 ((U233), പ്ലൂട്ടോണിയം-239 (Pu239) മുതലായവ. ഇവയെ അണുക ഇന്ധനങ്ങളെന്നു വിളിക്കുന്നു.
ഇവയിൽ ഡ235 മാത്രമേ പ്രകൃതിയിൽ കണ്ടുവരുന്നുള്ളൂ. മറ്റുരണ്ടും കൃത്രിമമായി ഉണ്ടാക്കുന്നു. തോറിയം-232 (Th232) ന്യൂട്രാണ് ആഗിരണം ചെയ്യുമ്പോള് യുറേനിയം-233 ((U233)-ഉം, യുറേനിയം-238 (U238) ന്യൂട്രാണ് ആഗിരണം ചെയ്യുമ്പോള് പ്ലൂട്ടോണിയം-239 (Pu239)-ഉം ലഭിക്കുന്നു. പ്ലൂട്ടോണിയം-239 ഉം, യുറേനിയം-233 ഉം ന്യൂക്ലിയർ ബോംബുകള് നിർമിക്കാനും ഉപയോഗിക്കുന്നു.
റോക്കറ്റ് ഇന്ധനങ്ങളും മറ്റ് ഉന്നതോർജ ഇന്ധനങ്ങളും
ജെറ്റ് എന്ജിന്റെയും റോക്കറ്റ് എന്ജിന്റെയും ആവിർഭാവത്തോടുകൂടി ഹൈഡ്രാകാർബണ് ഇന്ധനങ്ങളെക്കാള് ഫലപ്രദമായി പ്രവർത്തിക്കുന്ന ഇന്ധനങ്ങള് ആവശ്യമായിവന്നു. കുറച്ചുമാത്രം ഇന്ധനമുപയോഗിച്ച് പരമാവധി താപം ലഭ്യമാക്കേണ്ടതായും വന്നു. അങ്ങനെയാണ് റോക്കറ്റ് ഇന്ധനങ്ങളുടെയും മറ്റ് ഉന്നതോർജ ഇന്ധനങ്ങളുടെയും ആവിർഭാവം. റോക്കറ്റിൽ ഉപയോഗിക്കുന്ന രാസപദാർഥങ്ങളെ പൊതുവേ പ്രാപെല്ലന്റ് (Propellant)എന്നു പറയുന്നു. ഇതിൽ ഇന്ധനവും-ഓക്സീകാരകവും മറ്റു പദാർഥങ്ങളും അടങ്ങിയിരിക്കും. പ്രാപെല്ലന്റ് ഇന്ധനങ്ങളെ ദ്രവമെന്നും ഖരമെന്നും രണ്ടായി തിരിക്കാം.
1. ദ്രവപ്രാപെല്ലന്റുകള്. എന്ജിന്റെ ദഹന അറയിലേക്ക് പ്രവേശിക്കുന്ന ദ്രവപദാർഥമാണിത്. ഇതിൽ ഇന്ധനവും ഓക്സീകാരകവും ഉത്പ്രരകവും ചില നിഷ്ക്രിയപദാർഥങ്ങളും അടങ്ങിയിരിക്കുന്നു. ദ്രവപ്രാപെല്ലന്റ് ഉപയോഗിക്കുന്ന റോക്കറ്റ് എന്ജിനുകള് സാധാരണയായി ബൈ-പ്രാപെല്ലന്റ് (Bi-propellant) വ്യേവസ്ഥയാണ് ഉപയോഗിക്കുന്നത്. ഇതിൽ ഇന്ധനവും ഓക്സീകാരകവും വെണ്ണേറെ സൂക്ഷിച്ചുവയ്ക്കുകയും ദഹന അറയിലേക്ക് വെണ്ണേറെ പ്രവേശിപ്പിക്കുകയും ചെയ്യുന്നു. മോണോപ്രാപെല്ലന്റ് വ്യവസ്ഥയിൽ ഓക്സീകാരകവും ഇന്ധനവും ഒരുമിച്ച് മിശ്രിതമായി ഉപയോഗിക്കുന്നു. അമോണിയ, എഥിൽ ആൽക്കഹോള്, എഥിലിന് ഓക്സൈഡ് ഹൈഡ്രാസിന് (Hydrazine), JP-4 (ഒരു പെട്രാളിയ ഘടകം), അണ്സിമെട്രിക്കൽ ഡൈ മെഥിൽ ഹൈഡ്രാസിന് (UDMH-Unsymmetrical Dimethyl Hydrazine) മുതലായവയാണ് ദ്രവപ്രാപെല്ലന്റ് ഇന്ധനങ്ങളിൽ ചിലവ. ബോറോണ് സംയുക്തങ്ങളും ഉന്നത ഊർജം നല്കുന്ന ഇന്ധനങ്ങളാണ്.
റോക്കറ്റ് ഇന്ധനങ്ങളുടെ പ്രവർത്തനക്ഷമത അളക്കുന്നത് വിശിഷ്ടആവേഗം (Specific impulse)ഉപയോഗിച്ചാണ്. ഒരു സെക്കന്ഡിൽ ഒരു പൗണ്ട് പ്രാപെല്ലന്റ് ഉപയോഗിച്ചാൽ ഉണ്ടാകുന്ന പൗണ്ട്ബല(Pound force)ത്തെയാണ് വിശിഷ്ടആവേഗം എന്നു പറയുന്നത്.
റോക്കറ്റ് എന്ജിന്റെ പ്രണോദം (Thrust) അതിൽ ഉപയോഗിക്കുന്ന ഇന്ധനത്തിന്റെ തരത്തെയോ അതിൽ അടങ്ങിയിരിക്കുന്ന ഊർജത്തെയോ മാത്രമല്ല പ്രത്യുത, ഓക്സീകാരകത്തിന്റെ തരത്തെയും ദഹനശേഷം പുറന്തള്ളപ്പെടുന്ന വാതകങ്ങളുടെ തന്മാത്രാഭാരത്തെയും കൂടി ആശ്രയിച്ചിരിക്കും.
2. ഖരപ്രാപെല്ലന്റുകള്. റോക്കറ്റ് എന്ജിനുകളിൽ ഉപയോഗിക്കുന്ന ഖരരാസപദാർഥങ്ങളാണ് ഖരപ്രാപെല്ലന്റുകള്. ആവശ്യമായ മറ്റു ഗുണങ്ങള്ക്കു പുറമേ ഇതിന് ഉറപ്പും ഉണ്ടായിരിക്കണം. സാധാരണ ഉപയോഗിക്കുന്ന ഖരപ്രാപെല്ലന്റുകളെ ഭിന്നാത്മകം (Heterogeneous), ഏകാത്മകം (Homogeneous)എന്നിങ്ങനെ രണ്ടായി വിഭജിക്കാം. ഭിന്നാത്മക പ്രാപെല്ലന്റുകളിൽ ഓക്സീകാരകവും നിരോക്സീകാരകവും വെണ്ണേറെ അവസ്ഥകളിൽ (phases) കൊണുന്നു. ഏകാത്മക പ്രാപെല്ലന്റിൽ ഓക്സീകാരകവും നിരോക്സീകാരകവും ഒന്നായോ അഥവാ കൊളോയ്ഡീയ (colloidal) മിശ്രിതമായോ കാണപ്പെടുന്നു.
ഓക്സീകാരകം ഒരു ബന്ധക വസ്തു(binder)വിൽ പരിക്ഷേപിച്ചാണ് (dispersed) ഖര റോക്കറ്റ് പ്രാപെലന്റ് ഉണ്ടാക്കുന്നത്. ഈ ബന്ധകവസ്തു ഇന്ധനമായി വർത്തിക്കുന്നു. സാധാരണയായി പ്ലാസ്റ്റിക്, റെസിന്, കൃത്രിമ റബ്ബർ സംയുക്തങ്ങള് എന്നിവയാകാം ഇവ.
ഏകാത്മക പ്രാപെല്ലന്റുകളിൽ നൈട്രാഗ്ലിസറിനും, നൈട്രാസെല്ലുലോസും അടങ്ങിയിരിക്കുന്നു. ഭിന്നാത്മക പ്രാപെല്ലന്റുകളിൽ പോളിസള്ഫൈഡ്, പോളിയുറീതേന്, പ്ലാസ്റ്റിസോള് മുതലായവ ഉപയോഗിക്കാം. ഏറോപ്ലെക്സ്, ആസ്ട്രാഡയിന് (Astro-dyne) മുതലായ പേരുകളിൽ അറിയപ്പെടുന്ന ഭിന്നാത്മക പ്രാപെല്ലന്റുകള് പോളിയെസ്റ്റർ, കൃത്രിമ റബ്ബർ എന്നിവ യഥാക്രമം അടിസ്ഥാനമായുള്ള പ്രാപെല്ലന്റുകളാണ്. ഓക്സീകാരകമായി പൊട്ടാസ്യം പെർക്ലോറേറ്റ്, അമോണിയം നൈട്രറ്റ്, പൊട്ടാസ്യം നൈട്രറ്റ്, ലിഥിയം പെർക്ലോറേറ്റ് എന്നിവയും ഉപയോഗിക്കുന്നു.
ഇന്ധനങ്ങള് ഇന്ത്യയിൽ
ഇന്ത്യയിലെ ഏകദേശം 80 ശതമാനത്തോളം വരുന്ന ഗ്രാമീണജനത പ്രധാനമായും ചാണകം, വിറക് മുതലായവ ഇന്ധനമായി ഉപയോഗിക്കുന്നു. ചാണകത്തിൽനിന്ന് ഗോബർഗ്യാസ് ഉണ്ടാക്കുന്ന പ്രക്രിയയ്ക്കും പ്രചാരം ലഭിച്ചുതുടങ്ങിയിട്ടുണ്ട്.
കൽക്കരി
1774-ൽ ആണ് ആദ്യമായി കൽക്കരി ഇന്ത്യയിൽ ഖനനം ചെയ്തത്. ബംഗാളിലുള്ള റാണിഗഞ്ചിലാണ് ആദ്യത്തെ ഖനികള്. ഭൂഗർഭസർവേയുടെ ഫലമായി കൂടുതൽ കൽക്കരിഖനികള് കണ്ടുപിടിക്കപ്പെട്ടു. അവയിൽ ഏകദേശം പകുതിയിൽ അധികവും ബിഹാർ-ബംഗാള് മേഖലയിലാണ്.
പ്രധാനപ്പെട്ട കൽക്കരിഖനികള് പശ്ചിമബംഗാളിലെ റാണിഗഞ്ചിലും ബിഹാറിലെ ഝാരിയ, ബൊക്കാറോ മുതലായ സ്ഥലങ്ങളിലുമാണ് സ്ഥിതിചെയ്യുന്നത്. കൽക്കരി ലഭിക്കുന്ന മറ്റു സംസ്ഥാനങ്ങള് മധ്യപ്രദേശ്, ഒഡിഷ, ആന്ധ്രപ്രദേശ്, തമിഴ്നാട്, മഹാരാഷ്ട്ര, അസം, രാജസ്ഥാന്, കാശ്മീർ മുതലായവയാണ്. തെക്കേ ഇന്ത്യയിൽ കോക്കിങ് കൽക്കരി കാണപ്പെടുന്നില്ല.
പീറ്റ്, ഹൂഗ്ലി നദിയുടെ ഇരുകരകളിലും തെക്കേ ഇന്ത്യയിലെ നീലഗിരിക്കുന്നുകളിലും കാണപ്പെടുന്നു. ലിഗ്നൈറ്റ് പ്രധാനമായി ഉത്പാദിപ്പിക്കുന്നത് തമിഴ്നാട്ടിലെ നെയ്വേലിയിലാണ്. രാജസ്ഥാനിലെ പലാനയിലും, കാരിയിലും ജമ്മു-കാശ്മീരിലെ നിച്ചഹം, ഗുജറാത്തിലെ കച്ച്, ഭരോച് തുടങ്ങിയ ജില്ലകളിലും ലിഗ്നൈറ്റ് കണ്ടുവരുന്നു. ആന്ഥ്രസൈറ്റ് കാശ്മീരിലും ഡാർജിലിങ്ങിലും ആണ് ഉള്ളത്. ഝാരിയയിലും ബാരാകഡിലും കാണപ്പെടുന്ന കൽക്കരിയിൽ ഏകദേശം 3 ശതമാനം ജലാംശം ആണ്. ബാഷ്പശീലമുള്ള പദാർഥം താരതമ്യേന കുറവാണ്; ഏകദേശം 21-30 ശതമാനം. റാണിഗഞ്ചിലെ കൽക്കരിയെ അപേക്ഷിച്ച് ഇതിന് കലോറികമൂല്യം കൂടുതലാണ്. ചെറിയ ജ്വാലയോടെ കത്തുന്നതുകൊണ്ട് നീരാവിഎന്ജിനു(തീവണ്ടി)കളിലും മറ്റും ഉപയോഗിക്കുന്നു. ലോഹകർമീയകോക്ക് ഉണ്ടാക്കാനും ഉപകരിക്കുന്നു. റാണിഗഞ്ചിലെ കൽക്കരിയിലെ ജലാംശം 3-10 ശതമാനം വരും. ബാഷ്പശീലമുള്ള പദാർഥം 30-40 ശതമാനം കാണപ്പെടുന്നു. നീണ്ട ജ്വാലയോടെ കത്തുന്നു. ഇതിന് കോക്കിങ് സ്വഭാവമില്ല. വാതകമുണ്ടാക്കാന് ഉപയോഗിക്കുന്നു. കൂടാതെ ബോയിലറുകളിലും മറ്റും ഇത് ഉപയോഗപ്പെടുത്തുന്നുണ്ട്.
അസം കൽക്കരിയിൽ ചാരാംശം കുറവാണെങ്കിലും സള്ഫർ 3-8 ശതമാനം വരെ കാണുന്നു. അതുകൊണ്ട് ലോഹകർമീയകോക്ക് ഉണ്ടാക്കാന് ഉപയോഗിക്കുന്നില്ല. ഇന്ത്യയിൽ ബിറ്റ്യൂമിനീയ കൽക്കരിനിക്ഷേപം കുറവായതുകൊണ്ട് കൽക്കരി കഴുകി (coal washing) ചാരാംശം കളഞ്ഞും മറ്റുള്ള കൽക്കരിയുമായി ചേർത്തും ലോഹകർമീയകോക്ക് ഉണ്ടാക്കാന് ഉപയോഗിക്കുന്നു. ഇന്ത്യയിൽ ഉത്പാദിപ്പിക്കുന്ന കൽക്കരിയിലെ മൂന്നിൽ ഒരു ഭാഗം ഉപയോഗിക്കുന്നത് റെയിൽവേയാണ്. ഏകദേശം ആറിലൊന്ന് ലോഹകർമീയകോക്ക് ഉണ്ടാക്കാന് ഉപയോഗിക്കുന്നു. ഇന്ത്യയിലെ എല്ലാത്തരം കൽക്കരികളുടെയും മൊത്തം ശേഖരം 25,738 കോടി ടണ് ആയി കണക്കാക്കപ്പെട്ടിരിക്കുന്നു. കോക്കിങ്കൽക്കരിസമ്പത്ത് ഏകദേശം 2,46,130 ലക്ഷം ടണ്വരും.
പെട്രാളിയവും പ്രകൃതിവാതകവും
ഇന്ത്യയിൽ ആദ്യമായി പെട്രാളിയം കണ്ടെത്തുന്നത് 1889-ൽ അസമിലെ ദിഗ്ബോയിയിലാണ്. ഗുജറാത്തിലെ അങ്കലേശ്വറിലും അസമിലെ നഹാർഖാട്ടിയയിലും എച്ചപ്പാടങ്ങള് ഉണ്ട്. മുംബൈക്കടുത്ത് കടൽത്തറയിൽനിന്നും എച്ച ഉത്പാദിപ്പിച്ചുവരുന്നു. സമീപകാലത്ത് രാജസ്ഥാനിലും, ആന്ധ്രപ്രദേശിലെ കൃഷ്ണ ഗോദാവരി ഡെൽറ്റയിലും എച്ചയും പ്രകൃതിവാതകവും കണ്ടെത്തുകയും ഉത്പാദനം ആരംഭിക്കുകയും ചെയ്തിട്ടുണ്ട്.
ഗുജറാത്ത്, അസം എന്നീ സംസ്ഥാനങ്ങളിലാണ് പെട്രാളിയം ഉറവിടങ്ങള് കൂടുതലും ഉള്ളത്. എച്ച ഉത്പാദനത്തിൽ മുമ്പന്തിയിൽ നിൽക്കുന്നത് പൊതുമേഖലാ സ്ഥാപനമായ GAIL(Oil and Natural Gas Corporation) ആണ്. GAIL (Gas Authority of India)യാണ് പ്രകൃതിവാതക രംഗത്തെ പ്രമുഖ സ്ഥാപനം. ബർമാഷെൽ, എസ്സോ, കാൽടെക്സ്, അസം ഓയിൽക്കമ്പനി, ഗുവാഹത്തി, ബറൗണി, കൊയാലി, കൊച്ചി, ചെന്നൈ എന്നിവിടങ്ങളിലും മികച്ച എച്ച ശുദ്ധീകരണ ശാലകള് പ്രവർത്തിക്കുന്നുണ്ട്. ഇന്ത്യയിൽ ഉത്പാദിപ്പിക്കുന്ന പ്രധാന പെട്രാളിയം ഉത്പന്നങ്ങള് താഴെ പറയുന്നവയാണ്; ദ്രവീകൃത പെട്രാളിയം വാതകം (LPG), മോട്ടോർ സ്പിരിറ്റ്, വ്യോമയാന ഇന്ധനം, മണ്ണെണ്ണ, ഏവിയേഷന് ടർബൈന് ഇന്ധനം (Aviation Turbine Fuel), ഹൈസ്പീഡ് ഡീസൽ, ലൈറ്റ് ഡീസൽ എണ്ണ, ഫർണസ് എണ്ണ, ബിറ്റ്യൂമന്, സ്നേഹകഎണ്ണകള്. ആകെ ഉപയോഗത്തിന്റെ 6 ശതമാനം പെട്രാളും 70 ശതമാനം ഇന്ധന എണ്ണ, ഡീസൽ എണ്ണ, എണ്ണഎന്നിവയും ആകുന്നു.
ഇന്ത്യയിലെ പ്രകൃതിവാതക നിക്ഷേപം ഏകദേശം 52.8 ബില്ല്യണ് ക്യുബിക് മീറ്റർ ആയി കണക്കാക്കപ്പെട്ടിരിക്കുന്നു. നോ. ഇന്ത്യ, കൽക്കരി; പെട്രാളിയം; ഇന്ത്യന് ഓയിൽ കോർപ്പറേഷന്
(വി.കെ. ശശികുമാർ; പ്രാഫ. കെ. പാപ്പൂട്ടി; സ.പ.)