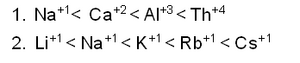This site is not complete. The work to converting the volumes of സര്വ്വവിജ്ഞാനകോശം is on progress. Please bear with us
Please contact webmastersiep@yahoo.com for any queries regarding this website.
Reading Problems? see Enabling Malayalam
അയോണ് വിനിമയം
സര്വ്വവിജ്ഞാനകോശം സംരംഭത്തില് നിന്ന്
(→അയോണ് വിനിമയം) |
Mksol (സംവാദം | സംഭാവനകള്) (→അയോണ് വിനിമയം) |
||
| (ഇടക്കുള്ള ഒരു പതിപ്പിലെ മാറ്റം ഇവിടെ കാണിക്കുന്നില്ല.) | |||
| വരി 4: | വരി 4: | ||
പരസ്പര സമ്പര്ക്കത്തിലുള്ള ഒരു ഇലക്ട്രോലൈറ്റ് ലായനിയും അലേയ ഖര വസ്തുവും തമ്മില് ഒരേ ചാര്ജുള്ള അയോണുകള് കൈമാറ്റം ചെയ്യുന്ന പ്രക്രിയ. ഒരു രാസപ്രവര്ത്തനം തന്നെയാണ് ഇത്. ഖരവസ്തുവും ലായനിയും ചേര്ന്ന വ്യൂഹം രണ്ടു ലായനികളോ രണ്ടു വാതകങ്ങളോ ചേര്ന്നുണ്ടാവുന്നതുപോലുള്ള ഒരു സജാതീയവ്യൂഹം (homogeneous system) അല്ല; വിജാതീയ വ്യൂഹം (heterogeneous system) ആണ്. ഇലക്ട്രൊലൈറ്റ്-ലായനി എന്നതുകൊണ്ട് ഉദ്ദേശിക്കുന്നത് ലീനവസ്തുവിന്റെ അയോണുകള് സ്വതന്ത്രമായി സ്വച്ഛന്ദം ചലിച്ചുകൊണ്ടിരിക്കുന്ന ലായനി എന്നാണ്. സാധാരണയായി അയോണ് വിനിമയം എന്ന പ്രതിഭാസം വിജാതീയവ്യൂഹങ്ങളിലാണ് നടക്കുന്നത്. എങ്കിലും മറ്റു അന്തരാപ്രതലങ്ങളിലും (inter-faces) ഇതു നടക്കാറുണ്ട്. ഉദാഹരണമായി അന്യോന്യം കലര്ന്നുചേരാത്ത രണ്ടു ഇലക്ട്രൊലൈറ്റ് ലായനികളില് മൂന്നാമതൊരു ഇലക്ട്രൊലൈറ്റിന്റെ വിതരണം അയോണ് വിനിമയമായി പരിഗണിക്കപ്പെടുന്നു. സിലിക്കേറ്റുകള്, ഫോസ്ഫേറ്റുകള്, ഫ്ലൂറൈഡുകള്, സെലുലോസ്, കമ്പിളിപ്രോട്ടീനുകള്, റെസിനുകള്, ലിഗ്നിന്, ഗ്ലാസ് എന്നു വേണ്ട ബേരിയം സള്ഫേറ്റ്, സില്വര് ക്ലോറൈഡ് മുതലായ അവക്ഷിപ്തങ്ങളില്വരെ അയോണ് വിനിമയം നടക്കുന്നതായി കണ്ടുപിടിച്ചിട്ടുണ്ട്. ഈ പ്രതിഭാസം വിനിമയ-അധിശോഷണം (exchange adsorption) ആയും ക്ഷാരവിനിമയം (alkali exchange) ആയും വിവരിക്കപ്പെട്ടിരിക്കുന്നു. | പരസ്പര സമ്പര്ക്കത്തിലുള്ള ഒരു ഇലക്ട്രോലൈറ്റ് ലായനിയും അലേയ ഖര വസ്തുവും തമ്മില് ഒരേ ചാര്ജുള്ള അയോണുകള് കൈമാറ്റം ചെയ്യുന്ന പ്രക്രിയ. ഒരു രാസപ്രവര്ത്തനം തന്നെയാണ് ഇത്. ഖരവസ്തുവും ലായനിയും ചേര്ന്ന വ്യൂഹം രണ്ടു ലായനികളോ രണ്ടു വാതകങ്ങളോ ചേര്ന്നുണ്ടാവുന്നതുപോലുള്ള ഒരു സജാതീയവ്യൂഹം (homogeneous system) അല്ല; വിജാതീയ വ്യൂഹം (heterogeneous system) ആണ്. ഇലക്ട്രൊലൈറ്റ്-ലായനി എന്നതുകൊണ്ട് ഉദ്ദേശിക്കുന്നത് ലീനവസ്തുവിന്റെ അയോണുകള് സ്വതന്ത്രമായി സ്വച്ഛന്ദം ചലിച്ചുകൊണ്ടിരിക്കുന്ന ലായനി എന്നാണ്. സാധാരണയായി അയോണ് വിനിമയം എന്ന പ്രതിഭാസം വിജാതീയവ്യൂഹങ്ങളിലാണ് നടക്കുന്നത്. എങ്കിലും മറ്റു അന്തരാപ്രതലങ്ങളിലും (inter-faces) ഇതു നടക്കാറുണ്ട്. ഉദാഹരണമായി അന്യോന്യം കലര്ന്നുചേരാത്ത രണ്ടു ഇലക്ട്രൊലൈറ്റ് ലായനികളില് മൂന്നാമതൊരു ഇലക്ട്രൊലൈറ്റിന്റെ വിതരണം അയോണ് വിനിമയമായി പരിഗണിക്കപ്പെടുന്നു. സിലിക്കേറ്റുകള്, ഫോസ്ഫേറ്റുകള്, ഫ്ലൂറൈഡുകള്, സെലുലോസ്, കമ്പിളിപ്രോട്ടീനുകള്, റെസിനുകള്, ലിഗ്നിന്, ഗ്ലാസ് എന്നു വേണ്ട ബേരിയം സള്ഫേറ്റ്, സില്വര് ക്ലോറൈഡ് മുതലായ അവക്ഷിപ്തങ്ങളില്വരെ അയോണ് വിനിമയം നടക്കുന്നതായി കണ്ടുപിടിച്ചിട്ടുണ്ട്. ഈ പ്രതിഭാസം വിനിമയ-അധിശോഷണം (exchange adsorption) ആയും ക്ഷാരവിനിമയം (alkali exchange) ആയും വിവരിക്കപ്പെട്ടിരിക്കുന്നു. | ||
| - | '''ചരിത്രം.''' വളര്ച്ചയ്ക്ക് അത്യന്താപേക്ഷിതമായ അമോണിയയെ ചെടികള് മണ്ണില്നിന്നു വലിച്ചെടുക്കുന്നത് എങ്ങനെയാണ് എന്ന വിഷയത്തെപ്പറ്റി തോംപ്സണ്, വേ എന്നീ രണ്ടു ബ്രിട്ടീഷു ശാസ്ത്രജ്ഞന്മാര് നടത്തിയ ഗവേഷണത്തിന്റെ ഫലമായിട്ടാണ് അയോണ് വിനിമയം എന്ന പ്രതിഭാസത്തെക്കുറിച്ചു ലോകം ആദ്യമായി (1848-54) മനസ്സിലാക്കിയത്. വളങ്ങളില് അമോണിയ ഉപസ്ഥിതമായിരിക്കുന്നത് പ്രായേണ അമോണിയം | + | '''ചരിത്രം.''' വളര്ച്ചയ്ക്ക് അത്യന്താപേക്ഷിതമായ അമോണിയയെ ചെടികള് മണ്ണില്നിന്നു വലിച്ചെടുക്കുന്നത് എങ്ങനെയാണ് എന്ന വിഷയത്തെപ്പറ്റി തോംപ്സണ്, വേ എന്നീ രണ്ടു ബ്രിട്ടീഷു ശാസ്ത്രജ്ഞന്മാര് നടത്തിയ ഗവേഷണത്തിന്റെ ഫലമായിട്ടാണ് അയോണ് വിനിമയം എന്ന പ്രതിഭാസത്തെക്കുറിച്ചു ലോകം ആദ്യമായി (1848-54) മനസ്സിലാക്കിയത്. വളങ്ങളില് അമോണിയ ഉപസ്ഥിതമായിരിക്കുന്നത് പ്രായേണ അമോണിയം സള്ഫേറ്റ് രൂപത്തിലാണ്. വളം മണ്ണില് കലരുമ്പോള് ജലത്തിന്റെ സഹായം ലഭിച്ച് അമോണിയം സള്ഫേറ്റിലെ ധന അയോണായ അമോണിയം അയോണും മണ്ണിലെ ധന അയോണായ കാല്സിയം അയോണും കൈമാറ്റം ചെയ്യപ്പെടുന്നു: |
| - | [[Image:page143for1.png| | + | |
| + | [[Image:page143for1.png|300px]] | ||
| + | |||
ഇപ്രകാരം അമോണിയം സള്ഫേറ്റില്നിന്ന് അമോണിയ മണ്ണിലേക്കു പകരുകയും പിന്നീട് അത് മണ്ണില്നിന്നു ചെടി വലിച്ചെടുക്കുകയും ചെയ്യുന്നു. ഈ പ്രക്രിയയില് മണ്ണില് നടക്കുന്നത് കാല്സിയം, അമോണിയം എന്നീ അയോണുകള് തമ്മിലുള്ള വിനിമയമാണ്. ചരിത്രപ്രധാനമായ ഈ കണ്ടുപിടിത്തതിനുശേഷം 1876-ല് ലെംബര്ഗ് എന്ന ശാസ്ത്രജ്ഞന് അയോണ് വിനിമയം ഒരു ഉത്ക്രമണീയ (reversible) പ്രക്രിയയാണെന്നു തെളിയിച്ചു. ഉദാഹരണമായി ലൂസൈറ്റ് (lucite) എന്ന ഖനിജം (K<sub>2</sub>O, Al<sub>2</sub>O<sub>3</sub>, 4SiO<sub>2</sub>) ഉപ്പു (NaCl) വെള്ളംകൊണ്ട് നിക്ഷാളനം ചെയ്യുമ്പോള് അത് അനല്സൈറ്റ് (analcite) എന്ന ഖനിജ (Na<sub>2</sub>O, Al<sub>2</sub>O<sub>3</sub>, 4SiO<sub>2</sub>) മായി മാറുകയും നേരെമറിച്ച് അനല്സൈറ്റ് പൊട്ടാസിയം ക്ളോറൈഡ് കൊണ്ടു നിക്ഷാളനം ചെയ്യുമ്പോള് ലൂസൈറ്റ് ആയി മാറുകയും ചെയ്യുന്നു. | ഇപ്രകാരം അമോണിയം സള്ഫേറ്റില്നിന്ന് അമോണിയ മണ്ണിലേക്കു പകരുകയും പിന്നീട് അത് മണ്ണില്നിന്നു ചെടി വലിച്ചെടുക്കുകയും ചെയ്യുന്നു. ഈ പ്രക്രിയയില് മണ്ണില് നടക്കുന്നത് കാല്സിയം, അമോണിയം എന്നീ അയോണുകള് തമ്മിലുള്ള വിനിമയമാണ്. ചരിത്രപ്രധാനമായ ഈ കണ്ടുപിടിത്തതിനുശേഷം 1876-ല് ലെംബര്ഗ് എന്ന ശാസ്ത്രജ്ഞന് അയോണ് വിനിമയം ഒരു ഉത്ക്രമണീയ (reversible) പ്രക്രിയയാണെന്നു തെളിയിച്ചു. ഉദാഹരണമായി ലൂസൈറ്റ് (lucite) എന്ന ഖനിജം (K<sub>2</sub>O, Al<sub>2</sub>O<sub>3</sub>, 4SiO<sub>2</sub>) ഉപ്പു (NaCl) വെള്ളംകൊണ്ട് നിക്ഷാളനം ചെയ്യുമ്പോള് അത് അനല്സൈറ്റ് (analcite) എന്ന ഖനിജ (Na<sub>2</sub>O, Al<sub>2</sub>O<sub>3</sub>, 4SiO<sub>2</sub>) മായി മാറുകയും നേരെമറിച്ച് അനല്സൈറ്റ് പൊട്ടാസിയം ക്ളോറൈഡ് കൊണ്ടു നിക്ഷാളനം ചെയ്യുമ്പോള് ലൂസൈറ്റ് ആയി മാറുകയും ചെയ്യുന്നു. | ||
| വരി 13: | വരി 15: | ||
അയോണ്വിനിമയ പ്രക്രിയയെ വ്യാഖ്യാനിക്കുവാന് പ്രധാനമായി രണ്ടു സിദ്ധാന്തങ്ങള് പുറത്തു വന്നിട്ടുണ്ടെങ്കിലും ഇവ പൂര്ണമായും തൃപ്തികരമല്ല. അയോണ് വിനിമയത്തില് പലതരം അയോണുകള് തമ്മിലുള്ള വ്യത്യാസങ്ങളെ വ്യാഖ്യാനിക്കുവാനും ശ്രമങ്ങള് നടന്നിട്ടുണ്ട്. കുറഞ്ഞ സാന്ദ്രതയില് സാധാരണ താപനിലകളില് വിനിമയം ചെയ്യപ്പെടുന്ന അയോണിന്റെ മാത്ര അതിന്റെ സംയോജകതയെയും അണുസംഖ്യയെയും ആശ്രയിച്ചിരിക്കും. ഉദാഹരണങ്ങള്: | അയോണ്വിനിമയ പ്രക്രിയയെ വ്യാഖ്യാനിക്കുവാന് പ്രധാനമായി രണ്ടു സിദ്ധാന്തങ്ങള് പുറത്തു വന്നിട്ടുണ്ടെങ്കിലും ഇവ പൂര്ണമായും തൃപ്തികരമല്ല. അയോണ് വിനിമയത്തില് പലതരം അയോണുകള് തമ്മിലുള്ള വ്യത്യാസങ്ങളെ വ്യാഖ്യാനിക്കുവാനും ശ്രമങ്ങള് നടന്നിട്ടുണ്ട്. കുറഞ്ഞ സാന്ദ്രതയില് സാധാരണ താപനിലകളില് വിനിമയം ചെയ്യപ്പെടുന്ന അയോണിന്റെ മാത്ര അതിന്റെ സംയോജകതയെയും അണുസംഖ്യയെയും ആശ്രയിച്ചിരിക്കും. ഉദാഹരണങ്ങള്: | ||
| - | [[Image:page143for2.png| | + | |
| + | [[Image:page143for2.png|300px]] | ||
| + | |||
സംയോജകത ഏറുന്തോറും വിനിമയം ഏറുമെന്നു ഒന്നാമത്തെ ഉദാഹരണത്തിലും അണുസംഖ്യ വര്ധിക്കുന്തോറും വിനിമയം കൂടുമെന്നു രണ്ടാമത്തെ ഉദാഹരണത്തിലും വ്യക്തമാക്കിയിട്ടുണ്ട്. (Na = സോഡിയം, Ca = കാല്സിയം, Al = അലുമിനിയം, Th = തോറിയം, Li = ലിഥിയം, K = പൊട്ടാസിയം, Rb = റുബീഡിയം, Cs = സീസിയം). | സംയോജകത ഏറുന്തോറും വിനിമയം ഏറുമെന്നു ഒന്നാമത്തെ ഉദാഹരണത്തിലും അണുസംഖ്യ വര്ധിക്കുന്തോറും വിനിമയം കൂടുമെന്നു രണ്ടാമത്തെ ഉദാഹരണത്തിലും വ്യക്തമാക്കിയിട്ടുണ്ട്. (Na = സോഡിയം, Ca = കാല്സിയം, Al = അലുമിനിയം, Th = തോറിയം, Li = ലിഥിയം, K = പൊട്ടാസിയം, Rb = റുബീഡിയം, Cs = സീസിയം). | ||
Current revision as of 11:46, 14 നവംബര് 2014
അയോണ് വിനിമയം
Ion Exchange
പരസ്പര സമ്പര്ക്കത്തിലുള്ള ഒരു ഇലക്ട്രോലൈറ്റ് ലായനിയും അലേയ ഖര വസ്തുവും തമ്മില് ഒരേ ചാര്ജുള്ള അയോണുകള് കൈമാറ്റം ചെയ്യുന്ന പ്രക്രിയ. ഒരു രാസപ്രവര്ത്തനം തന്നെയാണ് ഇത്. ഖരവസ്തുവും ലായനിയും ചേര്ന്ന വ്യൂഹം രണ്ടു ലായനികളോ രണ്ടു വാതകങ്ങളോ ചേര്ന്നുണ്ടാവുന്നതുപോലുള്ള ഒരു സജാതീയവ്യൂഹം (homogeneous system) അല്ല; വിജാതീയ വ്യൂഹം (heterogeneous system) ആണ്. ഇലക്ട്രൊലൈറ്റ്-ലായനി എന്നതുകൊണ്ട് ഉദ്ദേശിക്കുന്നത് ലീനവസ്തുവിന്റെ അയോണുകള് സ്വതന്ത്രമായി സ്വച്ഛന്ദം ചലിച്ചുകൊണ്ടിരിക്കുന്ന ലായനി എന്നാണ്. സാധാരണയായി അയോണ് വിനിമയം എന്ന പ്രതിഭാസം വിജാതീയവ്യൂഹങ്ങളിലാണ് നടക്കുന്നത്. എങ്കിലും മറ്റു അന്തരാപ്രതലങ്ങളിലും (inter-faces) ഇതു നടക്കാറുണ്ട്. ഉദാഹരണമായി അന്യോന്യം കലര്ന്നുചേരാത്ത രണ്ടു ഇലക്ട്രൊലൈറ്റ് ലായനികളില് മൂന്നാമതൊരു ഇലക്ട്രൊലൈറ്റിന്റെ വിതരണം അയോണ് വിനിമയമായി പരിഗണിക്കപ്പെടുന്നു. സിലിക്കേറ്റുകള്, ഫോസ്ഫേറ്റുകള്, ഫ്ലൂറൈഡുകള്, സെലുലോസ്, കമ്പിളിപ്രോട്ടീനുകള്, റെസിനുകള്, ലിഗ്നിന്, ഗ്ലാസ് എന്നു വേണ്ട ബേരിയം സള്ഫേറ്റ്, സില്വര് ക്ലോറൈഡ് മുതലായ അവക്ഷിപ്തങ്ങളില്വരെ അയോണ് വിനിമയം നടക്കുന്നതായി കണ്ടുപിടിച്ചിട്ടുണ്ട്. ഈ പ്രതിഭാസം വിനിമയ-അധിശോഷണം (exchange adsorption) ആയും ക്ഷാരവിനിമയം (alkali exchange) ആയും വിവരിക്കപ്പെട്ടിരിക്കുന്നു.
ചരിത്രം. വളര്ച്ചയ്ക്ക് അത്യന്താപേക്ഷിതമായ അമോണിയയെ ചെടികള് മണ്ണില്നിന്നു വലിച്ചെടുക്കുന്നത് എങ്ങനെയാണ് എന്ന വിഷയത്തെപ്പറ്റി തോംപ്സണ്, വേ എന്നീ രണ്ടു ബ്രിട്ടീഷു ശാസ്ത്രജ്ഞന്മാര് നടത്തിയ ഗവേഷണത്തിന്റെ ഫലമായിട്ടാണ് അയോണ് വിനിമയം എന്ന പ്രതിഭാസത്തെക്കുറിച്ചു ലോകം ആദ്യമായി (1848-54) മനസ്സിലാക്കിയത്. വളങ്ങളില് അമോണിയ ഉപസ്ഥിതമായിരിക്കുന്നത് പ്രായേണ അമോണിയം സള്ഫേറ്റ് രൂപത്തിലാണ്. വളം മണ്ണില് കലരുമ്പോള് ജലത്തിന്റെ സഹായം ലഭിച്ച് അമോണിയം സള്ഫേറ്റിലെ ധന അയോണായ അമോണിയം അയോണും മണ്ണിലെ ധന അയോണായ കാല്സിയം അയോണും കൈമാറ്റം ചെയ്യപ്പെടുന്നു:
ഇപ്രകാരം അമോണിയം സള്ഫേറ്റില്നിന്ന് അമോണിയ മണ്ണിലേക്കു പകരുകയും പിന്നീട് അത് മണ്ണില്നിന്നു ചെടി വലിച്ചെടുക്കുകയും ചെയ്യുന്നു. ഈ പ്രക്രിയയില് മണ്ണില് നടക്കുന്നത് കാല്സിയം, അമോണിയം എന്നീ അയോണുകള് തമ്മിലുള്ള വിനിമയമാണ്. ചരിത്രപ്രധാനമായ ഈ കണ്ടുപിടിത്തതിനുശേഷം 1876-ല് ലെംബര്ഗ് എന്ന ശാസ്ത്രജ്ഞന് അയോണ് വിനിമയം ഒരു ഉത്ക്രമണീയ (reversible) പ്രക്രിയയാണെന്നു തെളിയിച്ചു. ഉദാഹരണമായി ലൂസൈറ്റ് (lucite) എന്ന ഖനിജം (K2O, Al2O3, 4SiO2) ഉപ്പു (NaCl) വെള്ളംകൊണ്ട് നിക്ഷാളനം ചെയ്യുമ്പോള് അത് അനല്സൈറ്റ് (analcite) എന്ന ഖനിജ (Na2O, Al2O3, 4SiO2) മായി മാറുകയും നേരെമറിച്ച് അനല്സൈറ്റ് പൊട്ടാസിയം ക്ളോറൈഡ് കൊണ്ടു നിക്ഷാളനം ചെയ്യുമ്പോള് ലൂസൈറ്റ് ആയി മാറുകയും ചെയ്യുന്നു.
ഇരുപതാം ശ.-ത്തിന്റെ തുടക്കത്തിലാണ് അയോണ് വിനിമയം എന്ന ആശയത്തിനു വ്യാവസായിക രംഗത്ത് പ്രയോജനമുണ്ടാകുവാന് തുടങ്ങിയത്. പ്രകൃതിയില്നിന്നു ലഭിക്കുന്നതും കൃത്രിമമായി നിര്മിക്കപ്പെടുന്നതും ആയ സിലിക്ക അടങ്ങിയ സിലിഷിയസ് വിനിമയികളില് (siliceous exchangers) റോബര്ട് ഗാന്സ് എന്ന ജര്മന് ശാസ്ത്രജ്ഞന് ചില പരീക്ഷണങ്ങള് (1905) നടത്തിനോക്കിയപ്പോള് കഠിനജലം മൃദൂകരിക്കുന്നതിന് (soften) അവ പ്രയോഗക്ഷമമാണെന്നു മനസ്സിലാക്കി. അയോണ് വിനിമയത്തിന്റെ തത്ത്വമുപയോഗിച്ചുകൊണ്ടുള്ള വ്യവസായം എന്ന നിലയില് 1935 വരെ ജലമൃദൂകരണം മാത്രമേ ഉണ്ടായിരുന്നുള്ളു.
1935-ല് ചില കൃത്രിമ കാര്ബണിക റെസിനുകള്ക്ക് എളുപ്പത്തില് അയോണ് വിനിമയം നടത്താനുള്ള ശേഷിയുണ്ടെന്ന് ആഡംസ്, ഹോംസ് എന്നിവര് കണ്ടുപിടിച്ചു. മാത്രമല്ല ആനയോണുകളെയോ (anions) കാറ്റയോണുകളെയോ (cations) പ്രത്യേകം പ്രത്യേകം കൈമാറ്റം ചെയ്യാന് കഴിവുള്ള ചില ഫിനോളിക് റെസിനുകള്, സള്ഫോണിക് റെസിനുകള്, അമിനൊ റെസിനുകള് മുതലായവ നിര്മിക്കാന് കഴിയുമെന്നും ഇവരുടെ പരീക്ഷണങ്ങള് മൂലം തെളിഞ്ഞു. ഏറെത്താമസിയാതെ ഈ റെസിനുകളുടെ സ്ഥിരത്വം (stability), ക്ഷമത (ability) തുടങ്ങിയ ബഹുമുഖഗുണങ്ങള് മനസ്സിലായതോടുകൂടി അയോണ് വിനിയമചരിത്രത്തില് ഒരു പുതിയ അധ്യായം ആരംഭിച്ചു. 1940-നു ശേഷം അമ്ളത, ക്ഷാരത, സരന്ധ്രത (porosity) എന്നീ സ്വഭാവങ്ങളില് വൈവിധ്യമുള്ള നിരവധി അയോണ് വിനിമയികള് ലഭ്യമാകുവാന് തുടങ്ങിയപ്പോള് അയോണ്വിനിമയ പ്രക്രിയയുടെ പ്രാധാന്യവും പ്രയോഗക്ഷമതയും വര്ധിച്ചു. ഒരു പ്രത്യേക ഉപയോഗത്തിനു യോജിച്ച സവിശേഷഭൗതിക-രാസഗുണങ്ങള് ഇണങ്ങിയ റെസിനുകള് രൂപകല്പന ചെയ്തു നിര്മിക്കുവാന് കഴിയുമെന്നു അടുത്തകാലത്തു നടത്തിയ പരീക്ഷണങ്ങള് തെളിയിച്ചിട്ടുണ്ട്. ഈ റെസിനുകള് ഉപയോഗത്തില് വന്നതിനുശേഷം അയോണ് വിനിമയത്തിന് രസതന്ത്ര ടെക്നോളജി, കൃഷി, ഔഷധശാസ്ത്രം എന്നീ തുറകളില് വ്യാപകമായ ഉപയോഗമുണ്ടായിട്ടുണ്ട്.
അയോണ്വിനിമയ പ്രക്രിയയെ വ്യാഖ്യാനിക്കുവാന് പ്രധാനമായി രണ്ടു സിദ്ധാന്തങ്ങള് പുറത്തു വന്നിട്ടുണ്ടെങ്കിലും ഇവ പൂര്ണമായും തൃപ്തികരമല്ല. അയോണ് വിനിമയത്തില് പലതരം അയോണുകള് തമ്മിലുള്ള വ്യത്യാസങ്ങളെ വ്യാഖ്യാനിക്കുവാനും ശ്രമങ്ങള് നടന്നിട്ടുണ്ട്. കുറഞ്ഞ സാന്ദ്രതയില് സാധാരണ താപനിലകളില് വിനിമയം ചെയ്യപ്പെടുന്ന അയോണിന്റെ മാത്ര അതിന്റെ സംയോജകതയെയും അണുസംഖ്യയെയും ആശ്രയിച്ചിരിക്കും. ഉദാഹരണങ്ങള്:
സംയോജകത ഏറുന്തോറും വിനിമയം ഏറുമെന്നു ഒന്നാമത്തെ ഉദാഹരണത്തിലും അണുസംഖ്യ വര്ധിക്കുന്തോറും വിനിമയം കൂടുമെന്നു രണ്ടാമത്തെ ഉദാഹരണത്തിലും വ്യക്തമാക്കിയിട്ടുണ്ട്. (Na = സോഡിയം, Ca = കാല്സിയം, Al = അലുമിനിയം, Th = തോറിയം, Li = ലിഥിയം, K = പൊട്ടാസിയം, Rb = റുബീഡിയം, Cs = സീസിയം).
വര്ഗീകരണം. ഇപ്പോള് ഉപയോഗത്തിലുള്ള അയോണ് വിനിമയികളായ പദാര്ഥങ്ങളെ താഴെ കാണുംവിധം തരം തിരിക്കാം:
1. പ്രകൃതിലഭ്യമായ മണലുകള്: ഉദാ. ഗ്ലോക്കൊണൈറ്റ് (ന്യൂ ജെഴ്സിയിലെ പച്ചമണല്).
2. കൃത്രിമമായ അലൂമിനൊ-സിലിക്കേറ്റുകള്.
3. കൃത്രിമമായ ഓര്ഗാനിക് റെസിനുകള്;
(a) ഫിനോള്, ആല്ഡിഹൈഡ്, സള്ഫോണിക് അമ്ലം എന്നിവയില്നിന്നുണ്ടാകുന്ന കാറ്റയോണ് വിനിമയ റെസിനുകള്.
(b) ആരൊമാറ്റിക് അമീന്, ഫോര്മാല്ഡിഹൈഡ് എന്നിവയില്നിന്നു നിര്മിക്കപ്പെടുന്ന അനയോണ് വിനിമയ റെസിനുകള്.
(c) സ്റ്റൈറീന്, ഡൈ ഫെനില്, ബെന്സീന് എന്നിവ ഒന്നിച്ചു പോളിമറീകരിച്ച് (polymerised) ഉണ്ടാക്കുന്ന കാറ്റയോണ്-ആനയോണ് വിനിമയ-റെസിനുകള്.
ഉപയോഗങ്ങള്. അയോണ് വിനിമയത്തിന്റെ സുപ്രധാനമായ ചില പ്രയോഗങ്ങള് താഴെ പറയുന്നവയാണ്:
1.ജലമൃദൂകരണം: കഠിനജലം ഒരു കാറ്റയോണ്വിനിമയകാരിയില്ക്കൂടി കടത്തിവിടുമ്പോള് ആ ജലത്തിലുള്ള കാല്സിയം (Ca++), മഗ്നീഷ്യം (Mg++) എന്നീ അയോണുകള് വിനിമയം ചെയ്യപ്പെടുകയും തത്സ്ഥാനത്ത് സോഡിയം അയോണുകളോ (Na+) ഹൈഡ്രജന് അയോണുകളോ (H+) പ്രതിസ്ഥാപിക്കപ്പെടുകയും ചെയ്യുന്നു. ഈ പ്രക്രിയയില് ആദ്യകാലത്ത് ഉപയോഗിച്ചുവന്നിരുന്ന പ്രാകൃതികമായ ഗ്ളോക്കൊണൈറ്റിനും കൃത്രിമമായ അലൂമിനൊ-സിലിക്കേറ്റുകള്ക്കു പകരം കൃത്രിമറെസിനുകള് ഉപയോഗിച്ചുതുടങ്ങിയതോടുകൂടി ജലമൃദുലീകരണപദ്ധതി വ്യവസായശാലകളിലും മുനിസിപ്പാലിറ്റികളിലും മാത്രമല്ല വീടുകളിലും നിര്വഹിക്കത്തക്ക ഒന്നായിത്തീര്ന്നിട്ടുണ്ട്.
2.ഡീ-അയോണൈസേഷന് (deionisation): ജലത്തിലുള്ള എല്ലാ അയോണുകളെയും നീക്കം ചെയ്ത് സംപരിശുദ്ധജലം അഥവാ ചാലകതാമാപി ജലം (conductometric) ഉണ്ടാക്കുന്നതിനാണ് ഈ പദ്ധതി ഉപയോഗിക്കുന്നത്. ജലം ആദ്യമായി ഒരു കാറ്റയോണ് വിനിമയ-റെസിനില്ക്കൂടി കടത്തിവിടുമ്പോള് അതിലെ കാറ്റയോണുകളെല്ലാം ഹൈഡ്രജന് അയോണുകള് (H+) കൊണ്ട് വിനിമയം ചെയ്യപ്പെടുന്നു. അനന്തരം ഈ ജലം ഒരു ആനയോണ് വിനിമയ-റെസിനിലൂടെ കടത്തിവിടുമ്പോള് അതിലെ ആനയോണുകളെല്ലാം നീങ്ങി തത്സ്ഥാനത്ത് ഹൈഡ്രോക്സില് അയോണുകള് (OH-) വന്നുചേരുന്നു. ഹൈഡ്രജന്, ഹൈഡ്രോക്സില് എന്നീ അയോണുകള് സംയോജിച്ച് ജലമായി മാറുന്നതുകൊണ്ട് ശുദ്ധജലം ലഭിക്കുകയും ചെയ്യുന്നു. അടുത്ത കാലത്തു കാറ്റയോണ് വിനിമയ-റെസിനും ആനയോണ് വിനിമയ-റെസിനും ചേര്ന്ന ഒരു മിശ്രിതം ഉപയോഗിച്ചുള്ള 'മോണൊബെഡ്ഡി-അയോണൈസേഷന്' പദ്ധതിയും ആവിഷ്കരിച്ചു നടപ്പിലാക്കിയിട്ടുണ്ട്. കുറച്ചുകാലത്തെ ഉപയോഗത്തിനുശേഷം പ്രയോജനശൂന്യമായിത്തീര്ന്ന റെസിനുകളെ വീണ്ടും ഉപയോഗയോഗ്യമാക്കുന്നതിനും ചില മാര്ഗങ്ങള് ഇന്നുകണ്ടുപിടിക്കപ്പെട്ടിരിക്കുന്നു.
3.മറ്റു ഉപയോഗങ്ങള്. അനയോണ് വിനിമയ-റെസിനുകള് ഉപയോഗിച്ചാണ് ഇന്നു സ്റ്റ്രെപ്ടൊമൈസിന് വന്തോതില് ശുദ്ധീകരിച്ചെടുക്കുന്നത്. കൂടാതെ വിറ്റാമിനുകള്, എന്സൈമുകള്, ഹോര്മോണുകള് എന്നിവ ശുദ്ധീകരിക്കുന്നതിനും യുറേനിയം പ്ലൂട്ടോണിയം മുതലായ മൂലകങ്ങളെ പൃഥക്കരിച്ച് സാന്ദ്രീകരിക്കുന്നതിനും പെപ്ടിക് അള്സര് (peptic ulcer) ചികിത്സക്കായും ഈ റെസിനുകള് ഉപയോഗിക്കപ്പെടുന്നു. റയോണ്-നിര്മാണം, വിദ്യുല്ലേപനം (electroplating) എന്നിവയിലെ അവശിഷ്ടങ്ങളില്നിന്നു ലോഹങ്ങള് വീണ്ടെടുക്കുന്നതിനും ഇവയെ വിനിയോഗിച്ചുവരുന്നു. ചില കൊളോയ്ഡുകള് ഉണ്ടാക്കുന്നതിനും ചില പ്രക്രിയകളില് ഉത്പ്രേരകങ്ങളായും മറ്റും ഈ റെസിനുകള് പ്രയോഗിക്കപ്പെടുന്നുണ്ട്. നോ: ജലമൃദൂകരണം, ക്രൊമാറ്റൊഗ്രാഫി
(ഡോ. പി.എസ്. രാമന്)